Articles sur la santé
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Publié le 02/02/2021
Y-a-t-il une (brève) vie après la vie ?
Un des principes du prélèvement d'organes sur donneurs cadavériques est que le donneur doit être déclaré mort avant le début du prélèvement d'organes. Nous voici rassurés !
Mais les critères de mort varient selon les pays et ne sont pas toujours aussi clairs qu’en France où le diagnostic de mort cérébrale est exigé. Ailleurs, le prélèvement est le plus souvent possible après la détermination neurologique de la mort selon les critères standard de la mort cérébrale mais parfois également après la détermination de la mort sur le plan circulatoire. La réalisation de prélèvements suivant la constatation du décès « circulatoire » après retrait des mesures de maintien de la vie est devenue plus fréquente, et les critères utilisés pour déterminer le décès dans ce contexte ont beaucoup varié. Aussi, cet article s’il n’est pas bien adapté à la pratique française, nous éclaire sur ce qui se passe chez nos voisins.
Ne pas confondre urgence et précipitation
La plupart des protocoles relatifs au don d'organes après constatation de la mort circulatoire recommandent 5 minutes d'observation de l'apnée et de l'absence de pouls déterminée par le moniteur du cathéter artériel, ce temps d’observation variant de 2 à 10 minutes en pratique. Passée ce laps de temps, en l’absence de tentative de rétablissement de la circulation et alors qu’il n’y a pas de reprise spontanée de la circulation, l’arrêt de la circulation est considéré comme permanent et le prélèvement d’organes peut commencer. Or, la durée minimale de l'absence de pouls requise avant le don d'organe après le diagnostic de mort circulatoire n'a pas été bien étudiée.
Lacune que s’est proposé de combler une étude observationnelle prospective menée sur des adultes « décédés » après le retrait planifié des mesures de maintien des fonctions vitales dans 20 services de soins intensifs de trois pays (Canada, Tchéquie, Pays-Bas). Les patients devaient être surveillés pendant 30 minutes après la constatation du décès, pour détecter une éventuelle reprise de l'activité électrique et pulsatile cardiaque, qui était signalée prospectivement par les cliniciens au chevet des patients. La pression artérielle continue et le tracé ECG enregistrés ont été en revanche examinés rétrospectivement pour confirmer les observations faites au chevet des patients et pour déterminer s'il y avait eu d'autres reprises de l'activité cardiaque.
Aucun patient ayant eu une reprise d'activité cardiaque n'a repris conscience ou n’a survécu
Au total, 1 999 donneurs potentiels ont été identifiés et 631 ont été inclus dans l'étude. Une reprise de l'activité cardiaque, du mouvement respiratoire ou des deux, confirmée par l'ECG, a été signalée cliniquement chez 5 patients (1 %). L'analyse rétrospective de l'ECG et des courbes de pression artérielle de 480 patients a permis de retouver 67 cas (14 %) de reprise de l'activité cardiaque après une période d'absence de pouls, y compris les 5 cas signalés par les cliniciens de chevet. La durée la plus longue après une période d'absence de pouls avant la reprise de l'activité cardiaque a été de 4 minutes 20 secondes. Le dernier complexe QRS a coïncidé avec le dernier pouls artériel chez 19 % des patients. Aucun patient ayant eu une reprise d'activité cardiaque n'a repris conscience ou n’a survécu.
Cependant, la reprise transitoire du pouls a bien eu lieu, ce qui laisse supposer que les processus physiologiques de survenue de la mort somatique après l'arrêt des mesures de maintien de la vie peuvent inclure occasionnellement des périodes de cessation et de reprise de l'activité électrique cardiaque et l'activité artérielle pulsatile.
Les cinq dernières minutes
Cette étude soutient l'actuelle recommandation de respecter une période d'observation de 5 minutes requise par la plupart des protocoles avant de procéder au prélèvement d'organes après détermination de la mort sur le plan circulatoire. Elle confirme également qu’une activité électrique cardiaque se poursuit en l'absence d'activité cardiaque pulsatile et qu’il faut attendre l'arrêt de l'activité ECG pour déterminer la mort circulatoire…
Dr Bernard-Alex Gaüzère
Référence
Dhananiet S et coll. : Resumption of Cardiac Activity after Withdrawal of Life-Sustaining Measures. N Engl J Med., 2021;384:345-52. DOI: 10.1056/NEJMoa2022713
_________
Publié le 02/02/2021
Pallier la pénurie de FFP2 par des masques bi-filtres en élastomère ?
La pandémie de Covid-19 a souligné la nécessité d’équiper les soignants de masques faciaux. Cependant, la pénurie de masques N95 (FFP2) a amené à en prolonger l’emploi au-delà des recommandations du constructeur, tandis que l’augmentation de prix en rendait l’usage prohibitif. La première parade a été de restériliser et réemployer mais cette approche a montré ses limites. Aussi les auteurs de Pennsylvanie ont-ils cherché à remplacer les N95 par des demi masques P100 de protection respiratoire bi-filtres en élastomère, associés à des purificateurs d’air (avec système d’entrée d’air à 360 degrés).
Le matériel a été testé dans un réseau comportant 9 hôpitaux et 2 200 lits, en accordant la priorité aux équipes en contact avec des patients en phase aiguë de Covid-19 (bloc d’urgences, soins intensifs, anesthésie-réanimation). La direction infirmière a programmé des tests d’ajustement ; peu à peu, la disponibilité des matériels a été étendue aux soignants de phase 2 (radiologie, pharmacie), et, finalement, les masques ont été régulièrement désinfectés avant réutilisation et assignés à des soignants spécifiques.
Une réduction des coûts de 90 %
Dans chaque hôpital, un coordinateur a été chargé de former les équipes par des démonstrations (directives imprimées, vidéos, essai personnel, pose et dépose) avant distribution des P100. De même, les services de stérilisation ont été entraînés au démontage et remontage des masques, le tout sous la supervision d’un coordonnateur qui confirmait les connaissances de tout un chacun sur chaque stade du processus (nettoyage, désinfection, etc.)
Un test d’ajustement a été pratiqué sur 1 962 soignants (avec 1 840 succès) après démaquillage ou rasage de près (selon les sexes). Après réussite de la pose du masque, on a effectué des tests d’étanchéité au moyen d’une cagoule. En cas d’échec, on a essayé des masques de tailles différentes, ou on est revenu aux masques N95 et aux purificateurs d’air.
Dans une unité de soins intensifs de 18 lits, à pression négative, il a été calculé que le nombre moyen d’entrées par jour dans une chambre était de 87, soit 87 masques N95 par chambre et 1 566 pour les 18 chambres. Grâce aux P100, ce chiffre a été ramené à 0.
Compte tenu du fait que les filtres des P100 ne nécessitent qu’un changement par mois, en retenant le coût de 3 $ par masque N95 et de 20 $ pour un P100 (et 10 $ par cartouche), on constate une réduction de coût de 90 % par l’application de ces masques.
Dr Jean-Fred Warlin
Référence
Chalikonda S et coll. : Implementation of an elastomeric mask program as a strategy to eliminate disposable N95 mask use and resterilization: results from a large academic medical center. J Am Coll Surg 2020; 231: 333-338.
Y-a-t-il une (brève) vie après la vie ?
Un des principes du prélèvement d'organes sur donneurs cadavériques est que le donneur doit être déclaré mort avant le début du prélèvement d'organes. Nous voici rassurés !
Mais les critères de mort varient selon les pays et ne sont pas toujours aussi clairs qu’en France où le diagnostic de mort cérébrale est exigé. Ailleurs, le prélèvement est le plus souvent possible après la détermination neurologique de la mort selon les critères standard de la mort cérébrale mais parfois également après la détermination de la mort sur le plan circulatoire. La réalisation de prélèvements suivant la constatation du décès « circulatoire » après retrait des mesures de maintien de la vie est devenue plus fréquente, et les critères utilisés pour déterminer le décès dans ce contexte ont beaucoup varié. Aussi, cet article s’il n’est pas bien adapté à la pratique française, nous éclaire sur ce qui se passe chez nos voisins.
Ne pas confondre urgence et précipitation
La plupart des protocoles relatifs au don d'organes après constatation de la mort circulatoire recommandent 5 minutes d'observation de l'apnée et de l'absence de pouls déterminée par le moniteur du cathéter artériel, ce temps d’observation variant de 2 à 10 minutes en pratique. Passée ce laps de temps, en l’absence de tentative de rétablissement de la circulation et alors qu’il n’y a pas de reprise spontanée de la circulation, l’arrêt de la circulation est considéré comme permanent et le prélèvement d’organes peut commencer. Or, la durée minimale de l'absence de pouls requise avant le don d'organe après le diagnostic de mort circulatoire n'a pas été bien étudiée.
Lacune que s’est proposé de combler une étude observationnelle prospective menée sur des adultes « décédés » après le retrait planifié des mesures de maintien des fonctions vitales dans 20 services de soins intensifs de trois pays (Canada, Tchéquie, Pays-Bas). Les patients devaient être surveillés pendant 30 minutes après la constatation du décès, pour détecter une éventuelle reprise de l'activité électrique et pulsatile cardiaque, qui était signalée prospectivement par les cliniciens au chevet des patients. La pression artérielle continue et le tracé ECG enregistrés ont été en revanche examinés rétrospectivement pour confirmer les observations faites au chevet des patients et pour déterminer s'il y avait eu d'autres reprises de l'activité cardiaque.
Aucun patient ayant eu une reprise d'activité cardiaque n'a repris conscience ou n’a survécu
Au total, 1 999 donneurs potentiels ont été identifiés et 631 ont été inclus dans l'étude. Une reprise de l'activité cardiaque, du mouvement respiratoire ou des deux, confirmée par l'ECG, a été signalée cliniquement chez 5 patients (1 %). L'analyse rétrospective de l'ECG et des courbes de pression artérielle de 480 patients a permis de retouver 67 cas (14 %) de reprise de l'activité cardiaque après une période d'absence de pouls, y compris les 5 cas signalés par les cliniciens de chevet. La durée la plus longue après une période d'absence de pouls avant la reprise de l'activité cardiaque a été de 4 minutes 20 secondes. Le dernier complexe QRS a coïncidé avec le dernier pouls artériel chez 19 % des patients. Aucun patient ayant eu une reprise d'activité cardiaque n'a repris conscience ou n’a survécu.
Cependant, la reprise transitoire du pouls a bien eu lieu, ce qui laisse supposer que les processus physiologiques de survenue de la mort somatique après l'arrêt des mesures de maintien de la vie peuvent inclure occasionnellement des périodes de cessation et de reprise de l'activité électrique cardiaque et l'activité artérielle pulsatile.
Les cinq dernières minutes
Cette étude soutient l'actuelle recommandation de respecter une période d'observation de 5 minutes requise par la plupart des protocoles avant de procéder au prélèvement d'organes après détermination de la mort sur le plan circulatoire. Elle confirme également qu’une activité électrique cardiaque se poursuit en l'absence d'activité cardiaque pulsatile et qu’il faut attendre l'arrêt de l'activité ECG pour déterminer la mort circulatoire…
Dr Bernard-Alex Gaüzère
Référence
Dhananiet S et coll. : Resumption of Cardiac Activity after Withdrawal of Life-Sustaining Measures. N Engl J Med., 2021;384:345-52. DOI: 10.1056/NEJMoa2022713
_________
Publié le 02/02/2021
Pallier la pénurie de FFP2 par des masques bi-filtres en élastomère ?
La pandémie de Covid-19 a souligné la nécessité d’équiper les soignants de masques faciaux. Cependant, la pénurie de masques N95 (FFP2) a amené à en prolonger l’emploi au-delà des recommandations du constructeur, tandis que l’augmentation de prix en rendait l’usage prohibitif. La première parade a été de restériliser et réemployer mais cette approche a montré ses limites. Aussi les auteurs de Pennsylvanie ont-ils cherché à remplacer les N95 par des demi masques P100 de protection respiratoire bi-filtres en élastomère, associés à des purificateurs d’air (avec système d’entrée d’air à 360 degrés).
Le matériel a été testé dans un réseau comportant 9 hôpitaux et 2 200 lits, en accordant la priorité aux équipes en contact avec des patients en phase aiguë de Covid-19 (bloc d’urgences, soins intensifs, anesthésie-réanimation). La direction infirmière a programmé des tests d’ajustement ; peu à peu, la disponibilité des matériels a été étendue aux soignants de phase 2 (radiologie, pharmacie), et, finalement, les masques ont été régulièrement désinfectés avant réutilisation et assignés à des soignants spécifiques.
Une réduction des coûts de 90 %
Dans chaque hôpital, un coordinateur a été chargé de former les équipes par des démonstrations (directives imprimées, vidéos, essai personnel, pose et dépose) avant distribution des P100. De même, les services de stérilisation ont été entraînés au démontage et remontage des masques, le tout sous la supervision d’un coordonnateur qui confirmait les connaissances de tout un chacun sur chaque stade du processus (nettoyage, désinfection, etc.)
Un test d’ajustement a été pratiqué sur 1 962 soignants (avec 1 840 succès) après démaquillage ou rasage de près (selon les sexes). Après réussite de la pose du masque, on a effectué des tests d’étanchéité au moyen d’une cagoule. En cas d’échec, on a essayé des masques de tailles différentes, ou on est revenu aux masques N95 et aux purificateurs d’air.
Dans une unité de soins intensifs de 18 lits, à pression négative, il a été calculé que le nombre moyen d’entrées par jour dans une chambre était de 87, soit 87 masques N95 par chambre et 1 566 pour les 18 chambres. Grâce aux P100, ce chiffre a été ramené à 0.
Compte tenu du fait que les filtres des P100 ne nécessitent qu’un changement par mois, en retenant le coût de 3 $ par masque N95 et de 20 $ pour un P100 (et 10 $ par cartouche), on constate une réduction de coût de 90 % par l’application de ces masques.
Dr Jean-Fred Warlin
Référence
Chalikonda S et coll. : Implementation of an elastomeric mask program as a strategy to eliminate disposable N95 mask use and resterilization: results from a large academic medical center. J Am Coll Surg 2020; 231: 333-338.
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Publié le 01/02/2021
Mystère à Manaus
Manaus, métropole brésilienne de 2,2 millions d’habitants en plein cœur de la jungle amazonienne et de la pandémie de Covid-19 pose une énigme épidémiologique qui soulève des hypothèses inquiétantes pour le reste de la planète. Le Brésil fait partie des pays qui ont plutôt mal géré l’épidémie, mais Manaus s’est particulièrement distinguée par une politique de laisser-aller, plus subie que voulue : le virus a eu ainsi la plus grande latitude pour circuler assez librement, les autorités locales ayant jugé que la ville et ses habitants ne survivraient pas économiquement et socialement à un confinement. Les gestes barrières ont été préconisés avec plus ou moins de conviction, au point que globalement étaient réunis la plupart des facteurs propres à favoriser l’immunité de groupe. C’est ce qui, semble-t-il, est arrivé : une étude de séroprévalence effectuée en octobre 2020 chez des donneurs de sang a révélé que 76 % d’entre eux avaient été infectés par le SARS-CoV-2. Un chiffre rassurant qui semblait bien indiquer l’acquisition d’une immunité collective capable de protéger la population des attaques futures du virus.
Janvier 2021 : un rebond épidémique inattendu
Or, au cours du mois de janvier 2021, l’augmentation brutale et massive des hospitalisations pour cause de Covid-19 est venue déjouer tous les pronostics : en un mois, le nombre des admissions a été multiplié par six après être resté parfaitement stable et relativement bas pendant les mois (mai- novembre 2020) qui ont suivi la première vague de l’épidémie dont le pic s’est situé en avril 2020.
Mystère à Manaus ? Oui, ce rebond épidémique surprend et amène à formuler, pour l’expliquer, au moins quatre théories qui d’ailleurs peuvent se combiner tout en laissant la porte ouverte à d’autres hypothèses.
En premier lieu, il se pourrait que l’intensité de la première vague épidémique ait été surestimée et que l’immunité de groupe n’ait pas été finalement atteinte. De plus, les donneurs de sang ne seraient pas vraiment représentatifs de la population générale de la ville et il existerait des incertitudes sur la valeur réelle de la séroprévalence qui est susceptible de varier significativement d’un quartier à l’autre en fonction de la situation sanitaire locale le plus souvent médiocre.
Baisse de l’immunité de groupe et/ou émergence de variants
Autre hypothèse : il se pourrait que l’immunité individuelle développée au moins six mois auparavant ait commencé à décroître en décembre 2020 suffisamment pour s’éloigner de l’immunité de groupe. Les changements de comportement ont-ils aussi joué un rôle ? Cela semble peu probable, car la mobilité des habitants a plutôt diminué à la fin de l’année 2020.
En troisième lieu, faut-il y voir les effets des nouveaux variants du SARS-CoV-2 qui mettraient en échec l’immunité de groupe développée au contact du virus originel ? Trois lignées récemment détectées (B.1.1.7, B.1.351 et P.1) pourraient y prétendre du fait que chacune d’entre elles présente une constellation de mutations potentiellement importantes d’un point de vue biologique. Deux d’entre elles circulent activement au Brésil (B.1.1.7 et P.1) dont l’une (P.1) a été détectée le 12 janvier 2021 à Manaus.
Le génome de cette dernière lignée abrite au moins une dizaine de mutations intéressant les gènes qui codent pour la protéine spike, dont E484K et N501K et la lignée P.2 d’identification encore plus récente a un profil génétique qui n’inspire pas plus de confiance. Or ces génomes ont été détectés chez des patients réinfectés par le virus, alors même qu’in vitro, les mutations semblent bien réduire le pouvoir neutralisant des anticorps de convalescents. La valse des variants qui s’abat désormais sur le monde inspire à juste titre les plus vives inquiétudes, même si sa répercussion sur l’efficacité des vaccins n’est pas connue.
Des lignées nouvelles envahissantes et préoccupantes
Enfin, les lignées du SARS-CoV-2 qui circulent avec la deuxième vague de l’épidémie seraient plus aisément transmissibles que les lignées qui se sont manifestées lors de la première vague. La lignée P.1 a d’abord été identifiée à Manaus et dans une étude préliminaire, il semble bien qu’en décembre 2020, sur un effectif restreint (n = 31), elle corresponde à 42 % des génomes identifiés, alors qu’elle était absente entre mars et novembre 2020 au sein de 26 prélèvements. Sa transmissibilité est mal connue, mais elle serait élevée en raison de la présence de plusieurs mutations partagées avec les mutants identifiés au Royaume-Uni et en Afrique du Sud et déjà réputés pour leur contagiosité.
Ces lignées nouvelles de SARS-CoV-2 sont à l’évidence préoccupantes à Manaus comme ailleurs, car elles peuvent alimenter des rebonds épidémiques brutaux et pires que les précédents du fait de leur contagiosité accrue et de leur résistance potentielle à une immunité de groupe acquise au contact d’antigènes différents. Sans parler d’une mise en échec potentielle des vaccins qui arrivent actuellement sur le marché et d’une virulence supérieure à l’origine d’une mortalité supérieure à celle induite par les premières lignées du virus.
Angoisse et perplexité
L’expérience immunologique à ciel ouvert de Manaus incite à préciser le plus rapidement possible les caractéristiques génétiques, immunologiques, cliniques et épidémiologiques des nouveaux variants du SARS-CoV-2 qui plongent la planète dans la perplexité et l’angoisse, aucun pays n’étant à l’abri du scénario brésilien. La surveillance sérologique et génomique généralisée est plus que jamais à l’ordre du jour à un moment où la pandémie reprend du poil de la bête, aidée en cela par la flexibilité que lui offrent les nouveaux variants et leur résistance potentielle face à tous les moyens mis en œuvre dans l’extrême urgence pour la contrer. Le succès de la vaccination dans l’induction éventuelle d’une immunité de groupe pourrait être sérieusement remis en question si certaines des hypothèses suscitées par l’énigme de Manaus se confirmaient.
L’efficacité vaccinale se limiterait alors à protéger les sujets les plus fragiles ou les plus vulnérables ce qui permettrait d’éviter la saturation des hôpitaux. Ce ne serait déjà pas si mal en attendant de pouvoir faire mieux…mais le mystère plane encore sur la métropole amazonienne confrontée à un désastre sanitaire d’une incroyable ampleur qui renvoie aux ravages des grandes épidémies du passé…alors qu’il n’existait ni médicaments ni vaccination.
Dr Philippe Tellier
Référence
Sabino EC et coll. : Resurgence of COVID-19 in Manaus, Brazil, despite high seroprevalence. Lancet 2021 (27 janvier) : publication avancée en ligne.doi.org/10.1016/ S0140-6736(21)00183-5.
Mystère à Manaus
Manaus, métropole brésilienne de 2,2 millions d’habitants en plein cœur de la jungle amazonienne et de la pandémie de Covid-19 pose une énigme épidémiologique qui soulève des hypothèses inquiétantes pour le reste de la planète. Le Brésil fait partie des pays qui ont plutôt mal géré l’épidémie, mais Manaus s’est particulièrement distinguée par une politique de laisser-aller, plus subie que voulue : le virus a eu ainsi la plus grande latitude pour circuler assez librement, les autorités locales ayant jugé que la ville et ses habitants ne survivraient pas économiquement et socialement à un confinement. Les gestes barrières ont été préconisés avec plus ou moins de conviction, au point que globalement étaient réunis la plupart des facteurs propres à favoriser l’immunité de groupe. C’est ce qui, semble-t-il, est arrivé : une étude de séroprévalence effectuée en octobre 2020 chez des donneurs de sang a révélé que 76 % d’entre eux avaient été infectés par le SARS-CoV-2. Un chiffre rassurant qui semblait bien indiquer l’acquisition d’une immunité collective capable de protéger la population des attaques futures du virus.
Janvier 2021 : un rebond épidémique inattendu
Or, au cours du mois de janvier 2021, l’augmentation brutale et massive des hospitalisations pour cause de Covid-19 est venue déjouer tous les pronostics : en un mois, le nombre des admissions a été multiplié par six après être resté parfaitement stable et relativement bas pendant les mois (mai- novembre 2020) qui ont suivi la première vague de l’épidémie dont le pic s’est situé en avril 2020.
Mystère à Manaus ? Oui, ce rebond épidémique surprend et amène à formuler, pour l’expliquer, au moins quatre théories qui d’ailleurs peuvent se combiner tout en laissant la porte ouverte à d’autres hypothèses.
En premier lieu, il se pourrait que l’intensité de la première vague épidémique ait été surestimée et que l’immunité de groupe n’ait pas été finalement atteinte. De plus, les donneurs de sang ne seraient pas vraiment représentatifs de la population générale de la ville et il existerait des incertitudes sur la valeur réelle de la séroprévalence qui est susceptible de varier significativement d’un quartier à l’autre en fonction de la situation sanitaire locale le plus souvent médiocre.
Baisse de l’immunité de groupe et/ou émergence de variants
Autre hypothèse : il se pourrait que l’immunité individuelle développée au moins six mois auparavant ait commencé à décroître en décembre 2020 suffisamment pour s’éloigner de l’immunité de groupe. Les changements de comportement ont-ils aussi joué un rôle ? Cela semble peu probable, car la mobilité des habitants a plutôt diminué à la fin de l’année 2020.
En troisième lieu, faut-il y voir les effets des nouveaux variants du SARS-CoV-2 qui mettraient en échec l’immunité de groupe développée au contact du virus originel ? Trois lignées récemment détectées (B.1.1.7, B.1.351 et P.1) pourraient y prétendre du fait que chacune d’entre elles présente une constellation de mutations potentiellement importantes d’un point de vue biologique. Deux d’entre elles circulent activement au Brésil (B.1.1.7 et P.1) dont l’une (P.1) a été détectée le 12 janvier 2021 à Manaus.
Le génome de cette dernière lignée abrite au moins une dizaine de mutations intéressant les gènes qui codent pour la protéine spike, dont E484K et N501K et la lignée P.2 d’identification encore plus récente a un profil génétique qui n’inspire pas plus de confiance. Or ces génomes ont été détectés chez des patients réinfectés par le virus, alors même qu’in vitro, les mutations semblent bien réduire le pouvoir neutralisant des anticorps de convalescents. La valse des variants qui s’abat désormais sur le monde inspire à juste titre les plus vives inquiétudes, même si sa répercussion sur l’efficacité des vaccins n’est pas connue.
Des lignées nouvelles envahissantes et préoccupantes
Enfin, les lignées du SARS-CoV-2 qui circulent avec la deuxième vague de l’épidémie seraient plus aisément transmissibles que les lignées qui se sont manifestées lors de la première vague. La lignée P.1 a d’abord été identifiée à Manaus et dans une étude préliminaire, il semble bien qu’en décembre 2020, sur un effectif restreint (n = 31), elle corresponde à 42 % des génomes identifiés, alors qu’elle était absente entre mars et novembre 2020 au sein de 26 prélèvements. Sa transmissibilité est mal connue, mais elle serait élevée en raison de la présence de plusieurs mutations partagées avec les mutants identifiés au Royaume-Uni et en Afrique du Sud et déjà réputés pour leur contagiosité.
Ces lignées nouvelles de SARS-CoV-2 sont à l’évidence préoccupantes à Manaus comme ailleurs, car elles peuvent alimenter des rebonds épidémiques brutaux et pires que les précédents du fait de leur contagiosité accrue et de leur résistance potentielle à une immunité de groupe acquise au contact d’antigènes différents. Sans parler d’une mise en échec potentielle des vaccins qui arrivent actuellement sur le marché et d’une virulence supérieure à l’origine d’une mortalité supérieure à celle induite par les premières lignées du virus.
Angoisse et perplexité
L’expérience immunologique à ciel ouvert de Manaus incite à préciser le plus rapidement possible les caractéristiques génétiques, immunologiques, cliniques et épidémiologiques des nouveaux variants du SARS-CoV-2 qui plongent la planète dans la perplexité et l’angoisse, aucun pays n’étant à l’abri du scénario brésilien. La surveillance sérologique et génomique généralisée est plus que jamais à l’ordre du jour à un moment où la pandémie reprend du poil de la bête, aidée en cela par la flexibilité que lui offrent les nouveaux variants et leur résistance potentielle face à tous les moyens mis en œuvre dans l’extrême urgence pour la contrer. Le succès de la vaccination dans l’induction éventuelle d’une immunité de groupe pourrait être sérieusement remis en question si certaines des hypothèses suscitées par l’énigme de Manaus se confirmaient.
L’efficacité vaccinale se limiterait alors à protéger les sujets les plus fragiles ou les plus vulnérables ce qui permettrait d’éviter la saturation des hôpitaux. Ce ne serait déjà pas si mal en attendant de pouvoir faire mieux…mais le mystère plane encore sur la métropole amazonienne confrontée à un désastre sanitaire d’une incroyable ampleur qui renvoie aux ravages des grandes épidémies du passé…alors qu’il n’existait ni médicaments ni vaccination.
Dr Philippe Tellier
Référence
Sabino EC et coll. : Resurgence of COVID-19 in Manaus, Brazil, despite high seroprevalence. Lancet 2021 (27 janvier) : publication avancée en ligne.doi.org/10.1016/ S0140-6736(21)00183-5.
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Publié le 03/02/2021
Les (obscures) négociations entre l’Union Européenne et les laboratoires
Bruxelles, le mercredi 3 février 2021 – Entre préférence européenne, souci d’économie et lourdeur administrative, les difficiles négociations entre l’Union Européenne et les laboratoires pharmaceutiques pour l’achat de vaccin se dévoilent peu à peu.
Le divorce est entamé entre l’Union Européenne et AstraZeneca. Ce lundi, la Commission Européenne a indiqué qu’elle allait désormais principalement miser sur le vaccin du laboratoire Pfizer et de la firme allemande BionTech, dont elle a commandé 75 millions de doses supplémentaires. Cette décision intervient quelques jours après que AstraZeneca ait annoncé qu’il ne pourrait livrer que 25 des 100 millions de doses « promises » à l’Union Européenne pour le premier trimestre 2021. Face à la colère de Sandra Gallina, directrice générale de la Santé de la Commission, le président du laboratoire britannique assure qu’il a respecté son contrat avec l’Union Européenne, qui l’engage uniquement à « faire de son mieux » pour livrer l’Europe en vaccin.
Un bras de fer juridique qui pousse de plus en plus de parlementaires européens et d’associations à demander aux institutions européennes de lever le voile sur les négociations, jusque-là secrète, avec les laboratoires européens, au nom de la législation européenne sur l’accès au public des documents européens. Le médiateur européen a même ouvert une enquête pour « manquement à l’obligation de traiter les demandes d’accès public au document ». La pression commence à porter ses fruits puisque la Commission a déjà rendu public deux contrats, cependant en partie caviardée : celui avec le laboratoire allemand Curevac et celui avec AstraZeneca (pourquoi seulement ces deux-là ?).
Une usine à gaz administrative
Des premières révélations qui ont permis aux journalistes du Monde de refaire en partie l’histoire des négociations européennes sur les vaccins, dans un article publié ce mercredi. Démarré en juin dernier, le processus de négociations est parti d’une idée simple et louable : négocier ensemble l’achat des vaccins, afin d’éviter une concurrence interne entre les États membres et permettre aux pays les plus pauvres de l’Union d’avoir accès au vaccin. Mais entre la théorie et la pratique, il y a souvent un gap important et la négociation s’est rapidement transformée en une véritable usine à gaz. Aux institutions européennes classique, dont la direction générale de la Santé européenne, ce sont rajouté une kyrielle de commissions et de groupes de travail, certains communs à toute l’Union (comme le comité de pilotage pour l’achat des vaccins), d’autres ne regroupant que les États les plus importants.
Selon la plupart des observateurs, les négociateurs européens ont souvent été guidés plus par des préoccupations économiques que scientifiques. Ainsi, le vaccin d’AstraZeneca est rapidement devenu le chouchou de la Commission, en raison de son prix extrêmement bas (1,78 euros la dose contre 14,83 euros pour le vaccin Moderna) alors qu’il était loin d’être le vaccin le plus prometteur selon la plupart des scientifiques. Le 14 août, le laboratoire anglais est le premier à signer un contrat avec l’Union, pour 300 millions de doses.
Une stratégie européenne discutable
Une certaine préférence européenne semble également avoir guidé les négociateurs. Ainsi, le contrat passé avec Sanofi pour 300 millions de doses le 18 septembre « fait figure d’ovni » selon les journalistes du Monde, alors que les premières données sur le vaccin français étaient déjà à l’époque peu encourageantes. A l’inverse, les laboratoires Moderna et Pfizer, dont les vaccins ont les meilleurs résultats aujourd’hui, ne signent leur contrat avec l’Union Européenne que début novembre.
Les négociateurs justifient ce choix d’avoir favoriser les laboratoires européens. Selon eux, il s’agissait du seul moyen de s’assurer un approvisionnement rapide en vaccin, alors même que le Royaume-Uni et les Etats-Unis avaient, dans leurs contrats avec les laboratoires, signés des clauses empêchant l’exportation des vaccins produit sur leur sol. Mais le récent couac relatif au vaccin AstraZeneca semble révéler que ce choix n’était pas nécessairement le bon.
L’article du Monde révèle également comment les négociations ont été fortement ralenties par des débats liés à la responsabilité juridique des vaccins en cas d’effets secondaires. Officiellement, l’Union Européenne refusait que les laboratoires soient exonérés de toute responsabilité, comme c’est le cas aux Etats-Unis. En réalité, les négociateurs européens semblent avoir cédé sur ce point, puisque le contrat avec le laboratoire AstraZeneca stipule qu’il sera exonéré de toute responsabilité dès lors qu’il prouvera qu’il a fait « ses meilleurs efforts » pour assurer la sécurité du vaccin.
Au final, si l’Union Européenne a certes réussi à négocier de meilleurs prix que les Etats-Unis ou Israël, c’est peut-être au prix, justement, d’un moins bon approvisionnement en vaccin et d’une certaine incohérence dans les candidats retenus. Les dirigeants européens devront tirer les leçons de ces erreurs dans leur probable prochaine négociation en vue d’acheter des vaccins russes et chinois.
Quentin Haroche
__________________
Publié le 03/02/2021
Spoutnik V sur orbite ?
Après des effets de manche à l’Est et un scepticisme grandissant à l’Ouest voici une publication très attendue.
C’est l’utilisation d’un adénovirus recombinant qui a été choisie pour le vaccin russe (rAd), Gam-COVID-Vac (Spoutnik V). Celui-ci avait déjà montré un bon profil de sécurité et induit de fortes réponses immunitaires humorales et cellulaires chez les participants des essais cliniques de phase 1/2. Voici les résultats préliminaires sur l'efficacité et la sécurité issus de l'analyse intermédiaire de cet essai de phase 3 randomisé, en double aveugle et contrôlé par placebo dans 25 hôpitaux et polycliniques de Moscou (1).
Ont été inclus des participants âgés d'au moins 18 ans, présentant des tests de dépistages négatifs pour le VIH, les hépatites B et C, la syphilis, les SARS-Cov-2 (RT-PCR et sérologie) et sans antécédent de COVID-19 ou de contact avec une personne atteinte de COVID-19 au cours des 14 jours précédents. De plus chez les femmes en âge de procréer une méthode contraceptive efficace et un test de grossesse urinaire négatif étaient indispensables, les tests de dépistage de drogues et d'alcool devaient être négatifs et on ne devait retrouver aucun antécédent de réaction induite par un vaccin et aucune maladie infectieuse ou respiratoire aiguë dans les 14 jours précédant l’enrôlement. Les autres critères d'exclusion étaient les suivants : vaccination ou stéroïdes ou immunoglobulines dans les 30 jours précédents ; immunosuppression dans les 3 mois précédents ; allaitement ; syndrome coronarien aigu ou accident vasculaire cérébral dans l'année précédente ; tuberculose ou infections systémiques chroniques ; allergie ou hypersensibilité au médicament ou à ses composants ; néoplasies ; don de sang dans les 2 mois précédant l'inscription ; splénectomie ; neutropénie, agranulocytose, anémie sévère ou immunodéficience dans les 6 mois précédents ; forme active d'une maladie causée par le VIH, la syphilis ou l'hépatite B ou C ; anorexie ou déficit protéique ; tatouages importants au point d'injection ; antécédents d'alcoolisme ou de toxicomanie ; participation à tout autre essai clinique…
Plus de 20 000 Russes inclus
Les participants ont été répartis au hasard (3 pour 1) pour recevoir le vaccin ou le placebo, avec une stratification par groupe d'âge.
Le vaccin a été administré (0,5 mL/dose) par voie intramusculaire selon un schéma "prime-boost" avec un intervalle de 21 jours entre la première dose (rAd26) et la deuxième dose (rAd5), les deux vecteurs étant porteurs du gène de la glycoprotéine S complète du SRAS-CoV-2. L’objectif principal de l’étude qui était la mesure de la proportion de participants présentant une COVID-19 confirmée par PCR à partir du 21ème jour suivant la première dose, n’a été évalué que chez les participants qui avaient reçu deux doses de vaccin ou de placebo.
Les événements indésirables graves ont été évalués chez tous les participants qui avaient reçu au moins une dose au moment de la clôture de la base de données, et les événements indésirables rares ont été évalués chez tous les participants qui avaient reçu deux doses lors de la clôture de la base de données.
Entre le 7 septembre et le 24 novembre 2020, 21 977 adultes ont été assignés au hasard, soit au groupe vaccin (n=16 501), soit au groupe placebo (n=5 476). 19 866 qui ont reçu deux doses de vaccin ou de placebo et ont été inclus dans l'analyse du critère de jugement principal. Des comorbidités avec un risque connu de gravité de la COVID-19, étaient présentes chez environ un quart des participants.
À partir de 21 jours après la première dose de vaccin (le jour de la deuxième dose), 16 (0,1 %) des 14 964 participants du groupe vaccin et 62 (1,3 %) des 4 902 sujets du groupe placebo ont présenté une forme de COVID-19 symptomatique. L'efficacité du vaccin est donc de 91,6 % (IC 95 % : 85,6-95,2 %)… pour les formes symptomatiques.
Les courbes du taux d'incidence dans les deux groupes montrent que l'immunité requise pour prévenir la maladie symptomatique est apparue dans les 18 jours suivant la première dose. Cette protection a concerné toutes les tranches d'âge, y compris les personnes de plus de 60 ans, et les cas anecdotiques de personnes vaccinées mais infectées suggèrent que la gravité de la maladie diminue à mesure que l'immunité se développe.
Pas de détection régulière des formes asymptomatiques et sortie de l’essai des participants devenus asymptomatiques
Un test PCR a été effectué le jour de la deuxième dose (jour 21) pour le diagnostic des cas COVID-19 symptomatiques et asymptomatiques et les participants ne présentant pas de signes d'infection respiratoire ont été vaccinés avant la réception des résultats du test PCR. En cas de résultat positif au test PCR, les participants ont été classés comme asymptomatiques et n'ont pas été comptés comme des cas de COVID-19 dans l'analyse d'efficacité. Au cours de l'essai, à part la visite de dépistage et le jour de la deuxième dose, aucun autre test PCR n'a été effectué, sauf lorsque les participants ont signalé des symptômes de COVID-19.
Finalement, pas plus d’effets secondaires que les autres vaccins
La plupart des événements indésirables signalés étaient de grade 1 (7 485 [94,0 %] des 7 966 événements totaux). 45 (0,3 %) des 16 427 participants du groupe vaccin et 23 (0,4 %) des 5 435 participants du groupe placebo ont présenté des événements indésirables graves dont aucun n'a été considéré comme associé à la vaccination. Quatre décès ont été signalés au cours de l'étude (trois [<0,1 %] des 16 427 participants du groupe vaccin (à fortes comorbidités) et un [<0,1 %] des 5 435 participants du groupe placebo), dont aucun n'a été considéré comme lié au vaccin.
La charrue avant les bœufs : un vaccin déjà largement utilisé avant cette publication
Denis Y. Logunov et coll. concluent que cette analyse intermédiaire de phase 3 a donné des résultats prometteurs et que parallèlement à la mise en œuvre de multiples essais cliniques (Russie, Belarus, Émirats arabes unis, Inde), le vaccin a déjà été mis en circulation en Russie principalement dans les populations à risque, chez les personnels soignants et les enseignants. En date du 23 janvier 2021, plus de 2 millions de doses avaient déjà été administrées. Enfin, sont annoncées des recherches pour un régime à dose unique du vaccin, et cette perspective est vraiment très intéressante.
Quelques réserves
Pour le rédacteur de cet article du JIM (B-A G), il est incompréhensible que des tests RT-PCR n’aient été effectués (hormis systématiquement à J 21) que lorsque les participants ont développé des symptômes de la Covid, soit bien moins souvent que chez des joueurs de football professionnels ! En conséquence, l'analyse de l'efficacité ne porte que sur les cas symptomatiques et n’a donc pas répertorié systématiquement les cas asymptomatiques. Pire, en cas de résultat positif au test PCR, les participants ont été classés comme asymptomatiques et n'ont pas été comptés comme des cas de COVID-19 dans l'analyse d'efficacité, majorant ainsi artificiellement le taux d’efficacité annoncé de 91 %. Ce point ne semble pas avoir été relevé par les deux signataires enthousiastes de l’éditorial paru dans le Lancet (2). Des recherches complémentaires sur les cas asymptomatiques et la transmission s’avèrent donc nécessaires pour mieux évaluer l’efficacité réelle du vaccin. Néanmoins, l’objectif de protéger contre les formes modérées à sévères semble atteint.
Notons que 2 000 personnes de plus de 60 ans ont été incluses dans l’essai Spoutnik qui semble efficace dans cette tranche d’âge, alors que le débat fait rage pour le vaccin d’AstraZeneca qui n’en avait inclus que moins de 500 dans son essai de phase 3, d’où son rejet par l’Allemagne, l’Italie et la France (2/02/2021) pour vacciner les personnes âgées.
Signalons enfin qu’aucune donnée n’est fournie sur l’efficacité de Spoutnik sur les virus variants.
A la suite de cette publication du Lancet, l’Allemagne s’est officiellement proposée pour aider les Russes à préparer le dossier d’homologation auprès de l’Agence Européenne des Médicaments.
Dr Bernard-Alex Gaüzère
Références
1.Logunov D.Y. et coll. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia. The Lancet. Publication avancée en ligne le 2 février 2021 https://doi.org/10.1016/ S0140-6736(21)00234-8
2.Ian Jones, Polly Roy. Editorial : The Lancet. https://doi.org/10.1016/ S0140-6736(21)00191-4
jim.fr
Les (obscures) négociations entre l’Union Européenne et les laboratoires
Bruxelles, le mercredi 3 février 2021 – Entre préférence européenne, souci d’économie et lourdeur administrative, les difficiles négociations entre l’Union Européenne et les laboratoires pharmaceutiques pour l’achat de vaccin se dévoilent peu à peu.
Le divorce est entamé entre l’Union Européenne et AstraZeneca. Ce lundi, la Commission Européenne a indiqué qu’elle allait désormais principalement miser sur le vaccin du laboratoire Pfizer et de la firme allemande BionTech, dont elle a commandé 75 millions de doses supplémentaires. Cette décision intervient quelques jours après que AstraZeneca ait annoncé qu’il ne pourrait livrer que 25 des 100 millions de doses « promises » à l’Union Européenne pour le premier trimestre 2021. Face à la colère de Sandra Gallina, directrice générale de la Santé de la Commission, le président du laboratoire britannique assure qu’il a respecté son contrat avec l’Union Européenne, qui l’engage uniquement à « faire de son mieux » pour livrer l’Europe en vaccin.
Un bras de fer juridique qui pousse de plus en plus de parlementaires européens et d’associations à demander aux institutions européennes de lever le voile sur les négociations, jusque-là secrète, avec les laboratoires européens, au nom de la législation européenne sur l’accès au public des documents européens. Le médiateur européen a même ouvert une enquête pour « manquement à l’obligation de traiter les demandes d’accès public au document ». La pression commence à porter ses fruits puisque la Commission a déjà rendu public deux contrats, cependant en partie caviardée : celui avec le laboratoire allemand Curevac et celui avec AstraZeneca (pourquoi seulement ces deux-là ?).
Une usine à gaz administrative
Des premières révélations qui ont permis aux journalistes du Monde de refaire en partie l’histoire des négociations européennes sur les vaccins, dans un article publié ce mercredi. Démarré en juin dernier, le processus de négociations est parti d’une idée simple et louable : négocier ensemble l’achat des vaccins, afin d’éviter une concurrence interne entre les États membres et permettre aux pays les plus pauvres de l’Union d’avoir accès au vaccin. Mais entre la théorie et la pratique, il y a souvent un gap important et la négociation s’est rapidement transformée en une véritable usine à gaz. Aux institutions européennes classique, dont la direction générale de la Santé européenne, ce sont rajouté une kyrielle de commissions et de groupes de travail, certains communs à toute l’Union (comme le comité de pilotage pour l’achat des vaccins), d’autres ne regroupant que les États les plus importants.
Selon la plupart des observateurs, les négociateurs européens ont souvent été guidés plus par des préoccupations économiques que scientifiques. Ainsi, le vaccin d’AstraZeneca est rapidement devenu le chouchou de la Commission, en raison de son prix extrêmement bas (1,78 euros la dose contre 14,83 euros pour le vaccin Moderna) alors qu’il était loin d’être le vaccin le plus prometteur selon la plupart des scientifiques. Le 14 août, le laboratoire anglais est le premier à signer un contrat avec l’Union, pour 300 millions de doses.
Une stratégie européenne discutable
Une certaine préférence européenne semble également avoir guidé les négociateurs. Ainsi, le contrat passé avec Sanofi pour 300 millions de doses le 18 septembre « fait figure d’ovni » selon les journalistes du Monde, alors que les premières données sur le vaccin français étaient déjà à l’époque peu encourageantes. A l’inverse, les laboratoires Moderna et Pfizer, dont les vaccins ont les meilleurs résultats aujourd’hui, ne signent leur contrat avec l’Union Européenne que début novembre.
Les négociateurs justifient ce choix d’avoir favoriser les laboratoires européens. Selon eux, il s’agissait du seul moyen de s’assurer un approvisionnement rapide en vaccin, alors même que le Royaume-Uni et les Etats-Unis avaient, dans leurs contrats avec les laboratoires, signés des clauses empêchant l’exportation des vaccins produit sur leur sol. Mais le récent couac relatif au vaccin AstraZeneca semble révéler que ce choix n’était pas nécessairement le bon.
L’article du Monde révèle également comment les négociations ont été fortement ralenties par des débats liés à la responsabilité juridique des vaccins en cas d’effets secondaires. Officiellement, l’Union Européenne refusait que les laboratoires soient exonérés de toute responsabilité, comme c’est le cas aux Etats-Unis. En réalité, les négociateurs européens semblent avoir cédé sur ce point, puisque le contrat avec le laboratoire AstraZeneca stipule qu’il sera exonéré de toute responsabilité dès lors qu’il prouvera qu’il a fait « ses meilleurs efforts » pour assurer la sécurité du vaccin.
Au final, si l’Union Européenne a certes réussi à négocier de meilleurs prix que les Etats-Unis ou Israël, c’est peut-être au prix, justement, d’un moins bon approvisionnement en vaccin et d’une certaine incohérence dans les candidats retenus. Les dirigeants européens devront tirer les leçons de ces erreurs dans leur probable prochaine négociation en vue d’acheter des vaccins russes et chinois.
Quentin Haroche
__________________
Publié le 03/02/2021
Spoutnik V sur orbite ?
Après des effets de manche à l’Est et un scepticisme grandissant à l’Ouest voici une publication très attendue.
C’est l’utilisation d’un adénovirus recombinant qui a été choisie pour le vaccin russe (rAd), Gam-COVID-Vac (Spoutnik V). Celui-ci avait déjà montré un bon profil de sécurité et induit de fortes réponses immunitaires humorales et cellulaires chez les participants des essais cliniques de phase 1/2. Voici les résultats préliminaires sur l'efficacité et la sécurité issus de l'analyse intermédiaire de cet essai de phase 3 randomisé, en double aveugle et contrôlé par placebo dans 25 hôpitaux et polycliniques de Moscou (1).
Ont été inclus des participants âgés d'au moins 18 ans, présentant des tests de dépistages négatifs pour le VIH, les hépatites B et C, la syphilis, les SARS-Cov-2 (RT-PCR et sérologie) et sans antécédent de COVID-19 ou de contact avec une personne atteinte de COVID-19 au cours des 14 jours précédents. De plus chez les femmes en âge de procréer une méthode contraceptive efficace et un test de grossesse urinaire négatif étaient indispensables, les tests de dépistage de drogues et d'alcool devaient être négatifs et on ne devait retrouver aucun antécédent de réaction induite par un vaccin et aucune maladie infectieuse ou respiratoire aiguë dans les 14 jours précédant l’enrôlement. Les autres critères d'exclusion étaient les suivants : vaccination ou stéroïdes ou immunoglobulines dans les 30 jours précédents ; immunosuppression dans les 3 mois précédents ; allaitement ; syndrome coronarien aigu ou accident vasculaire cérébral dans l'année précédente ; tuberculose ou infections systémiques chroniques ; allergie ou hypersensibilité au médicament ou à ses composants ; néoplasies ; don de sang dans les 2 mois précédant l'inscription ; splénectomie ; neutropénie, agranulocytose, anémie sévère ou immunodéficience dans les 6 mois précédents ; forme active d'une maladie causée par le VIH, la syphilis ou l'hépatite B ou C ; anorexie ou déficit protéique ; tatouages importants au point d'injection ; antécédents d'alcoolisme ou de toxicomanie ; participation à tout autre essai clinique…
Plus de 20 000 Russes inclus
Les participants ont été répartis au hasard (3 pour 1) pour recevoir le vaccin ou le placebo, avec une stratification par groupe d'âge.
Le vaccin a été administré (0,5 mL/dose) par voie intramusculaire selon un schéma "prime-boost" avec un intervalle de 21 jours entre la première dose (rAd26) et la deuxième dose (rAd5), les deux vecteurs étant porteurs du gène de la glycoprotéine S complète du SRAS-CoV-2. L’objectif principal de l’étude qui était la mesure de la proportion de participants présentant une COVID-19 confirmée par PCR à partir du 21ème jour suivant la première dose, n’a été évalué que chez les participants qui avaient reçu deux doses de vaccin ou de placebo.
Les événements indésirables graves ont été évalués chez tous les participants qui avaient reçu au moins une dose au moment de la clôture de la base de données, et les événements indésirables rares ont été évalués chez tous les participants qui avaient reçu deux doses lors de la clôture de la base de données.
Entre le 7 septembre et le 24 novembre 2020, 21 977 adultes ont été assignés au hasard, soit au groupe vaccin (n=16 501), soit au groupe placebo (n=5 476). 19 866 qui ont reçu deux doses de vaccin ou de placebo et ont été inclus dans l'analyse du critère de jugement principal. Des comorbidités avec un risque connu de gravité de la COVID-19, étaient présentes chez environ un quart des participants.
À partir de 21 jours après la première dose de vaccin (le jour de la deuxième dose), 16 (0,1 %) des 14 964 participants du groupe vaccin et 62 (1,3 %) des 4 902 sujets du groupe placebo ont présenté une forme de COVID-19 symptomatique. L'efficacité du vaccin est donc de 91,6 % (IC 95 % : 85,6-95,2 %)… pour les formes symptomatiques.
Les courbes du taux d'incidence dans les deux groupes montrent que l'immunité requise pour prévenir la maladie symptomatique est apparue dans les 18 jours suivant la première dose. Cette protection a concerné toutes les tranches d'âge, y compris les personnes de plus de 60 ans, et les cas anecdotiques de personnes vaccinées mais infectées suggèrent que la gravité de la maladie diminue à mesure que l'immunité se développe.
Pas de détection régulière des formes asymptomatiques et sortie de l’essai des participants devenus asymptomatiques
Un test PCR a été effectué le jour de la deuxième dose (jour 21) pour le diagnostic des cas COVID-19 symptomatiques et asymptomatiques et les participants ne présentant pas de signes d'infection respiratoire ont été vaccinés avant la réception des résultats du test PCR. En cas de résultat positif au test PCR, les participants ont été classés comme asymptomatiques et n'ont pas été comptés comme des cas de COVID-19 dans l'analyse d'efficacité. Au cours de l'essai, à part la visite de dépistage et le jour de la deuxième dose, aucun autre test PCR n'a été effectué, sauf lorsque les participants ont signalé des symptômes de COVID-19.
Finalement, pas plus d’effets secondaires que les autres vaccins
La plupart des événements indésirables signalés étaient de grade 1 (7 485 [94,0 %] des 7 966 événements totaux). 45 (0,3 %) des 16 427 participants du groupe vaccin et 23 (0,4 %) des 5 435 participants du groupe placebo ont présenté des événements indésirables graves dont aucun n'a été considéré comme associé à la vaccination. Quatre décès ont été signalés au cours de l'étude (trois [<0,1 %] des 16 427 participants du groupe vaccin (à fortes comorbidités) et un [<0,1 %] des 5 435 participants du groupe placebo), dont aucun n'a été considéré comme lié au vaccin.
La charrue avant les bœufs : un vaccin déjà largement utilisé avant cette publication
Denis Y. Logunov et coll. concluent que cette analyse intermédiaire de phase 3 a donné des résultats prometteurs et que parallèlement à la mise en œuvre de multiples essais cliniques (Russie, Belarus, Émirats arabes unis, Inde), le vaccin a déjà été mis en circulation en Russie principalement dans les populations à risque, chez les personnels soignants et les enseignants. En date du 23 janvier 2021, plus de 2 millions de doses avaient déjà été administrées. Enfin, sont annoncées des recherches pour un régime à dose unique du vaccin, et cette perspective est vraiment très intéressante.
Quelques réserves
Pour le rédacteur de cet article du JIM (B-A G), il est incompréhensible que des tests RT-PCR n’aient été effectués (hormis systématiquement à J 21) que lorsque les participants ont développé des symptômes de la Covid, soit bien moins souvent que chez des joueurs de football professionnels ! En conséquence, l'analyse de l'efficacité ne porte que sur les cas symptomatiques et n’a donc pas répertorié systématiquement les cas asymptomatiques. Pire, en cas de résultat positif au test PCR, les participants ont été classés comme asymptomatiques et n'ont pas été comptés comme des cas de COVID-19 dans l'analyse d'efficacité, majorant ainsi artificiellement le taux d’efficacité annoncé de 91 %. Ce point ne semble pas avoir été relevé par les deux signataires enthousiastes de l’éditorial paru dans le Lancet (2). Des recherches complémentaires sur les cas asymptomatiques et la transmission s’avèrent donc nécessaires pour mieux évaluer l’efficacité réelle du vaccin. Néanmoins, l’objectif de protéger contre les formes modérées à sévères semble atteint.
Notons que 2 000 personnes de plus de 60 ans ont été incluses dans l’essai Spoutnik qui semble efficace dans cette tranche d’âge, alors que le débat fait rage pour le vaccin d’AstraZeneca qui n’en avait inclus que moins de 500 dans son essai de phase 3, d’où son rejet par l’Allemagne, l’Italie et la France (2/02/2021) pour vacciner les personnes âgées.
Signalons enfin qu’aucune donnée n’est fournie sur l’efficacité de Spoutnik sur les virus variants.
A la suite de cette publication du Lancet, l’Allemagne s’est officiellement proposée pour aider les Russes à préparer le dossier d’homologation auprès de l’Agence Européenne des Médicaments.
Les vaccins à vecteur adénoviral : qu’est-ce ?
Selon l'OMS, 64 candidats-vaccins sont en phase évaluation clinique (dont 13 en phase 3) et 173 en phase d’analyses précliniques. Parmi eux plusieurs vaccins à vecteur adénoviral.
Leur sécurité a été largement étudiée et des thérapeutiques à base de vecteurs adénoviraux sont déjà utilisées en clinique. Les antigènes délivrés par un vecteur adénoviral sont connus pour induire une immunité cellulaire et humorale après une seule dose. En outre, l'utilisation de deux doses donne une réponse immunitaire durable et de longue durée. Bien que les vaccins à vecteur adénoviral puissent induire des réponses immunitaires dirigées contre les composants du vecteur et atténuer celles induites par l'antigène, la vaccination hétérologue prime-boost avec deux vecteurs différents (comme dans le cas de Spoutnik) permet de minimiser cet effet. De plus, l'utilisation de deux sérotypes différents, qui sont administrés à 21 jours d'intervalle, vise à surmonter toute immunité préexistante contre l'adénovirus dans la population.
Ces vaccins ne nécessitent pas d'adjuvant et peuvent donner une bonne immunité après une seule dose. Leur robustesse physique est censée permettre un stockage à des températures d'environ -18 °C, ce qui est réalisable pour de nombreuses chaînes d'approvisionnement. L'inconvénient des vaccins recombinants à base d'adénovirus est qu'ils nécessitent des doses importantes, généralement 1010 ou 1011 particules, ce qui entraine des exigences importantes en matière de fabrication et de quantification pour le déploiement à l'échelle mondiale.
Dr Bernard-Alex Gaüzère
Références
1.Logunov D.Y. et coll. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia. The Lancet. Publication avancée en ligne le 2 février 2021 https://doi.org/10.1016/ S0140-6736(21)00234-8
2.Ian Jones, Polly Roy. Editorial : The Lancet. https://doi.org/10.1016/ S0140-6736(21)00191-4
jim.fr
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Publié le 09/03/2021
Le groupe A (et AB) rendrait plus vulnérable vis-à-vis de la Covid-19
Alors que les personnes du groupe O sont un peu protégées vis-à-vis du SARS-CoV-2, celles des groupes A et AB pourraient au contraire être plus vulnérables. A l'échelle de notre génome, de récentes études d'association ont identifié le locus responsable de l'expression du groupe sanguin ABO, comme l'un des plus importants prédicteurs génétiques du risque d'infection par le SARS-CoV-2. Bien que des études antérieures et ultérieures corroborent ces résultats, des données supplémentaires n'ont pas permis d'observer une association entre groupe sanguin ABO et infection par le SARS-CoV-2. Il est possible que des anticorps anti-groupe sanguin puissent également influencer l'infection par le SARS-CoV-2 du fait de la présence d'antigènes du groupe sanguin ABO à la surface du virus. Toutefois, ces anticorps peuvent être trouvés chez des individus de plusieurs groupes sanguins (par exemple, les anticorps anti-groupe sanguin B sont présents à la fois chez les individus du groupe sanguin A et du groupe sanguin O) et pourraient donc ne pas expliquer entièrement la propension des individus du groupe sanguin A, en particulier, à présenter un risque accru d'infection par le SARS-CoV-2.
Des mécanismes non élucidés
Dans cette étude, chaque domaine de liaison (RBD) du SARS-CoV-2 aux récepteurs de nos cellules a été cloné et purifié. Le RBD du SARS-CoV-2 a été incubé avec des cellules T HEK293 qui expriment l'enzyme de conversion de l'angiotensine 2 (ACE2), ou avec des hématies, puis détecté avec un anticorps anti-His (Anti-His-Tag mAb-Alexa Fluor 647) et soumis à une analyse cytométrique de flux. L'anticorps anti-A a également été utilisé pour détecter l'antigène A sur les hématies du groupe sanguin A. La liaison de la RBD aux puces à glycanes a été détectée par un anticorps anti-His, puis l'image a été générée par un scanner de puces.
Bien que la protéine de pointe S puisse faciliter l'entrée dans les cellules grâce aux interactions bien connues entre sa RBD et l'ACE2, il est possible que la RBD du SARS-CoV-2 interagisse avec d'autres molécules de l'hôte, y compris les antigènes des groupes sanguins, ce qui pourrait contribuer à la susceptibilité à la maladie. En particulier, la RBD du SARS-CoV-2 présente des caractéristiques structurelles générales similaires à celles des galectines, une ancienne famille de protéines de liaison aux glucides exprimées chez tous les métazoaires.
L'alignement des séquences a révélé des similitudes de séquence entre la RBD et l'ACE2 et les galectines humaines. Comme il a été démontré que les galectines présentent une grande affinité pour les antigènes de groupe sanguin, les auteurs ont ensuite examiné si la RBD du SARS-CoV-2 pouvait présenter une reconnaissance similaire des antigènes de groupe sanguin en examinant la liaison de la RBD avec des hématies isolées d’individus de groupe sanguin A, B ou O.
Des antigènes ABO de type I sur les cellules épithéliales respiratoires et de type II sur les hématies
En plus des antigènes du groupe sanguin ABO exprimés sur les hématies, appelés antigènes du groupe sanguin ABO de type II, des antigènes ABO de type I sont également exprimés sur divers autres tissus de l'organisme, y compris l'épithélium respiratoire mais sont subtilement, quoique fondamentalement différents de leurs homologues de type II en raison d'une configuration de liaison distincte entre l'avant-dernier résidu de galactose et la N-acétylglucosamine (type I, β1-3 ; type II, β1-4). Étant donné la voie d'infection aéroportée, le SARS-CoV-2 pourrait avoir développé une préférence spécifique pour les types d'antigènes ABO de type I exprimés le long des cellules épithéliales respiratoires. L’utilisation de puces à glycanes a permis d’élucider les spécificités fines des liaisons et de prédire avec précision les interactions avec de nombreux types de cellules.
Pas d’affinité particulière du virus pour les hématies du groupe A
Il en ressort que le domaine RBD du SARS-CoV-2 ne se lie que faiblement aux hématies humaines de tous types et ne montre aucune préférence pour les hématies du groupe sanguin A ou autres. En revanche, il se lie facilement aux cellules T HEK293 exprimant l'ACE2, et l'anticorps anti-A se lie également aux hématies du groupe sanguin A. Ainsi, la liaison significative de la RBD du SARS-CoV-2 aux structures du groupe sanguin A trouvées sur les hématies du groupe sanguin A humain ne semble pas contribuer à l'augmentation de la probabilité d'infection par le SARS-CoV-2 chez les individus du groupe sanguin A.
Des études antérieures ont démontré l'association entre l'expression du groupe sanguin ABO et l'infection par le SARS-CoV, de mécanisme encore inconnu. Bien que SARS-CoV et SARS-CoV-2 ne partagent que 73 % de leurs identités, ils présentent la même préférence de liaison au glycane ABO pour l'antigène A exprimé dans les voies respiratoires.
D’autres études pour confirmer ou infirmer
Toutefois, comme ces résultats ne démontrent pas de manière définitive que le groupe sanguin A « contribue » directement à l'infection par le SARS-CoV-2 et d’autres études sont certainement nécessaires pour approfondir ces premiers résultats et notamment pour confirmer que l'expression ABO influence l'adhésion du virus à différentes régions des voies naso-pharyngées et respiratoires, l'infection réelle de ces cellules de manière indépendante ou dépendante du récepteur ACE2, ou la stabilité globale du virus le long de la surface muqueuse.
En plus d'influencer potentiellement les interactions entre le SARS-CoV-2 et les cellules hôtes, l'impact de l'expression de l'antigène ABO sur les niveaux de facteur Von Willebrand pourrait également influer sur survenue des complications thromboemboliques.
Quoi qu’il en soit, les personne appartenant au groupe O (42 % en France) ont tout intérêt à continuer d’appliquer les gestes barrière pour se protéger, et celles des groupes A (45 % en France) et AB (4 % en France) à ne pas céder à la panique ou à la déprime.
Dr Bernard-Alex Gaüzère
Référence
Wu SC et coll. : The SARS-CoV-2 receptor-binding domain preferentially recognizes blood group A. Blood Adv. 2021;5 (5):1305-1309. doi:10.1182/bloodadvances.2020003259.
jim.fr
----
Publié le 11/12/2020
Contre la Covid-19, O rhésus moins
Il est admis que le groupe sanguin O tend à protéger contre l’infection respiratoire à SARS-CoV-2. Selon des travaux non publiés, le statut rhésus négatif (RH-) pourrait également être protecteur.
Du fait de des incertitudes persistantes à propos de ces associations, G Ray et collaborateurs ont mené un travail, basé sur l’analyse d’une cohorte de population, dans le but d’évaluer la fréquence des infections à SARS-CoV-2 et des formes graves de Covid-19 en fonction des groupes sanguins ABO et RH. Il s’agit d’une étude rétrospective, réalisée dans la province canadienne de l’Ontario, dans laquelle sont tenus plusieurs registres donnant accès à de multiples données d’ordre médical et permettant une centralisation des informations recueillies. Ont été concernés tous les individus ayant eu une détermination de leur groupe sanguin entre Janvier 2007 et Décembre 2019, puis qui, dans un temps ultérieur, ont été testés par polymerase chain reaction (PCR) pour rechercher l’ARN viral du SARS-CoV-2 entre le 15 Janvier et le 30 Juin 2020. L’objectif essentiel de l’étude était de déterminer la survenue d’une infection à SARS-CoV-2, définie par un test PCR positif. Le second était de préciser la fréquence d’un événement composite combinant formes graves de la Covid et décès. Une forme grave était définie par une admission en soins intensifs, une hospitalisation de 7 jours minimum, la survenue d’une nécrose myocardique ou d’une pneumonie virale dans les 14 jours précédant ou suivant la date de positivité du test PCR. L’analyse porte sur leur fréquence dans chacun des groupes sanguins, sur la comparaison groupe O vs tous les autres, sur la comparaison RH- vs RH+ ainsi que sur celle O- vs les autres groupes ABO. Les auteurs de la publication ont calculé les risques relatifs (RR) ainsi que les différences absolues de risque (ARD), ajustées à l’âge, au sexe, au lieu de domicile, aux comorbidités et autres antécédents médicaux majeurs dans les 5 années précédentes.
Il a aussi été procédé à une stratification en fonction de l’âge, avant et après 70 ans. Diverses analyses additionnelles tiennent compte de la possibilité de tests faux négatifs et du fait que les personnes ayant eu la détermination de leur groupe sanguin peuvent différer de la population générale.
Entre 2007 et 2019, une détermination de groupe sanguin a été effectuée chez 2 659 328 individus ; 2 432 151 n’ont pas, secondairement, eu de tests de laboratoire pour rechercher une infection à SARS-CoV-2 durant la période d’observation. Au total, la cohorte d’étude est composée de 225 556 personnes avec 36,3 % de sujets de groupe A, 14,9 % de groupe B et 44,3 % de groupe O. Le pourcentage de RH- se situe à 13,1 %. L’âge moyen était de 53,8 ans. On note 29 % d’hommes dans la cohorte. Treize à 15 % des personnes de l’ensemble avaient souffert d’une cardiopathie,11 % étaient porteurs d’une insuffisance rénale chronique, 21 % étaient anémiés et 27 à 29 % avaient un cancer. On retrouvait également 18 % d’asthme, 13 à 17 % de broncho pneumopathie chronique et 10 à 11 % de défaillance cardiaque. Les cas de démences, de diabète ou d’hypertension étaient aussi très fréquents.
Probabilité de 2 % d’être infecté pour les 0-, plus de 4 % pour les B-
Parmi les sujets de groupe O-, la probabilité d’avoir contracté une infection à SARS-CoV-2 s’est révélée minime, se situant à 2,1 % (intervalle de confiance à 95 % IC : 1,8- 2,3). A l’inverse, la probabilité la plus forte est retrouvée pour le groupe B-, à 4,2 % (IC : 4,0- 4,5) %. Le RR ajusté d’infection est plus élevé pour le type AB que pour le type A, calculé à 1,15 (IC : 1,03- 1,20) ou pour le type B, à 1,21 (IC : 1,13- 1,29). Le RR pour le type O se situe à 0,95 (IC : 0,91- 1,01). Quand la comparaison porte sur le groupe O vs l’ensemble des autres groupes le RR s’établit à 0,88 (IC : 0,84- 0,94) avec une ARD à – 3,9/ 100 (IC : -5,4 à – 2,5). Le statut RH – a aussi un effet protecteur contre les infections à SARS-CoV-2 avec un RR ajusté à 0,79 (IC : 0,73- 0,85), une ARD à – 6,8/ 1 000 (IC : - 8,9 à – 4,7). La protection la plus forte est observée dans le groupe O- avec un RR à 0,74 (IC : 0,66- 0,83) et une ARD à -8,2/1 000 (IC : -10,8à -5,31). Des analyses stratifiées en fonction de l’âge révèlent que l’impact des groupes O, RH- et O- est plus marqué chez les sujets jeunes que chez les plus de 70 ans.
On dénombre, au sein de la cohorte d’étude, 1 328 formes graves de Covid -19 ou de décès. Les pourcentages les plus élevés sont notés parmi les groupes AB et B. Ces derniers sont significativement à plus grand risque d’infections sévères que ceux de type A (aRR : 1,21 ; IC : 1,04- 1,40 et ARD à 1,2/ 1 000 ; IC: 0,2- 2,2). Par contre, quand l’incidence des cas graves dans le groupe O est comparée à celle dans tous les autres, l’aRR est à 0,87 (IC : 0,78- 0,97) et l’ARD se situe à – 0,8/ 1 000 (IC : - 1,4 à – 0,6). En comparaison avec les sujets RH+, ceux RH- ont un aRR plus faible d’évènements composites graves, à 0,82 (IC : 0,68- 0,96). Le groupe O- ne semble pas bénéficier d’une protection complémentaire spécifique avec un RR à 0,84 (IC : 0,64- 1,07).
Ce travail, avec un nombre considérable de tets SARS-CoV-2 effectués, confirme donc que les types sanguins O et RH- sont associés à un moindre risque d’infections à SARS-CoV-2 et de formes graves ou létales de Covid-19. Plusieurs points forts sont à relever. Le dépistage du SARS-CoV-2 était très large, non limité aux seuls sujets symptomatiques. La possibilité de tests PCR faussement négatifs a été prise en compte dans des analyses additionnelles. Mais des réserves sont aussi à émettre. Il a pu exister un biais de sélection car la détermination ABO-RH a précédé le dépistage SARS-CoV- 2. Les sujets les plus fragiles ont pu décéder avant la réalisation du test de dépistage. On peut aussi émettre l’hypothèse que le sujets O ou RH- aient pu être moins symptomatiques et aient pu échapper au dépistage. Les résultats de ce travail recoupent ceux d’une étude chinoise qui avait retrouvé un OR non ajusté à 0,67 (IC : 0,60- 0 ;7) en comparant le type O vs les autres groupes et ceux d’autres publications qui avaient analysé la fréquence des intubations ou de la nécessité de ventilation artificielle en fonction du statut des groupes sanguins. Point à remarquer, l’enquête a été réalisée dans une province canadienne multi ethnique mais l’origine des participants n’a pas été déterminée, une recherche ultérieure étant à mener dans des sous populations particulières, peut être à plus haut risque. Le travail n’a pas, non plus, précisé l’incidence des thrombo embolies veineuses.
Or, il est connu que les sujets O ont un taux plus bas de facteur VIII et de facteur Von Willebrand.
En conclusion, le type O est associé à un moindre risque d’infection par le SARS-CoV-2 et à un moindre risque de survenue d’une forme grave de Covid-19 ou de décès. Une protection minime contre ce virus pourrait donc être apportée par le groupe sanguin O et, possiblement aussi, par le type RH-. On ignore si ces données peuvent influer sur la prévention ou la prise en charge thérapeutiques des infections à ce virus.
Dr Pierre Margent
Référence
Ray J G t coll. : Association between ABO and RH Blood Groups and SARS-COV-2 and Severe COVID-19 Illness.. Annals Intern Med. , 2020 ; publication avancée en ligne le 24 novembre. doi: 10.7326/M20-4511.
jim.fr
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Newborn Antibodies to SARS-CoV-2 detected in cord blood after maternal vaccination
Paul Gilbert, View ORCID ProfileChad Rudnick
doi: https://doi.org/10.1101/2021.02.03.21250579
This article is a preprint and has not been peer-reviewed [what does this mean?]. It reports new medical research that has yet to be evaluated and so should not be used to guide clinical practice.
Abstract
Background Maternal vaccination for Influenza and TDaP have been well studied in terms of safety and efficacy for protection of the newborn by placental passage of antibodies. Similar newborn protection would be expected after maternal vaccination against SARS-CoV-2 (the virus responsible for COVID-19). There is a significant and urgent need for research regarding safety and efficacy of vaccination against SARS-CoV-2 during pregnancy. Here, we report the first known case of an infant with SARS-CoV-2 IgG antibodies detectable in cord blood after maternal vaccination.
Case presentation A vigorous, healthy, full-term female was born to a COVID-19 naïve mother who had received a single dose of mRNA vaccine for SARS-CoV-2 three weeks prior to delivery. Cord blood antibodies (IgG) were detected to the S-protein of SARS-CoV-2 at time of delivery.
Conclusion Here, we report the first known case of an infant with SARS-CoV-2 IgG antibodies detectable in cord blood after maternal vaccination.
Background
Maternal vaccination for Influenza and TDaP have been well studied in terms of safety and efficacy for protection of the newborn by placental passage of antibodies. Similar newborn protection would be expected after maternal vaccination against SARS-CoV-2 (the virus responsible for COVID-19). There is a significant and urgent need for research regarding safety and efficacy of vaccination against SARS-CoV-2 during pregnancy. Here, we report the first known case of an infant with SARS-CoV-2 IgG antibodies detectable in cord blood after maternal vaccination.
Methods
Maternal vaccination was provided to a COVID-19-naïve front-line healthcare worker with the Moderna mRNA COVID-19 vaccine, at gestational age of 36 weeks 3 days. A normal, spontaneous vaginal birth occurred 3 weeks after dose 1 of the Moderna vaccine. The product of this 39 week 3 days gestation was a vigorous, healthy, full-term girl with normal newborn nursery course and subsequent well-infant evaluation. Under aseptic conditions and along with standard cord blood sampling for newborn blood type and direct antiglobulin test (DAT) a cord blood sample was taken immediately after birth and prior to placenta delivery with 0.5mL drawn into a red-top tube for serum. The serum was sent for SARS-CoV-2 antibody test to the S-protein as performed by Labcorp. The mother, who has been breastfeeding exclusively, then received the second dose of the Moderna vaccine during the post-partum period per the normal 28-day vaccination protocol timeline.
Results
Cord blood antibodies (IgG) were detected to SARS-CoV-2 at a level of 1.31 U/mL. This Electrochemiluminescence Immunoassay (ECLIA) uses a recombinant protein representing the RBD (receptor-binding domain) of the S antigen for the quantitative determination of antibodies against SARS-CoV-21.
Discussion
Vaccination during pregnancy with TDaP and Flu is both well studied and formally recommended2-5. The COVID-19 Pandemic and subsequent EUAs for two mRNA vaccines have created significant need for active research regarding safety and efficacy in pregnant and lactating mothers, as well as their offspring6,7.
The novel mRNA vaccines theoretically will demonstrate similar safety in this population, including placental passage of protective antibodies. Natural SARS-CoV-2 infection, however, seems to confer lower than expected passage of antibodies to the fetus which may indicate newborns born to vaccinated mothers will remain at risk for infection8.
We have demonstrated that SARS-CoV-2 IgG antibodies are detectable in a newborn’s cord blood sample after only a single dose of the Moderna COVID-19 vaccine. Thus, there is potential for protection and infection risk reduction from SARS-CoV-2 with maternal vaccination. Quantification of the antibody response can help to determine the specific antibody titer and aid in longitudinal monitoring of the dynamics of the antibody response in individual patients. Protective efficacy in newborns and ideal timing of maternal vaccination remains unknown. Further studies will be needed to quantify the amount of viral neutralizing antibodies present in babies born to SARS-CoV-2 naïve mothers who are vaccinated prior to delivery. Additionally, the duration of antibody protection in this population is not yet known and serial total antibody measurements may be used to determine how long protection is expected which may help to determine when the best time would be to begin vaccination in newborns born to mothers who received a vaccine for SARS-CoV-2.
We urge other investigators to create pregnancy and breastfeeding registries as well as conduct efficacy and safety studies of the COVID-19 vaccines in pregnant and breastfeeding woman and their offspring.
References
1.↵Woo PC, Lau SK, Wong BH, et al. Differential Sensitivities of Severe Acute Respiratory Syndrome (SARS) Coronavirus Spike Polypeptide Enzyme-Linked Immunosorbent Assay (ELISA) and SARS Coronavirus Nucleocapsid Protein ELISA for Serodiagnosis of SARS Coronavirus Pneumonia. J Clin Microbiol. 2005 Jul;43(7):3054–3058
Abstract/FREE Full TextGoogle Scholar
2.↵ AJ Hardy-Fairbanks et al. Immune Responses in Infants Whose Mother Received Tdap Vaccine During Pregnancy. The Pediatric Infectious Disease Journal: November 2013 – Volume 32 – Issue 11 – p 1257–1260
CrossRefPubMedGoogle Scholar
3. T Walls et al. Infant outcomes after exposure to Tdap vaccine in pregnancy: an observation study. BMJ Open 2016;6:e009536.
Abstract/FREE Full TextGoogle Scholar
4. R Baxter et al. Effectiveness of vaccination during pregnancy to prevent infant pertussis. Pediatrics. 2017;139(5):e20164091
Abstract/FREE Full TextGoogle Scholar
5.↵ SB Black et al. Effectiveness of Influenza Vaccine during Pregnancy in Preventing Hospitalizations and Outpatient Visits for Respiratory Illness and in Pregnant Women and Their Infants. American Journal of Perinatology. 2004;21(6) p 333–339
CrossRefPubMedWeb of ScienceGoogle Scholar
6.↵Oliver S, Gargano J, Marin M, et al. The Advisory Committee on Immunization Practices’ Interim Recommendation for Use of Moderna COVID-19 Vaccine — United States, December 2020. MMWR Morb Mortal Wkly Rep 2021;69:1653–1656.
CrossRefGoogle Scholar
7.↵Vaccinating Pregnant and Lactating Patients Against COVID-19. ACOG Practice Advisory, December 2020.
Google Scholar
8.↵Edlow AG, Li JZ, Collier AY, et al. Assessment of Maternal and Neonatal SARS-CoV-2 Viral Load, Transplacental Antibody Transfer, and Placental Pathology in Pregnancies During the COVID-19 Pandemic. JAMA Netw Open. 2020;3(12):e2030455.
Google Scholar
__________________
Blood Type A Tied to SARS-CoV-2 Risks
By Marilynn Larkin
March 16, 2021
source: medscape
NEW YORK (Reuters Health) - Blood type A was associated with a greater risk of severe SARS-CoV-2 in one recent study and a higher risk of contracting the disease in another.
"The two studies are complementary," Dr. James Szymanski of Montefiore Medical Center and Albert Einstein College of Medicine in New York City, coauthor of one of the reports, told Reuters Health by email. "Our study adds support that blood group A may confer a higher risk, whereas the other study gives one possibility as to the 'how' part. That study provides evidence that the SARS-CoV-2 receptor binding domain (RBD) directly interacts with respiratory cells through the blood group A antigen."
"ABO blood type is a nonmodifiable risk factor, and current studies show the strength of the association as being limited," he noted. "Future studies need to prospectively confirm the association of ABO blood group with SARS-CoV-2 and further characterize the specific biological mechanisms that underlie it."
As reported in Transfusion, Dr. Szymanski and colleagues analyzed electronic health record data on close to 5,000 patients (mean age, 62; about 48% men) hospitalized or with an emergency department visit who received a positive nucleic acid test result for SARS-CoV-2 from March 10, 2020-June 8, 2020.
The all-cause mortality rate was 23%. To estimate overall risk by ABO type and account for the competing risks of in-hospital mortality and discharge, the team calculated the cumulative incidence function for each event. Cause-specific hazard ratios for in-hospital mortality and discharge were analyzed using multivariable Cox proportional hazards models to evaluate the effect of blood type after controlling for age, sex, body mass index, initial estimated glomerular filtration rate, and initial partial pressure of oxygen, as well as covariates.
Type A blood was associated with the increased cause-specific hazard of death among COVID-19 patients compared to type O (HR, 1.17) and type B (HR, 1.32).
Separately, Dr. Sean Stowell of Brigham and Women's Hospital in Boston and colleagues conducted a series of laboratory experiments to investigate the mechanism by which blood group antigens - particularly those of blood group A -might influence the risk for SARS-CoV-2 infection.
As reported in Blood Advances, the team studied the SARS-CoV-2 RBD protein, the part of the virus that attaches to the host cells. They assessed synthetic blood group antigens on respiratory and red blood cells found in blood groups A, B, and O and analyzed how the SARS-CoV-2 RBD interacted with each blood type.
They found that the RBD had a strong preference for binding to blood group A (but not to other blood types) on respiratory cells only, not red blood cells.
The team also tested whether the RBD of SARS-CoV, the virus that causes severe acute respiratory syndrome (SARS), had a similar preference, and indeed it did.
Like Dr. Szymanski, Dr. Stowell told Reuters Health, "whether blood group status truly influences the risk of SARS-CoV-2 infection or outcomes remains to be determined."
"There is no indication that patients should be managed differently because of their blood type," he said by email. "As our understanding regarding the possible influence of blood group antigens on SARS-CoV-2 infection grows, it may be possible in the future to leverage this information to develop strategies to reduce infection risk. However, many studies need to be done before it is clear whether such strategies may even be possible.
SOURCES: https://bit.ly/3vrZbDY Transfusion, online March 5, 2021, and https://bit.ly/3cuhrUI Blood Advances, online March 3, 2021.
Paul Gilbert, View ORCID ProfileChad Rudnick
doi: https://doi.org/10.1101/2021.02.03.21250579
This article is a preprint and has not been peer-reviewed [what does this mean?]. It reports new medical research that has yet to be evaluated and so should not be used to guide clinical practice.
Abstract
Background Maternal vaccination for Influenza and TDaP have been well studied in terms of safety and efficacy for protection of the newborn by placental passage of antibodies. Similar newborn protection would be expected after maternal vaccination against SARS-CoV-2 (the virus responsible for COVID-19). There is a significant and urgent need for research regarding safety and efficacy of vaccination against SARS-CoV-2 during pregnancy. Here, we report the first known case of an infant with SARS-CoV-2 IgG antibodies detectable in cord blood after maternal vaccination.
Case presentation A vigorous, healthy, full-term female was born to a COVID-19 naïve mother who had received a single dose of mRNA vaccine for SARS-CoV-2 three weeks prior to delivery. Cord blood antibodies (IgG) were detected to the S-protein of SARS-CoV-2 at time of delivery.
Conclusion Here, we report the first known case of an infant with SARS-CoV-2 IgG antibodies detectable in cord blood after maternal vaccination.
Background
Maternal vaccination for Influenza and TDaP have been well studied in terms of safety and efficacy for protection of the newborn by placental passage of antibodies. Similar newborn protection would be expected after maternal vaccination against SARS-CoV-2 (the virus responsible for COVID-19). There is a significant and urgent need for research regarding safety and efficacy of vaccination against SARS-CoV-2 during pregnancy. Here, we report the first known case of an infant with SARS-CoV-2 IgG antibodies detectable in cord blood after maternal vaccination.
Methods
Maternal vaccination was provided to a COVID-19-naïve front-line healthcare worker with the Moderna mRNA COVID-19 vaccine, at gestational age of 36 weeks 3 days. A normal, spontaneous vaginal birth occurred 3 weeks after dose 1 of the Moderna vaccine. The product of this 39 week 3 days gestation was a vigorous, healthy, full-term girl with normal newborn nursery course and subsequent well-infant evaluation. Under aseptic conditions and along with standard cord blood sampling for newborn blood type and direct antiglobulin test (DAT) a cord blood sample was taken immediately after birth and prior to placenta delivery with 0.5mL drawn into a red-top tube for serum. The serum was sent for SARS-CoV-2 antibody test to the S-protein as performed by Labcorp. The mother, who has been breastfeeding exclusively, then received the second dose of the Moderna vaccine during the post-partum period per the normal 28-day vaccination protocol timeline.
Results
Cord blood antibodies (IgG) were detected to SARS-CoV-2 at a level of 1.31 U/mL. This Electrochemiluminescence Immunoassay (ECLIA) uses a recombinant protein representing the RBD (receptor-binding domain) of the S antigen for the quantitative determination of antibodies against SARS-CoV-21.
Discussion
Vaccination during pregnancy with TDaP and Flu is both well studied and formally recommended2-5. The COVID-19 Pandemic and subsequent EUAs for two mRNA vaccines have created significant need for active research regarding safety and efficacy in pregnant and lactating mothers, as well as their offspring6,7.
The novel mRNA vaccines theoretically will demonstrate similar safety in this population, including placental passage of protective antibodies. Natural SARS-CoV-2 infection, however, seems to confer lower than expected passage of antibodies to the fetus which may indicate newborns born to vaccinated mothers will remain at risk for infection8.
We have demonstrated that SARS-CoV-2 IgG antibodies are detectable in a newborn’s cord blood sample after only a single dose of the Moderna COVID-19 vaccine. Thus, there is potential for protection and infection risk reduction from SARS-CoV-2 with maternal vaccination. Quantification of the antibody response can help to determine the specific antibody titer and aid in longitudinal monitoring of the dynamics of the antibody response in individual patients. Protective efficacy in newborns and ideal timing of maternal vaccination remains unknown. Further studies will be needed to quantify the amount of viral neutralizing antibodies present in babies born to SARS-CoV-2 naïve mothers who are vaccinated prior to delivery. Additionally, the duration of antibody protection in this population is not yet known and serial total antibody measurements may be used to determine how long protection is expected which may help to determine when the best time would be to begin vaccination in newborns born to mothers who received a vaccine for SARS-CoV-2.
We urge other investigators to create pregnancy and breastfeeding registries as well as conduct efficacy and safety studies of the COVID-19 vaccines in pregnant and breastfeeding woman and their offspring.
References
1.↵Woo PC, Lau SK, Wong BH, et al. Differential Sensitivities of Severe Acute Respiratory Syndrome (SARS) Coronavirus Spike Polypeptide Enzyme-Linked Immunosorbent Assay (ELISA) and SARS Coronavirus Nucleocapsid Protein ELISA for Serodiagnosis of SARS Coronavirus Pneumonia. J Clin Microbiol. 2005 Jul;43(7):3054–3058
Abstract/FREE Full TextGoogle Scholar
2.↵ AJ Hardy-Fairbanks et al. Immune Responses in Infants Whose Mother Received Tdap Vaccine During Pregnancy. The Pediatric Infectious Disease Journal: November 2013 – Volume 32 – Issue 11 – p 1257–1260
CrossRefPubMedGoogle Scholar
3. T Walls et al. Infant outcomes after exposure to Tdap vaccine in pregnancy: an observation study. BMJ Open 2016;6:e009536.
Abstract/FREE Full TextGoogle Scholar
4. R Baxter et al. Effectiveness of vaccination during pregnancy to prevent infant pertussis. Pediatrics. 2017;139(5):e20164091
Abstract/FREE Full TextGoogle Scholar
5.↵ SB Black et al. Effectiveness of Influenza Vaccine during Pregnancy in Preventing Hospitalizations and Outpatient Visits for Respiratory Illness and in Pregnant Women and Their Infants. American Journal of Perinatology. 2004;21(6) p 333–339
CrossRefPubMedWeb of ScienceGoogle Scholar
6.↵Oliver S, Gargano J, Marin M, et al. The Advisory Committee on Immunization Practices’ Interim Recommendation for Use of Moderna COVID-19 Vaccine — United States, December 2020. MMWR Morb Mortal Wkly Rep 2021;69:1653–1656.
CrossRefGoogle Scholar
7.↵Vaccinating Pregnant and Lactating Patients Against COVID-19. ACOG Practice Advisory, December 2020.
Google Scholar
8.↵Edlow AG, Li JZ, Collier AY, et al. Assessment of Maternal and Neonatal SARS-CoV-2 Viral Load, Transplacental Antibody Transfer, and Placental Pathology in Pregnancies During the COVID-19 Pandemic. JAMA Netw Open. 2020;3(12):e2030455.
Google Scholar
__________________
Blood Type A Tied to SARS-CoV-2 Risks
By Marilynn Larkin
March 16, 2021
source: medscape
NEW YORK (Reuters Health) - Blood type A was associated with a greater risk of severe SARS-CoV-2 in one recent study and a higher risk of contracting the disease in another.
"The two studies are complementary," Dr. James Szymanski of Montefiore Medical Center and Albert Einstein College of Medicine in New York City, coauthor of one of the reports, told Reuters Health by email. "Our study adds support that blood group A may confer a higher risk, whereas the other study gives one possibility as to the 'how' part. That study provides evidence that the SARS-CoV-2 receptor binding domain (RBD) directly interacts with respiratory cells through the blood group A antigen."
"ABO blood type is a nonmodifiable risk factor, and current studies show the strength of the association as being limited," he noted. "Future studies need to prospectively confirm the association of ABO blood group with SARS-CoV-2 and further characterize the specific biological mechanisms that underlie it."
As reported in Transfusion, Dr. Szymanski and colleagues analyzed electronic health record data on close to 5,000 patients (mean age, 62; about 48% men) hospitalized or with an emergency department visit who received a positive nucleic acid test result for SARS-CoV-2 from March 10, 2020-June 8, 2020.
The all-cause mortality rate was 23%. To estimate overall risk by ABO type and account for the competing risks of in-hospital mortality and discharge, the team calculated the cumulative incidence function for each event. Cause-specific hazard ratios for in-hospital mortality and discharge were analyzed using multivariable Cox proportional hazards models to evaluate the effect of blood type after controlling for age, sex, body mass index, initial estimated glomerular filtration rate, and initial partial pressure of oxygen, as well as covariates.
Type A blood was associated with the increased cause-specific hazard of death among COVID-19 patients compared to type O (HR, 1.17) and type B (HR, 1.32).
Separately, Dr. Sean Stowell of Brigham and Women's Hospital in Boston and colleagues conducted a series of laboratory experiments to investigate the mechanism by which blood group antigens - particularly those of blood group A -might influence the risk for SARS-CoV-2 infection.
As reported in Blood Advances, the team studied the SARS-CoV-2 RBD protein, the part of the virus that attaches to the host cells. They assessed synthetic blood group antigens on respiratory and red blood cells found in blood groups A, B, and O and analyzed how the SARS-CoV-2 RBD interacted with each blood type.
They found that the RBD had a strong preference for binding to blood group A (but not to other blood types) on respiratory cells only, not red blood cells.
The team also tested whether the RBD of SARS-CoV, the virus that causes severe acute respiratory syndrome (SARS), had a similar preference, and indeed it did.
Like Dr. Szymanski, Dr. Stowell told Reuters Health, "whether blood group status truly influences the risk of SARS-CoV-2 infection or outcomes remains to be determined."
"There is no indication that patients should be managed differently because of their blood type," he said by email. "As our understanding regarding the possible influence of blood group antigens on SARS-CoV-2 infection grows, it may be possible in the future to leverage this information to develop strategies to reduce infection risk. However, many studies need to be done before it is clear whether such strategies may even be possible.
SOURCES: https://bit.ly/3vrZbDY Transfusion, online March 5, 2021, and https://bit.ly/3cuhrUI Blood Advances, online March 3, 2021.
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
A lire Évènements thrombotiques après le vaccin AstraZeneca : et si c’était lié a une réponse immunitaire discordante ?
A lire Detecting Rapid Spread of SARS-CoV-2 Variants, France, January 26–February 16, 2021
______________
Publié le 01/04/2021
10 000 lits de réanimation : un pis-aller plutôt qu’une véritable promesse ?
Paris, le jeudi 1er avril 2021 – Évidemment, et il ne s’y attendait sans doute pas, Emmanuel Macron n’a pas su convaincre hier ceux qui parmi les médecins et les professionnels de santé espéraient des mesures très strictes pour faire face à l’épidémie de Covid. Ces praticiens suivent il est vrai une logique très différente de celle du chef de l’État : quand ils espèrent une élimination de la circulation du virus (Zéro Covid, qui nécessiterait des mesures drastiques prolongées), le Président de la République a affirmé hier qu’il s’est toujours inscrit dans la perspective de « vivre avec le virus ».
D’ailleurs, hier, le Président s’est bien gardé cette fois de fixer aucun objectif chiffré pour garantir la levée des mesures que ce soit en termes de nombre de contaminations ou de patients en réanimation.
En bonne voie, mais doit prouver l’efficacité de ses efforts
Pour beaucoup d’autres praticiens, plus modérés, et qui ont pour principale préoccupation de voir les services de réanimation pouvoir accueillir dans de bonnes conditions (et non pas toujours dans les moins mauvaises conditions) tous les patients (et pas seulement les sujets atteints de Covid), tout en préservant l’équilibre éducatif, social, économique et psychologique, les mesures modérées d’Emmanuel Macron ont le plus souvent suscité une certaine adhésion. Des interrogations demeurent néanmoins quant à l’efficacité réelle du « confinement aéré » qui désormais s’impose sur toute la France, étant donné le manque de recul, mais la fermeture simultanée de toutes les écoles pendant trois semaines (dont deux de vacances), parce qu’elle permet à la fois d’espérer un véritable frein à la circulation du virus et de limiter les conséquences pédagogiques et sociales semble considérée comme une mesure juste.
Un emplâtre sur une jambe de bois
Il est un point cependant qui suscite plus de circonspection, voire de crispation, c’est l’annonce de la libération de 10 000 lits de réanimation, contre aujourd’hui déjà plus de 7000 (pour une capacité initiale autour de 5000). « En juillet déjà, Olivier Véran avait annoncé 12 000 lits possibles pour la rentrée. Mais il y a un vrai déficit en personnel. Je ne sais pas comment le président compte résoudre ce problème. Mettre des gens non formés à ces techniques ne serait qu’un emplâtre sur une jambe de bois », s’irrite dans la Croix Bertrand Dureuil, chef du service de réanimation du CHU de Rouen.
Formations accélérées, respirateurs et stocks de curare
Si 10 000 places de réanimation peuvent être dégagées en France, il ne s’agit nullement de 10 000 lits répondant aux mêmes standards de qualité et de sécurité qu’habituellement. En outre, ce n’est qu’au prix de déprogrammations majeures qu’un tel niveau peut être atteint. Des efforts ont cependant été réalisés depuis le printemps dernier. Concernant le matériel, les lits de surveillance continue et les lits de réveil peuvent effectivement être transformés en lits de réanimation. Les respirateurs artificiels nécessaires ne manquent plus aujourd’hui : 10 000 ont bien été produits en 50 jours par un consortium de quatre industriels (Air Liquide, PSA, Valeo et Schneider Electric) qui s’était fixé ce pari ambitieux au printemps dernier. Par ailleurs, des stocks de curare ont été réalisés, ce qui devrait permettre d’éviter que se renouvellent les inquiétudes de la première vague.
Formation accélérée
Demeure l’épineux problème des personnels. Chaque vague épidémique entraîne son lot d’appels aux renforts, en sollicitant notamment personnels à la retraite, étudiants ou professionnels ayant momentanément cessé leur activité. En novembre « 12 000 professionnels de santé se sont portés volontaires pour prêter main forte dans les Ehpad et les hôpitaux. Les étudiants en santé, et les professionnels en formation sont également mobilisés » avait indiqué le ministre de la Santé. Même si ce chiffre pourrait ne pas être aussi élevé aujourd’hui, une réserve non négligeable existe encore néanmoins. Cependant, pour ceux qui seront mobilisés en réanimation, impossible d’improviser. Là encore, la situation n’est pas aussi périlleuse qu’en mars. Des centaines de formation accélérée ont en effet été dispensées (12 000 hospitaliers ont été formés par la Société européenne de soins intensifs pour soutenir les équipes d’USI en novembre et décembre). La semaine dernière en Ile-de-France ont en outre débuté des sessions express de trois jours qui s’adressent aux infirmiers et à 1 200 étudiants. Placement des patients en décubitus ventral, installation d’une ventilation mécanique, préparation des seringues de curare : certains gestes essentiels sont enseignés. Bien sûr, ces formations ne sont pas optimales et beaucoup de médecins mettent en garde contre un risque de soins dégradés.
Des déprogrammations problématiques
Cependant, pour la plupart, le principal risque de ce déploiement de 10 000 lits de réanimation concerne la déprogrammation. C’est notamment la préoccupation du professeur Bruno Mégarbane (AP-HP, Lariboisière). Il faut dire que sur ce point, les chiffres de 2020 récemment dévoilés par la Fédération hospitalière sont inquiétants. « La déprogrammation n’est pas une solution sans conséquence grave (…) Un nombre très important d’interventions lourdes voire vitales ont été déprogrammées sans être rattrapées en cours d’année » a ainsi déploré Zaynab Riet, déléguée générale de la FHF. Ainsi, 15 000 séjours en neurochirurgie et chirurgie du rachis n’ont pas été rattrapés, tandis que la transplantation rénale a reculé de 30 % « sans rattrapage notable ».
Ainsi, si 10 000 lits de réanimation pourront effectivement répondre si nécessaire à un nombre de patients encore plus élevé que lors de la première vague, afin notamment d’éviter le fameux « tri » qu’affirmaient imprudemment inéluctable quelques médecins, il ne s’agit nullement d’un véritable objectif vertueux mais plus certainement d’un pis-aller. Le gouvernement ne pourra pas faire l’impasse sur une véritable réflexion sur l’augmentation pérenne des capacités de réanimation de notre pays.
Aurélie Haroche
jim.fr
A lire Detecting Rapid Spread of SARS-CoV-2 Variants, France, January 26–February 16, 2021
______________
Publié le 01/04/2021
10 000 lits de réanimation : un pis-aller plutôt qu’une véritable promesse ?
Paris, le jeudi 1er avril 2021 – Évidemment, et il ne s’y attendait sans doute pas, Emmanuel Macron n’a pas su convaincre hier ceux qui parmi les médecins et les professionnels de santé espéraient des mesures très strictes pour faire face à l’épidémie de Covid. Ces praticiens suivent il est vrai une logique très différente de celle du chef de l’État : quand ils espèrent une élimination de la circulation du virus (Zéro Covid, qui nécessiterait des mesures drastiques prolongées), le Président de la République a affirmé hier qu’il s’est toujours inscrit dans la perspective de « vivre avec le virus ».
D’ailleurs, hier, le Président s’est bien gardé cette fois de fixer aucun objectif chiffré pour garantir la levée des mesures que ce soit en termes de nombre de contaminations ou de patients en réanimation.
En bonne voie, mais doit prouver l’efficacité de ses efforts
Pour beaucoup d’autres praticiens, plus modérés, et qui ont pour principale préoccupation de voir les services de réanimation pouvoir accueillir dans de bonnes conditions (et non pas toujours dans les moins mauvaises conditions) tous les patients (et pas seulement les sujets atteints de Covid), tout en préservant l’équilibre éducatif, social, économique et psychologique, les mesures modérées d’Emmanuel Macron ont le plus souvent suscité une certaine adhésion. Des interrogations demeurent néanmoins quant à l’efficacité réelle du « confinement aéré » qui désormais s’impose sur toute la France, étant donné le manque de recul, mais la fermeture simultanée de toutes les écoles pendant trois semaines (dont deux de vacances), parce qu’elle permet à la fois d’espérer un véritable frein à la circulation du virus et de limiter les conséquences pédagogiques et sociales semble considérée comme une mesure juste.
Un emplâtre sur une jambe de bois
Il est un point cependant qui suscite plus de circonspection, voire de crispation, c’est l’annonce de la libération de 10 000 lits de réanimation, contre aujourd’hui déjà plus de 7000 (pour une capacité initiale autour de 5000). « En juillet déjà, Olivier Véran avait annoncé 12 000 lits possibles pour la rentrée. Mais il y a un vrai déficit en personnel. Je ne sais pas comment le président compte résoudre ce problème. Mettre des gens non formés à ces techniques ne serait qu’un emplâtre sur une jambe de bois », s’irrite dans la Croix Bertrand Dureuil, chef du service de réanimation du CHU de Rouen.
Formations accélérées, respirateurs et stocks de curare
Si 10 000 places de réanimation peuvent être dégagées en France, il ne s’agit nullement de 10 000 lits répondant aux mêmes standards de qualité et de sécurité qu’habituellement. En outre, ce n’est qu’au prix de déprogrammations majeures qu’un tel niveau peut être atteint. Des efforts ont cependant été réalisés depuis le printemps dernier. Concernant le matériel, les lits de surveillance continue et les lits de réveil peuvent effectivement être transformés en lits de réanimation. Les respirateurs artificiels nécessaires ne manquent plus aujourd’hui : 10 000 ont bien été produits en 50 jours par un consortium de quatre industriels (Air Liquide, PSA, Valeo et Schneider Electric) qui s’était fixé ce pari ambitieux au printemps dernier. Par ailleurs, des stocks de curare ont été réalisés, ce qui devrait permettre d’éviter que se renouvellent les inquiétudes de la première vague.
Formation accélérée
Demeure l’épineux problème des personnels. Chaque vague épidémique entraîne son lot d’appels aux renforts, en sollicitant notamment personnels à la retraite, étudiants ou professionnels ayant momentanément cessé leur activité. En novembre « 12 000 professionnels de santé se sont portés volontaires pour prêter main forte dans les Ehpad et les hôpitaux. Les étudiants en santé, et les professionnels en formation sont également mobilisés » avait indiqué le ministre de la Santé. Même si ce chiffre pourrait ne pas être aussi élevé aujourd’hui, une réserve non négligeable existe encore néanmoins. Cependant, pour ceux qui seront mobilisés en réanimation, impossible d’improviser. Là encore, la situation n’est pas aussi périlleuse qu’en mars. Des centaines de formation accélérée ont en effet été dispensées (12 000 hospitaliers ont été formés par la Société européenne de soins intensifs pour soutenir les équipes d’USI en novembre et décembre). La semaine dernière en Ile-de-France ont en outre débuté des sessions express de trois jours qui s’adressent aux infirmiers et à 1 200 étudiants. Placement des patients en décubitus ventral, installation d’une ventilation mécanique, préparation des seringues de curare : certains gestes essentiels sont enseignés. Bien sûr, ces formations ne sont pas optimales et beaucoup de médecins mettent en garde contre un risque de soins dégradés.
Des déprogrammations problématiques
Cependant, pour la plupart, le principal risque de ce déploiement de 10 000 lits de réanimation concerne la déprogrammation. C’est notamment la préoccupation du professeur Bruno Mégarbane (AP-HP, Lariboisière). Il faut dire que sur ce point, les chiffres de 2020 récemment dévoilés par la Fédération hospitalière sont inquiétants. « La déprogrammation n’est pas une solution sans conséquence grave (…) Un nombre très important d’interventions lourdes voire vitales ont été déprogrammées sans être rattrapées en cours d’année » a ainsi déploré Zaynab Riet, déléguée générale de la FHF. Ainsi, 15 000 séjours en neurochirurgie et chirurgie du rachis n’ont pas été rattrapés, tandis que la transplantation rénale a reculé de 30 % « sans rattrapage notable ».
Ainsi, si 10 000 lits de réanimation pourront effectivement répondre si nécessaire à un nombre de patients encore plus élevé que lors de la première vague, afin notamment d’éviter le fameux « tri » qu’affirmaient imprudemment inéluctable quelques médecins, il ne s’agit nullement d’un véritable objectif vertueux mais plus certainement d’un pis-aller. Le gouvernement ne pourra pas faire l’impasse sur une véritable réflexion sur l’augmentation pérenne des capacités de réanimation de notre pays.
Aurélie Haroche
jim.fr
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Publié le 09/04/2021
Covid-19 : bon sang ne saurait mentir ?
Un première étude chinoise a suggéré que le groupe sanguin A était associé à une sensibilité accrue et le groupe sanguin O à une sensibilité réduite à l'infection par le SARS-CoV-2. Des études ultérieures menées en Italie et en Espagne l’ont confirmé. En revanche, des observations réalisées à Boston et à New York n'ont pas retrouvé d'association spécifique entre le groupe sanguin ABO et la maladie. La controverse soulevée par ces études aux résultats discordants a conduit à cette nouvelle étude cas-témoins dont l’objet était de vérifier de manière indépendante si le groupe sanguin est associé à la sensibilité au SARS-CoV-2 et à la gravité de la Covid-19.
Intermountain Healthcare, un système de soins de santé intégré à but non lucratif comprenant 24 hôpitaux et 215 cliniques dans l'Utah, l'Idaho et le Nevada, a constitué une base de données de dossiers médicaux électroniques spécifiques de la Covid-19. A partir de celle-ci ont été étudiées les données les personnes testées pour le SARS-CoV-2 entre le 3 mars et le 2 novembre 2020, et dont le groupe sanguin était mentionné : résultats positifs et négatifs des tests, patients hospitalisés et non hospitalisés, et patients admis en USI et les autres. L'infectivité a été déterminée par la RT-PCR sur des écouvillons nasaux ou des échantillons de salive.
Au total, 107 796 personnes (âge moyen [écart type ET], 42,0 [17,8] ans ; 82 875 [76,9 %] femmes) ont été incluses dans l'étude. Parmi les patients atteints de Covid-19, l'hospitalisation était associée au sexe masculin (1 165 hommes [50,1 %] hospitalisés versus 1 871 hommes [20,5 %] non hospitalisés) et à l'âge (âge moyen [ET] chez les patients hospitalisés, 57,0 [18,1] ans contre 41,4 [14,9] ans versus les personnes non hospitalisées).
L'admission en USI était également associée au sexe masculin (426 hommes [61,8 %] admis en USI versus 725 hommes [44,8 %] non admis) et à l'âge (âge moyen [écart type] chez les patients admis dans une USI ; 60,7 [158] ans versus 55,4 [18,8] ans chez les patients non admis. Les ethnies non blanches (Afro-Américains, Amérindiens ou autochtones d'Alaska, Amérindiens d'Hawaï ou des îles du Pacifique, Asiatiques) étaient associées à la détection du virus (1 592 personnes [13,9 %] avec des résultats positifs versus 6 610 personnes [6,9 %] avec des résultats négatifs) et à l'hospitalisation (556 patients [23,9 %] hospitalisés versus 1 036 personnes [11,3 %] non hospitalisées).
Le groupe sanguin n'est pas associé à la susceptibilité ou à la gravité de la maladie, à la présence du virus, à l'hospitalisation ou à l'admission en USI
Par rapport au groupe sanguin O, le groupe A n'était pas associé à une augmentation de la positivité des tests de détection du virus (Odds ratio OR, 0,97 [intervalle de confiance à 95 % IC à 95 %, 0,93-1,01] ; p = 0,11), de l'hospitalisation (OR, 0,89 [IC à 95 %, 0,80-0,99] ; p = 0,03) ou de l'admission en USI (OR, 0,84 [IC à 95 %, 0,69-1,02] ; p = 0,08). De même, les groupes B et AB n'étaient pas associés à des pronostics plus péjoratifs que le type O. Par contre, les analyses limitées à la race blanche ont donné des résultats similaires à ceux des études précédentes.
Comment expliquer ces résultats en opposition avec les études antérieures ?
Selon les auteurs, la taille réduite des échantillons et la nature rétrospective et observationnelle de nombreuses études antérieures, ainsi que l'hétérogénéité frappante des associations ABO avec la susceptibilité et la gravité des maladies, pourraient être dues à des variations fortuites, à un biais de publication, à des différences de bagage génétique, de géographie et d'environnement, et à des souches virales.
Le gène ABO est hautement polymorphe, et les groupes sanguins ABO sont distribués différemment selon l'ascendance et la géographie. Les différences de susceptibilité aux maladies pourraient être dues à des anticorps naturels ou à des effets pro-thrombotiques avec les individus n'appartenant pas au groupe O.
Cependant, les résultats de cette étude sont similaires à ceux des études précédentes en ce qui concerne les Blancs.
Compte tenu de la nature vaste et prospective de cette étude et de ses résultats les auteurs pensent que des liens entre Covid-19 et groupes ABO sont peu probables et ne seront pas des facteurs utiles pour statuer sur la prédisposition à la maladie ou sa gravité possible, que ce soit au niveau individuel ou au niveau de la population pour des environnements et des ascendances similaires. Des études supplémentaires, étroitement contrôlées pour la génétique, la géographie et la souche virale, sont nécessaires avant d'admettre que le groupe sanguin est un déterminant de la prédisposition à la Covid-19 ou de sa gravité. Fin de partie ?
Dr Bernard-Alex Gaüzère
Référence
Anderson JL et coll. : Association of Sociodemographic Factors and Blood Group Type With Risk of COVID-19 in a US Population. JAMA Netw Open. 2021;4(4):e217429. doi:10.1001/jamanetworkopen.2021.7429
____
Publié le 12/04/2021
Thromboses après vaccin AstraZeneca, la clé de l’énigme ?
La lutte contre la pandémie de Covid-19 liée au virus SARS-CoV-2 repose actuellement de façon prépondérante sur la vaccination à grande échelle. De décembre 2020 à mars 2021, quatre vaccins ont été autorisés par l'agence européenne sur la base des résultats issus d'essais prospectifs contrôlés réalisés en double aveugle: deux vaccins dits à ARN : -le BNT162b2 (Pfizer–BioNTech) et le mRNA-1273 (Moderna) - où l'ARN codant pour la protéine spike du virus SARS-CoV-2, encapsulé dans des nanoparticules lipidiques, est injecté, et deux vaccins où le génome codant pour la protéine spike du virus SARS-CoV-2 est inséré au génome d' un vecteur viral : un adénovirus recombinant du chimpanzé dans le cas du vaccin ChAdOx1 nCov-19 (AstraZeneca ) et un adénovirus recombinant de type 26 dans le cas du vaccin Ad26.COV2.S (Johnson & Johnson/Janssen).
Au 7 avril 2021, plus de 82 millions de personnes ont été vaccinées en Europe (1 ou 2 doses de vaccin) ; ainsi, en Allemagne, plus de 10 millions de personnes ont eu au moins une dose. Un quart de ces personnes environ a reçu le vaccin ChAdOx1 nCov-19 (AstraZeneca). En février plusieurs cas de thrombose après ce vaccin ont été rapportés.
Une première série de onze patients en Allemagne
En Allemagne, le premier cas observé mi-février 2021 a concerné une soignante de 49 ans sans antécédents particuliers ayant succombé à un « syndrome thrombotique » survenu dès 5 jours après l'administration du vaccin ChAdOx1 nCov-19 et qui s’est aggravé malgré le traitement anticoagulant, tableau constitué de thromboses extensives des vaisseaux splanchniques et même de microthromboses de l'aorte et des artères iliaques et d'une thrombose veineuse cérébrale (confirmées par les examens complémentaires et les données autopsiques). Plusieurs autres cas ont été observés et mi-mars 2021 dix autres cas étaient répertoriés. Le dernier cas inclus s'est révélé par un tableau d'hémorragie cérébrale à l’origine de laquelle une thrombose veineuse a été retenue, hypothèse dont la confirmation était en attente au moment de la publication de l'article.
Les caractéristiques sémiologiques des événements thrombotiques constatés dans cette première série de 11 patients (en incluant le cas princeps) sont donc les suivantes : le début survient de 5 j à 16 j après l'administration du vaccin ChAdOx1 nCov-19 ; il s'agit de thromboses veineuses cérébrales dans 9 cas, des veines splanchniques dans 3 cas, d'embolies pulmonaires dans 3 cas et de thromboses affectant d'autres territoires dans 4 cas. Sur 10 patients, 5 présentaient plus d'une thrombose. Une évolution fatale a été constatée dans 6 cas sur 10 répertoriés. Ainsi devant la gravité de ces événements thrombotiques de sémiologie atypique, la recherche du mécanisme physiopathologique s'imposait rapidement. Les résultats font l'objet de cet article.
Le tableau clinique évoque celui des thrombopénies induites par l’héparine
Dans cette série de patients, l’âge médian est de 36 ans (22-49 ans) et on note une prédominance féminine : 9 femmes pour 2 hommes. Il existait constamment une thrombopénie avec un nadir médian à 20 000 /μL environ (9000-103 000 /μL). Aucun patient n'avait reçu d'héparine préalablement. Le tableau clinique évoquait celui des thrombopénies induites par l'héparine où le développement d'anticorps anti PF4 -héparine induit l'activation des plaquettes et la survenue de thromboses. Le PF4 ou Facteur 4 plaquettaire est une glycoprotéine contenue dans les granules alpha des plaquettes, libérée à la surface de celles-ci lors de leur activation, présentant une grande affinité pour les glycosaminoglycans des membranes cellulaires et en particulier pour l'héparine. Dès lors les auteurs de l'article (experts internationaux pour certains dans ce domaine) ont recherché chez ces patients ces anticorps anti-PF4-héparine et anti PF4 par ELISA. Ils ont aussi développé un test d'activation plaquettaire in vitro PFA-dépendante où est mesuré le délai d'apparition de l'agrégation plaquettaire induite par le PF4, délai inversement proportionnel à l'intensité de l'activation plaquettaire.
Les résultats montrent une thrombopénie constante souvent sévère inférieure à 30 000/μL dans 7 cas /10 et associée à une coagulation
intravasculaire disséminée (CIVD) dans 5 cas diagnostiquée devant une forte augmentation des D-dimères, une altération des tests d'hémostase et une hypofibrinogénémie à des degrés divers. Hormis chez 1 patient ayant une anomalie V Leiden et des anticorps anticardiopides, il n'était pas mentionné d'anomalies prothrombotiques pré-existantes chez ces patients. Les tests ELISA anti-PF4 -héparine effectués chez 9 patients (dont le patient 11) étaient tous fortement positifs associés à un test d'activation plaquettaire positif d’intensité variable. Aucun des sujets contrôles n'avait de test d'activation plaquettaire positif. Les tests d'activation plaquettaire étaient négativés in vitro par de fortes doses d'héparine mais aussi de façon intéressante par l’ajout de l'anticorps monoclonal IV-3 ou par les immunoglobulines indiquant que l'activation plaquettaire observée était médiée par le récepteur Fcγ des immunoglobulines.
Tous les patients ont des anticorps anti-Facteur 4 plaquettaire
Ultérieurement, les auteurs ont étudié les sérums de patients qui leur étaient adressés parce qu'ayant présenté des thromboses post vaccin : au total 28 sérums ont été testés (comprenant ceux de l'étude initiale) : ils présentaient tous un test ELISA anti-PF4-héparine et un test ELISA anti-PF4 positifs et induisaient tous un test d'activation plaquettaire PF4 dépendante également positif. Dans deux cas, il a été possible de purifier par immunoaffinité l'anticorps anti-PF4 et de montrer qu'il induisait une forte activation plaquettaire induite spécifiquement par le PF4.
Ainsi le tableau thrombotique présenté par ces patients après vaccin évoque cliniquement un tableau de thrombopénie induite par l'héparine qui est due au développement d'anticorps dirigés contre les complexes multimoléculaires formés entre le PF4 cationique et l'héparine anionique. De fait il est retrouvé de façon constante chez les patients de cette étude des anticorps anti PF4-Héparine et anti PF4 par test ELISA. Néanmoins aucun patient n'avait reçu préalablement d'héparine ou un autre médicament polyanionique connu pour induire également ce type de thrombopénie. Il faut donc rapprocher le tableau de thrombopénie thrombotique présenté après vaccin par ces patients, caractérisé par la présence d'anticorps anti-PF4 et anti PF4-héparine (en dehors de toute administration d'héparine), de celui décrit au décours de certaines infections virales ou bactériennes voire après chirurgie prothétique du genou (1). Par rapport au tableau observé au cours des thrombopénies induites par l'héparine classiques, le tableau observé sans exposition préalable à l'héparine est souvent marqué par une thrombopénie particulièrement profonde, accompagnée de CIVD et compliquée de thromboses dans des territoires atypiques comme cela a été noté chez les patients de cette étude. A l'heure actuelle il est difficile de savoir si ces anticorps anti-PF4 sont des auto-anticorps développés dans le contexte de la forte réaction inflammatoire déclenchée par le vaccin ou des anticorps dirigés contre certains constituants du vaccin et présentant une réaction croisée avec le PF4. Il semble peu probable que l'adénovirus (virus par ailleurs connu pour être capable d'activer les plaquettes) présent à de très faibles concentrations dans le vaccin, ait été responsable d'une activation plaquettaire capable de déclencher un tel tableau thrombotique. Par contre le rôle de fragments d'ADN libre dans le vaccin n'est pas à exclure et ce d'autant plus que les auteurs ont montré antérieurement que des fragments d'ADN ou d'ARN étaient capables d'induire de tels anticorps anti PF4 -héparine dans un système murin (2).
Des immunoglobulines IV à fortes doses pour assurer la « clearance » des anticorps
Au plan clinique la connaissance de ce tableau et de son mécanisme sont de la première importance : ainsi devant la survenue d'une thrombopénie thrombotique chez un patient ayant reçu un vaccin 5 à 15 jours auparavant, la recherche d'anticorps anti PF4 s'impose, réalisable par ELISA ou immunodiffusion à grande échelle dans la plupart des laboratoires hospitaliers. La confirmation par un test fonctionnel d'activation plaquettaire PF4 dépendante avec inhibition in vitro par héparine est souhaitable. Néanmoins avant même les résultats de ces tests, l'administration d'immunoglobulines à fortes doses en intra-veineux peut être proposée dans ce contexte clinique ayant pour but d'accélérer la ''clearance'' des anticorps anti PF4 et la remontée du chiffre plaquettaire comme cela a pu être effectué au cours de thrombopénies induites par l'héparine classiques particulièrement sévères (3). Cette remontée du chiffre plaquettaire devrait faciliter la mise en route du traitement anticoagulant en proscrivant bien évidemment de façon formelle l'utilisation de l'héparine (sous toutes ses formes).
Le terme de ‘'vaccine-induced immune thrombotic thrombocytopenia (VITT)" soit "thrombopénie thrombotique immune induite par vaccin" est proposé par les auteurs.
Dr Sylvia Bellucci
Références
Greinacher A, et coll: Thrombotic Thrombocytopenia after ChAdOx1 nCov-19 Vaccination. N Engl J Med 2021; édition avancée du 9 avril 2021
1) Warkentin TE et al. : A spontaneous prothrombotic disorder resembling heparin-induced thrombocytopenia. Am J Med., 2008; 121: 632-6 36.
2) Jaax ME et al. : Complex formation with nucleic acids and aptamers alters the antigenic properties of platelet factor 4. Blood 2013; 122: 272-281.
3) Warkentin TE : High-dose intravenous immunoglobulin for the treatment and prevention of heparin-induced thrombocytopenia : a review. Expert Rev Hematol., 2019; 12: 685- 698.
jim.fr
____
CME / ABIM MOC / CE
What Are the Factors That Improve COVID Vaccine Antibody Response?
Authors: News Author: Miriam E. Tucker; CME Author: Charles P. Vega, MDFaculty and Disclosures
CME / ABIM MOC / CE Released: 4/2/2021
Valid for credit through: 4/2/2022
Note: The information on the coronavirus outbreak is continually evolving. The content within this activity serves as a historical reference to the information that was available at the time of this publication. We continue to add to the collection of activities on this subject as new information becomes available. It is the policy of Medscape Education to avoid the mention of brand names or specific manufacturers in accredited educational activities. However, manufacturer names related to COVID-19 vaccines may be provided in this activity to promote clarity. The use of manufacturer names should not be viewed as an endorsement by Medscape of any specific product or manufacturer.
Clinical Context
One of the most important and controversial issues in the fight against the COVID-19 pandemic is the temporary application of just 1 dose of the currently available messenger RNA (mRNA)-based vaccines in the United States instead of the currently authorized 2-dose regimen. Proponents of a single-dose strategy argue that these vaccines still are effective against COVID-19 when applied as a single dose, and the current crisis in the United States coupled with problems with vaccine distribution and application mandates a single-dose approach to get as many people vaccinated as soon as possible.
These supporters of a single dose have some good points. First, it is very likely that single dosing will result in more people being vaccinated. In addition, the emergency use authorizations for both the Pfizer-BioNTech[1] and Moderna[2] vaccines cited good vaccine efficacy in a single dose (82% and 80.2%, respectively); however, there are real risks associated with significant delay of a booster dose of these vaccines. Would the protected period against COVID-19 be shortened without a booster? In addition, could the booster provide the additional support necessary as new variants off SARS-CoV-2 emerge? Finally, it is possible that a less effective vaccine might help select for variants that are more vaccine-resistant and possibly more virulent overall.
This debate will continue, fueled by the epidemiology of COVID-19 and the logistical challenge of vaccinating hundreds of millions of people, but what about clinical variables that might affect vaccine efficacy? The current study addresses this issue.
Study Synopsis and Perspective
The capacity to mount humoral immune responses to COVID-19 vaccinations may be reduced among people who are heavier, older, and male, new findings suggest.
The data pertain specifically to the mRNA vaccine, BNT162b2, developed by Pfizer Inc. and BioNTech SE. The study was conducted by Italian researchers and was published February 26 as a preprint.[3]
The study involved 248 healthcare workers who each received 2 doses of the vaccine. Of the participants, 99.5% developed a humoral immune response after the second dose. Those responses varied by body mass index (BMI), age, and sex.
"The findings imply that female, lean and young people have an increased capacity to mount humoral immune responses compared to male, overweight and older populations," said Raul Pellini, professor at the IRCCS Regina Elena National Cancer Institute, Rome, Italy, and colleagues.
"To our knowledge, this study is the first to analyze Covid-19 vaccine response in correlation to BMI," they noted.
"Although further studies are needed, this data may have important implications to the development of vaccination strategies for COVID-19, particularly in obese people," they wrote.
If the data are confirmed by larger studies, "giving obese people an extra dose of the vaccine or a higher dose could be options to be evaluated in this population."
Results Contrast With Pfizer Trials of Vaccine
The BMI finding seemingly contrasts with final data from the phase 3 clinical trial of the vaccine, which were reported in a supplement index to an article published December 31, 2020, in the New England Journal of Medicine.[4] In that study, vaccine efficacy did not differ by obesity status.
Asked to comment, Akiko Iwasaki, PhD, professor of immunology at the Howard Hughes Medical Institute and an investigator at Yale University School of Medicine, New Haven, Connecticut, noted that although the current Italian study showed somewhat lower levels of antibodies in people with obesity compared with people who did not have obesity, the phase 3 trial found no difference in symptomatic infection rates.
"These results indicate that even with a slightly lower level of antibody induced in obese people, that level was sufficient to protect against symptomatic infection," Iwasaki told Medscape Medical News.
Indeed, Pellini and colleagues pointed out that responses to vaccines against influenza, hepatitis B, and rabies are also reduced in persons with obesity compared to lean individuals.
They said, however, that it was especially important to study the effectiveness of COVID-19 vaccines in people with obesity because obesity is a major risk factor for morbidity and mortality in COVID-19.
"The constant state of low-grade inflammation, present in overweight people, can weaken some immune responses, including those launched by T-cells, which can directly kill infected cells," the authors noted.
Findings Reported in British Newspapers
The findings of the Italian study were widely covered in the lay press in the United Kingdom, with headlines such as, "Pfizer vaccine may be less effective in people with obesity, says study"[5] and "Pfizer vaccine: overweight people might need bigger dose, Italian study says." In tabloid newspapers, some headlines were slightly more stigmatizing.
The reports did stress that the Italian research was published as a preprint and has not been peer reviewed, or "is yet to be scrutinized by fellow scientists."
Most made the point that there were only 26 people with obesity among the 248 persons in the study.
"We always knew that BMI was an enormous predictor of poor immune response to vaccines, so this paper is definitely interesting, although it is based on a rather small preliminary dataset," Danny Altmann, a professor of immunology at Imperial College London, told The Guardian newspaper.
"It confirms that having a vaccinated population isn't synonymous with having an immune population, especially in a country with high obesity, and emphasizes the vital need for long-term immune monitoring programs," he added.
Antibody Responses Differ by BMI, Age, and Sex
Researchers in the Italian study assigned the participants -- 158 women and 90 men -- to receive a priming BNT162b2 vaccine dose with a booster at day 21. They collected blood and nasopharyngeal swabs at baseline and 7 days after the second vaccine dose.
After the second dose, 99.5% of participants developed a humoral immune response; one person did not respond. None tested positive for SARS-CoV-2.
Titers of SARS-CoV-2 binding antibodies were greater in younger than in older participants. There were statistically significant differences between persons aged ≤ 37 years (453.5 AU/mL) in comparison with persons aged 47 to 56 years (239.8 AU/mL; P = .005), persons aged ≤ 37 years vs persons aged > 56 years (453.5 vs 182.4 AU/mL; P < .0001), and persons aged 37 to 47 years vs persons aged > 56 years (330.9 vs 182.4 AU/mL; P = .01).
Antibody response was significantly greater for women than for men (338.5 vs 212.6 AU/mL; P = .001).
Humoral responses were greater in persons of normal-weight BMI (18.5 to 24.9 kg/m2; 325.8 AU/mL) and persons of underweight BMI (<18.5 kg/m2; 455.4 AU/mL) compared with persons with pre-obesity, defined as BMI of 25 to 29.9 kg/m2 (222.4 AU/mL), and persons with obesity (BMI ≥ 30 kg/m2; 167 AU/mL; P < .0001). This association remained after adjustment for age (P = .003).
"Our data stresses the importance of close vaccination monitoring of obese people, considering the growing list of countries with obesity problems," the researchers noted.
Hypertension was also associated with lower antibody titers (P = .006), but that lost statistical significance after matching for age (P = .22).
"We strongly believe that our results are extremely encouraging and useful for the scientific community," Pellini and colleagues concluded.
The authors have disclosed no relevant financial relationships. Iwasaki is a cofounder of RIGImmune and is a member of its scientific advisory board.
Study Highlights
The study population comprised healthcare workers at one hospital in Italy who were presenting for the Pfizer-BioNTech COVID-19 vaccine. All participants were between ages 18 and 75 years, and individuals with evidence of current or previous SARS-CoV-2 infection or a history of possible immunosuppression were excluded.
Participants received 30 µg/0.3 mL dose of the vaccine at the outset of the study and then another dose 21 days later.
Investigators collected blood and a nasopharyngeal samples before the first vaccine dose and 7 days after the booster dose. Researchers collected sera from adults with known COVID-19 to compare immunoglobulin G (IgG) antibody levels against S1/S2 antigens of SARS-CoV-2 with those of vaccinated participants.
248 healthcare workers participated in the study. 63.7% of cohort were women, and the median age was 47 years.
None of the participants had a positive polymerase chain reaction test for SARS-CoV-2 before or after vaccination.
The antibody geometric mean concentrations after vaccination and among the cohort who provided convalescent sera after COVID-19 infection were 285.9 AU/mL and 39.4 AU/mL, respectively (P < .0001).
99.5% of vaccine recipients were considered to have responded after the vaccine. Only one participant did not.
There was a fairly linear decline in immune response from participants aged < 37 years to groups aged 37 to 47 years, 47 to 56 years, and more than 56 years.
The antibody geometric mean concentrations after vaccination among women and men were 338.5 AU/mL and 212.6 AU/mL, respectively (P = .001).
The other major variable associated with a reduced immune response to the vaccine was overweight or obesity vs underweight or normal weight.
The presence of hypertension failed to affect vaccine response in adjusted analysis.
Clinical Implications
The COVID-19 mRNA vaccines appear to have efficacy around 80% against COVID-19 after a single dose, but it is unclear how long this protection might last.
In the current study by Pellini and colleagues, older age, male sex, and overweight/obesity were associated with a reduced IgG response after application of an mRNA vaccine against COVID-19.
Implications for the healthcare team: The healthcare team should continue to emphasize routine protective measures such as physical distancing and mask wearing after administration of the COVID-19 vaccine. This advice might particularly be important among men, older adults, and persons with overweight/obesity.
Disclaimer
The educational activity presented above may involve simulated, case-based scenarios. The patients depicted in these scenarios are fictitious and no association with any actual patient, whether living or deceased, is intended or should be inferred. The material presented here does not necessarily reflect the views of Medscape, LLC, or any individuals or commercial entities that support companies that support educational programming on medscape.org. These materials may include discussion of therapeutic products that have not been approved by the US Food and Drug Administration, off-label uses of approved products, or data that were presented in abstract form. These data should be considered preliminary until published in a peer-reviewed journal. Readers should verify all information and data before treating patients or employing any therapies described in this or any educational activity. A qualified healthcare professional should be consulted before using any therapeutic product discussed herein.
Medscape Education © 2021 Medscape, LLC
Covid-19 : bon sang ne saurait mentir ?
Un première étude chinoise a suggéré que le groupe sanguin A était associé à une sensibilité accrue et le groupe sanguin O à une sensibilité réduite à l'infection par le SARS-CoV-2. Des études ultérieures menées en Italie et en Espagne l’ont confirmé. En revanche, des observations réalisées à Boston et à New York n'ont pas retrouvé d'association spécifique entre le groupe sanguin ABO et la maladie. La controverse soulevée par ces études aux résultats discordants a conduit à cette nouvelle étude cas-témoins dont l’objet était de vérifier de manière indépendante si le groupe sanguin est associé à la sensibilité au SARS-CoV-2 et à la gravité de la Covid-19.
Intermountain Healthcare, un système de soins de santé intégré à but non lucratif comprenant 24 hôpitaux et 215 cliniques dans l'Utah, l'Idaho et le Nevada, a constitué une base de données de dossiers médicaux électroniques spécifiques de la Covid-19. A partir de celle-ci ont été étudiées les données les personnes testées pour le SARS-CoV-2 entre le 3 mars et le 2 novembre 2020, et dont le groupe sanguin était mentionné : résultats positifs et négatifs des tests, patients hospitalisés et non hospitalisés, et patients admis en USI et les autres. L'infectivité a été déterminée par la RT-PCR sur des écouvillons nasaux ou des échantillons de salive.
Au total, 107 796 personnes (âge moyen [écart type ET], 42,0 [17,8] ans ; 82 875 [76,9 %] femmes) ont été incluses dans l'étude. Parmi les patients atteints de Covid-19, l'hospitalisation était associée au sexe masculin (1 165 hommes [50,1 %] hospitalisés versus 1 871 hommes [20,5 %] non hospitalisés) et à l'âge (âge moyen [ET] chez les patients hospitalisés, 57,0 [18,1] ans contre 41,4 [14,9] ans versus les personnes non hospitalisées).
L'admission en USI était également associée au sexe masculin (426 hommes [61,8 %] admis en USI versus 725 hommes [44,8 %] non admis) et à l'âge (âge moyen [écart type] chez les patients admis dans une USI ; 60,7 [158] ans versus 55,4 [18,8] ans chez les patients non admis. Les ethnies non blanches (Afro-Américains, Amérindiens ou autochtones d'Alaska, Amérindiens d'Hawaï ou des îles du Pacifique, Asiatiques) étaient associées à la détection du virus (1 592 personnes [13,9 %] avec des résultats positifs versus 6 610 personnes [6,9 %] avec des résultats négatifs) et à l'hospitalisation (556 patients [23,9 %] hospitalisés versus 1 036 personnes [11,3 %] non hospitalisées).
Le groupe sanguin n'est pas associé à la susceptibilité ou à la gravité de la maladie, à la présence du virus, à l'hospitalisation ou à l'admission en USI
Par rapport au groupe sanguin O, le groupe A n'était pas associé à une augmentation de la positivité des tests de détection du virus (Odds ratio OR, 0,97 [intervalle de confiance à 95 % IC à 95 %, 0,93-1,01] ; p = 0,11), de l'hospitalisation (OR, 0,89 [IC à 95 %, 0,80-0,99] ; p = 0,03) ou de l'admission en USI (OR, 0,84 [IC à 95 %, 0,69-1,02] ; p = 0,08). De même, les groupes B et AB n'étaient pas associés à des pronostics plus péjoratifs que le type O. Par contre, les analyses limitées à la race blanche ont donné des résultats similaires à ceux des études précédentes.
Comment expliquer ces résultats en opposition avec les études antérieures ?
Selon les auteurs, la taille réduite des échantillons et la nature rétrospective et observationnelle de nombreuses études antérieures, ainsi que l'hétérogénéité frappante des associations ABO avec la susceptibilité et la gravité des maladies, pourraient être dues à des variations fortuites, à un biais de publication, à des différences de bagage génétique, de géographie et d'environnement, et à des souches virales.
Le gène ABO est hautement polymorphe, et les groupes sanguins ABO sont distribués différemment selon l'ascendance et la géographie. Les différences de susceptibilité aux maladies pourraient être dues à des anticorps naturels ou à des effets pro-thrombotiques avec les individus n'appartenant pas au groupe O.
Cependant, les résultats de cette étude sont similaires à ceux des études précédentes en ce qui concerne les Blancs.
Compte tenu de la nature vaste et prospective de cette étude et de ses résultats les auteurs pensent que des liens entre Covid-19 et groupes ABO sont peu probables et ne seront pas des facteurs utiles pour statuer sur la prédisposition à la maladie ou sa gravité possible, que ce soit au niveau individuel ou au niveau de la population pour des environnements et des ascendances similaires. Des études supplémentaires, étroitement contrôlées pour la génétique, la géographie et la souche virale, sont nécessaires avant d'admettre que le groupe sanguin est un déterminant de la prédisposition à la Covid-19 ou de sa gravité. Fin de partie ?
Dr Bernard-Alex Gaüzère
Référence
Anderson JL et coll. : Association of Sociodemographic Factors and Blood Group Type With Risk of COVID-19 in a US Population. JAMA Netw Open. 2021;4(4):e217429. doi:10.1001/jamanetworkopen.2021.7429
____
Publié le 12/04/2021
Thromboses après vaccin AstraZeneca, la clé de l’énigme ?
La lutte contre la pandémie de Covid-19 liée au virus SARS-CoV-2 repose actuellement de façon prépondérante sur la vaccination à grande échelle. De décembre 2020 à mars 2021, quatre vaccins ont été autorisés par l'agence européenne sur la base des résultats issus d'essais prospectifs contrôlés réalisés en double aveugle: deux vaccins dits à ARN : -le BNT162b2 (Pfizer–BioNTech) et le mRNA-1273 (Moderna) - où l'ARN codant pour la protéine spike du virus SARS-CoV-2, encapsulé dans des nanoparticules lipidiques, est injecté, et deux vaccins où le génome codant pour la protéine spike du virus SARS-CoV-2 est inséré au génome d' un vecteur viral : un adénovirus recombinant du chimpanzé dans le cas du vaccin ChAdOx1 nCov-19 (AstraZeneca ) et un adénovirus recombinant de type 26 dans le cas du vaccin Ad26.COV2.S (Johnson & Johnson/Janssen).
Au 7 avril 2021, plus de 82 millions de personnes ont été vaccinées en Europe (1 ou 2 doses de vaccin) ; ainsi, en Allemagne, plus de 10 millions de personnes ont eu au moins une dose. Un quart de ces personnes environ a reçu le vaccin ChAdOx1 nCov-19 (AstraZeneca). En février plusieurs cas de thrombose après ce vaccin ont été rapportés.
Une première série de onze patients en Allemagne
En Allemagne, le premier cas observé mi-février 2021 a concerné une soignante de 49 ans sans antécédents particuliers ayant succombé à un « syndrome thrombotique » survenu dès 5 jours après l'administration du vaccin ChAdOx1 nCov-19 et qui s’est aggravé malgré le traitement anticoagulant, tableau constitué de thromboses extensives des vaisseaux splanchniques et même de microthromboses de l'aorte et des artères iliaques et d'une thrombose veineuse cérébrale (confirmées par les examens complémentaires et les données autopsiques). Plusieurs autres cas ont été observés et mi-mars 2021 dix autres cas étaient répertoriés. Le dernier cas inclus s'est révélé par un tableau d'hémorragie cérébrale à l’origine de laquelle une thrombose veineuse a été retenue, hypothèse dont la confirmation était en attente au moment de la publication de l'article.
Les caractéristiques sémiologiques des événements thrombotiques constatés dans cette première série de 11 patients (en incluant le cas princeps) sont donc les suivantes : le début survient de 5 j à 16 j après l'administration du vaccin ChAdOx1 nCov-19 ; il s'agit de thromboses veineuses cérébrales dans 9 cas, des veines splanchniques dans 3 cas, d'embolies pulmonaires dans 3 cas et de thromboses affectant d'autres territoires dans 4 cas. Sur 10 patients, 5 présentaient plus d'une thrombose. Une évolution fatale a été constatée dans 6 cas sur 10 répertoriés. Ainsi devant la gravité de ces événements thrombotiques de sémiologie atypique, la recherche du mécanisme physiopathologique s'imposait rapidement. Les résultats font l'objet de cet article.
Le tableau clinique évoque celui des thrombopénies induites par l’héparine
Dans cette série de patients, l’âge médian est de 36 ans (22-49 ans) et on note une prédominance féminine : 9 femmes pour 2 hommes. Il existait constamment une thrombopénie avec un nadir médian à 20 000 /μL environ (9000-103 000 /μL). Aucun patient n'avait reçu d'héparine préalablement. Le tableau clinique évoquait celui des thrombopénies induites par l'héparine où le développement d'anticorps anti PF4 -héparine induit l'activation des plaquettes et la survenue de thromboses. Le PF4 ou Facteur 4 plaquettaire est une glycoprotéine contenue dans les granules alpha des plaquettes, libérée à la surface de celles-ci lors de leur activation, présentant une grande affinité pour les glycosaminoglycans des membranes cellulaires et en particulier pour l'héparine. Dès lors les auteurs de l'article (experts internationaux pour certains dans ce domaine) ont recherché chez ces patients ces anticorps anti-PF4-héparine et anti PF4 par ELISA. Ils ont aussi développé un test d'activation plaquettaire in vitro PFA-dépendante où est mesuré le délai d'apparition de l'agrégation plaquettaire induite par le PF4, délai inversement proportionnel à l'intensité de l'activation plaquettaire.
Les résultats montrent une thrombopénie constante souvent sévère inférieure à 30 000/μL dans 7 cas /10 et associée à une coagulation
intravasculaire disséminée (CIVD) dans 5 cas diagnostiquée devant une forte augmentation des D-dimères, une altération des tests d'hémostase et une hypofibrinogénémie à des degrés divers. Hormis chez 1 patient ayant une anomalie V Leiden et des anticorps anticardiopides, il n'était pas mentionné d'anomalies prothrombotiques pré-existantes chez ces patients. Les tests ELISA anti-PF4 -héparine effectués chez 9 patients (dont le patient 11) étaient tous fortement positifs associés à un test d'activation plaquettaire positif d’intensité variable. Aucun des sujets contrôles n'avait de test d'activation plaquettaire positif. Les tests d'activation plaquettaire étaient négativés in vitro par de fortes doses d'héparine mais aussi de façon intéressante par l’ajout de l'anticorps monoclonal IV-3 ou par les immunoglobulines indiquant que l'activation plaquettaire observée était médiée par le récepteur Fcγ des immunoglobulines.
Tous les patients ont des anticorps anti-Facteur 4 plaquettaire
Ultérieurement, les auteurs ont étudié les sérums de patients qui leur étaient adressés parce qu'ayant présenté des thromboses post vaccin : au total 28 sérums ont été testés (comprenant ceux de l'étude initiale) : ils présentaient tous un test ELISA anti-PF4-héparine et un test ELISA anti-PF4 positifs et induisaient tous un test d'activation plaquettaire PF4 dépendante également positif. Dans deux cas, il a été possible de purifier par immunoaffinité l'anticorps anti-PF4 et de montrer qu'il induisait une forte activation plaquettaire induite spécifiquement par le PF4.
Ainsi le tableau thrombotique présenté par ces patients après vaccin évoque cliniquement un tableau de thrombopénie induite par l'héparine qui est due au développement d'anticorps dirigés contre les complexes multimoléculaires formés entre le PF4 cationique et l'héparine anionique. De fait il est retrouvé de façon constante chez les patients de cette étude des anticorps anti PF4-Héparine et anti PF4 par test ELISA. Néanmoins aucun patient n'avait reçu préalablement d'héparine ou un autre médicament polyanionique connu pour induire également ce type de thrombopénie. Il faut donc rapprocher le tableau de thrombopénie thrombotique présenté après vaccin par ces patients, caractérisé par la présence d'anticorps anti-PF4 et anti PF4-héparine (en dehors de toute administration d'héparine), de celui décrit au décours de certaines infections virales ou bactériennes voire après chirurgie prothétique du genou (1). Par rapport au tableau observé au cours des thrombopénies induites par l'héparine classiques, le tableau observé sans exposition préalable à l'héparine est souvent marqué par une thrombopénie particulièrement profonde, accompagnée de CIVD et compliquée de thromboses dans des territoires atypiques comme cela a été noté chez les patients de cette étude. A l'heure actuelle il est difficile de savoir si ces anticorps anti-PF4 sont des auto-anticorps développés dans le contexte de la forte réaction inflammatoire déclenchée par le vaccin ou des anticorps dirigés contre certains constituants du vaccin et présentant une réaction croisée avec le PF4. Il semble peu probable que l'adénovirus (virus par ailleurs connu pour être capable d'activer les plaquettes) présent à de très faibles concentrations dans le vaccin, ait été responsable d'une activation plaquettaire capable de déclencher un tel tableau thrombotique. Par contre le rôle de fragments d'ADN libre dans le vaccin n'est pas à exclure et ce d'autant plus que les auteurs ont montré antérieurement que des fragments d'ADN ou d'ARN étaient capables d'induire de tels anticorps anti PF4 -héparine dans un système murin (2).
Des immunoglobulines IV à fortes doses pour assurer la « clearance » des anticorps
Au plan clinique la connaissance de ce tableau et de son mécanisme sont de la première importance : ainsi devant la survenue d'une thrombopénie thrombotique chez un patient ayant reçu un vaccin 5 à 15 jours auparavant, la recherche d'anticorps anti PF4 s'impose, réalisable par ELISA ou immunodiffusion à grande échelle dans la plupart des laboratoires hospitaliers. La confirmation par un test fonctionnel d'activation plaquettaire PF4 dépendante avec inhibition in vitro par héparine est souhaitable. Néanmoins avant même les résultats de ces tests, l'administration d'immunoglobulines à fortes doses en intra-veineux peut être proposée dans ce contexte clinique ayant pour but d'accélérer la ''clearance'' des anticorps anti PF4 et la remontée du chiffre plaquettaire comme cela a pu être effectué au cours de thrombopénies induites par l'héparine classiques particulièrement sévères (3). Cette remontée du chiffre plaquettaire devrait faciliter la mise en route du traitement anticoagulant en proscrivant bien évidemment de façon formelle l'utilisation de l'héparine (sous toutes ses formes).
Le terme de ‘'vaccine-induced immune thrombotic thrombocytopenia (VITT)" soit "thrombopénie thrombotique immune induite par vaccin" est proposé par les auteurs.
Dr Sylvia Bellucci
Références
Greinacher A, et coll: Thrombotic Thrombocytopenia after ChAdOx1 nCov-19 Vaccination. N Engl J Med 2021; édition avancée du 9 avril 2021
1) Warkentin TE et al. : A spontaneous prothrombotic disorder resembling heparin-induced thrombocytopenia. Am J Med., 2008; 121: 632-6 36.
2) Jaax ME et al. : Complex formation with nucleic acids and aptamers alters the antigenic properties of platelet factor 4. Blood 2013; 122: 272-281.
3) Warkentin TE : High-dose intravenous immunoglobulin for the treatment and prevention of heparin-induced thrombocytopenia : a review. Expert Rev Hematol., 2019; 12: 685- 698.
jim.fr
____
CME / ABIM MOC / CE
What Are the Factors That Improve COVID Vaccine Antibody Response?
Authors: News Author: Miriam E. Tucker; CME Author: Charles P. Vega, MDFaculty and Disclosures
CME / ABIM MOC / CE Released: 4/2/2021
Valid for credit through: 4/2/2022
Note: The information on the coronavirus outbreak is continually evolving. The content within this activity serves as a historical reference to the information that was available at the time of this publication. We continue to add to the collection of activities on this subject as new information becomes available. It is the policy of Medscape Education to avoid the mention of brand names or specific manufacturers in accredited educational activities. However, manufacturer names related to COVID-19 vaccines may be provided in this activity to promote clarity. The use of manufacturer names should not be viewed as an endorsement by Medscape of any specific product or manufacturer.
Clinical Context
One of the most important and controversial issues in the fight against the COVID-19 pandemic is the temporary application of just 1 dose of the currently available messenger RNA (mRNA)-based vaccines in the United States instead of the currently authorized 2-dose regimen. Proponents of a single-dose strategy argue that these vaccines still are effective against COVID-19 when applied as a single dose, and the current crisis in the United States coupled with problems with vaccine distribution and application mandates a single-dose approach to get as many people vaccinated as soon as possible.
These supporters of a single dose have some good points. First, it is very likely that single dosing will result in more people being vaccinated. In addition, the emergency use authorizations for both the Pfizer-BioNTech[1] and Moderna[2] vaccines cited good vaccine efficacy in a single dose (82% and 80.2%, respectively); however, there are real risks associated with significant delay of a booster dose of these vaccines. Would the protected period against COVID-19 be shortened without a booster? In addition, could the booster provide the additional support necessary as new variants off SARS-CoV-2 emerge? Finally, it is possible that a less effective vaccine might help select for variants that are more vaccine-resistant and possibly more virulent overall.
This debate will continue, fueled by the epidemiology of COVID-19 and the logistical challenge of vaccinating hundreds of millions of people, but what about clinical variables that might affect vaccine efficacy? The current study addresses this issue.
Study Synopsis and Perspective
The capacity to mount humoral immune responses to COVID-19 vaccinations may be reduced among people who are heavier, older, and male, new findings suggest.
The data pertain specifically to the mRNA vaccine, BNT162b2, developed by Pfizer Inc. and BioNTech SE. The study was conducted by Italian researchers and was published February 26 as a preprint.[3]
The study involved 248 healthcare workers who each received 2 doses of the vaccine. Of the participants, 99.5% developed a humoral immune response after the second dose. Those responses varied by body mass index (BMI), age, and sex.
"The findings imply that female, lean and young people have an increased capacity to mount humoral immune responses compared to male, overweight and older populations," said Raul Pellini, professor at the IRCCS Regina Elena National Cancer Institute, Rome, Italy, and colleagues.
"To our knowledge, this study is the first to analyze Covid-19 vaccine response in correlation to BMI," they noted.
"Although further studies are needed, this data may have important implications to the development of vaccination strategies for COVID-19, particularly in obese people," they wrote.
If the data are confirmed by larger studies, "giving obese people an extra dose of the vaccine or a higher dose could be options to be evaluated in this population."
Results Contrast With Pfizer Trials of Vaccine
The BMI finding seemingly contrasts with final data from the phase 3 clinical trial of the vaccine, which were reported in a supplement index to an article published December 31, 2020, in the New England Journal of Medicine.[4] In that study, vaccine efficacy did not differ by obesity status.
Asked to comment, Akiko Iwasaki, PhD, professor of immunology at the Howard Hughes Medical Institute and an investigator at Yale University School of Medicine, New Haven, Connecticut, noted that although the current Italian study showed somewhat lower levels of antibodies in people with obesity compared with people who did not have obesity, the phase 3 trial found no difference in symptomatic infection rates.
"These results indicate that even with a slightly lower level of antibody induced in obese people, that level was sufficient to protect against symptomatic infection," Iwasaki told Medscape Medical News.
Indeed, Pellini and colleagues pointed out that responses to vaccines against influenza, hepatitis B, and rabies are also reduced in persons with obesity compared to lean individuals.
They said, however, that it was especially important to study the effectiveness of COVID-19 vaccines in people with obesity because obesity is a major risk factor for morbidity and mortality in COVID-19.
"The constant state of low-grade inflammation, present in overweight people, can weaken some immune responses, including those launched by T-cells, which can directly kill infected cells," the authors noted.
Findings Reported in British Newspapers
The findings of the Italian study were widely covered in the lay press in the United Kingdom, with headlines such as, "Pfizer vaccine may be less effective in people with obesity, says study"[5] and "Pfizer vaccine: overweight people might need bigger dose, Italian study says." In tabloid newspapers, some headlines were slightly more stigmatizing.
The reports did stress that the Italian research was published as a preprint and has not been peer reviewed, or "is yet to be scrutinized by fellow scientists."
Most made the point that there were only 26 people with obesity among the 248 persons in the study.
"We always knew that BMI was an enormous predictor of poor immune response to vaccines, so this paper is definitely interesting, although it is based on a rather small preliminary dataset," Danny Altmann, a professor of immunology at Imperial College London, told The Guardian newspaper.
"It confirms that having a vaccinated population isn't synonymous with having an immune population, especially in a country with high obesity, and emphasizes the vital need for long-term immune monitoring programs," he added.
Antibody Responses Differ by BMI, Age, and Sex
Researchers in the Italian study assigned the participants -- 158 women and 90 men -- to receive a priming BNT162b2 vaccine dose with a booster at day 21. They collected blood and nasopharyngeal swabs at baseline and 7 days after the second vaccine dose.
After the second dose, 99.5% of participants developed a humoral immune response; one person did not respond. None tested positive for SARS-CoV-2.
Titers of SARS-CoV-2 binding antibodies were greater in younger than in older participants. There were statistically significant differences between persons aged ≤ 37 years (453.5 AU/mL) in comparison with persons aged 47 to 56 years (239.8 AU/mL; P = .005), persons aged ≤ 37 years vs persons aged > 56 years (453.5 vs 182.4 AU/mL; P < .0001), and persons aged 37 to 47 years vs persons aged > 56 years (330.9 vs 182.4 AU/mL; P = .01).
Antibody response was significantly greater for women than for men (338.5 vs 212.6 AU/mL; P = .001).
Humoral responses were greater in persons of normal-weight BMI (18.5 to 24.9 kg/m2; 325.8 AU/mL) and persons of underweight BMI (<18.5 kg/m2; 455.4 AU/mL) compared with persons with pre-obesity, defined as BMI of 25 to 29.9 kg/m2 (222.4 AU/mL), and persons with obesity (BMI ≥ 30 kg/m2; 167 AU/mL; P < .0001). This association remained after adjustment for age (P = .003).
"Our data stresses the importance of close vaccination monitoring of obese people, considering the growing list of countries with obesity problems," the researchers noted.
Hypertension was also associated with lower antibody titers (P = .006), but that lost statistical significance after matching for age (P = .22).
"We strongly believe that our results are extremely encouraging and useful for the scientific community," Pellini and colleagues concluded.
The authors have disclosed no relevant financial relationships. Iwasaki is a cofounder of RIGImmune and is a member of its scientific advisory board.
Study Highlights
The study population comprised healthcare workers at one hospital in Italy who were presenting for the Pfizer-BioNTech COVID-19 vaccine. All participants were between ages 18 and 75 years, and individuals with evidence of current or previous SARS-CoV-2 infection or a history of possible immunosuppression were excluded.
Participants received 30 µg/0.3 mL dose of the vaccine at the outset of the study and then another dose 21 days later.
Investigators collected blood and a nasopharyngeal samples before the first vaccine dose and 7 days after the booster dose. Researchers collected sera from adults with known COVID-19 to compare immunoglobulin G (IgG) antibody levels against S1/S2 antigens of SARS-CoV-2 with those of vaccinated participants.
248 healthcare workers participated in the study. 63.7% of cohort were women, and the median age was 47 years.
None of the participants had a positive polymerase chain reaction test for SARS-CoV-2 before or after vaccination.
The antibody geometric mean concentrations after vaccination and among the cohort who provided convalescent sera after COVID-19 infection were 285.9 AU/mL and 39.4 AU/mL, respectively (P < .0001).
99.5% of vaccine recipients were considered to have responded after the vaccine. Only one participant did not.
There was a fairly linear decline in immune response from participants aged < 37 years to groups aged 37 to 47 years, 47 to 56 years, and more than 56 years.
The antibody geometric mean concentrations after vaccination among women and men were 338.5 AU/mL and 212.6 AU/mL, respectively (P = .001).
The other major variable associated with a reduced immune response to the vaccine was overweight or obesity vs underweight or normal weight.
The presence of hypertension failed to affect vaccine response in adjusted analysis.
Clinical Implications
The COVID-19 mRNA vaccines appear to have efficacy around 80% against COVID-19 after a single dose, but it is unclear how long this protection might last.
In the current study by Pellini and colleagues, older age, male sex, and overweight/obesity were associated with a reduced IgG response after application of an mRNA vaccine against COVID-19.
Implications for the healthcare team: The healthcare team should continue to emphasize routine protective measures such as physical distancing and mask wearing after administration of the COVID-19 vaccine. This advice might particularly be important among men, older adults, and persons with overweight/obesity.
Disclaimer
The educational activity presented above may involve simulated, case-based scenarios. The patients depicted in these scenarios are fictitious and no association with any actual patient, whether living or deceased, is intended or should be inferred. The material presented here does not necessarily reflect the views of Medscape, LLC, or any individuals or commercial entities that support companies that support educational programming on medscape.org. These materials may include discussion of therapeutic products that have not been approved by the US Food and Drug Administration, off-label uses of approved products, or data that were presented in abstract form. These data should be considered preliminary until published in a peer-reviewed journal. Readers should verify all information and data before treating patients or employing any therapies described in this or any educational activity. A qualified healthcare professional should be consulted before using any therapeutic product discussed herein.
Medscape Education © 2021 Medscape, LLC
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Publié le 13/04/2021
Paramédicaux de la fonction publique hospitalière : une nouvelle revalorisation en octobre
Paris, le 13 avril 2021 – A l’ occasion d’une réunion du comité de suivi du Ségur de la santé, Olivier Véran a annoncé, hier, une nouvelle revalorisation pour les personnels paramédicaux de la fonction publique hospitalière, qui entrera en vigueur en octobre.
Une progression qui doit permettre de « donner des perspectives aux soignants déjà dans le système de santé » et d’« améliorer l’attractivité de ces métiers ». Une enveloppe de 740 millions d’euros est prévue en année pleine pour déployer la mesure.
Cette révision des grilles s’ajoute à l’augmentation de 183 euros nets par mois attribuée aux personnels paramédicaux et non médicaux des établissements de santé et des Ehpad (1,5 million de personnes), mise en œuvre en deux temps en septembre puis en décembre, grâce à une enveloppe de 7,6 milliards d’euros.
3 398 euros brut par mois pour un infirmier
Avec cette nouvelle augmentation, selon les calculs du ministère, pour les 153 000 infirmiers en soins généraux, cette revalorisation représentera 107 euros nets de plus par mois après un an de carrière, 152 euros après cinq ans ou encore 278 euros après vingt ans.
Le traitement de fin de carrière passera de 2 863 euros à 3 398 euros par mois, en combinant la première augmentation de 183 euros ainsi que la revalorisation.
Pour 200 000 aides-soignants, il s’agira d’une progression de 45 euros nets après un an en exercice, 78 euros après cinq ans, et 468 euros en fin de carrière, pour atteindre une rémunération de 2 954 euros brut mensuel.
Prochaine étape : des hausses vont également être discutées pour les personnels paramédicaux des fonctions publiques d’État et territoriale (15 000 à 20 000 « équivalents temps plein »), ainsi que du secteur privé lucratif et non lucratif, soit 250 000 « équivalents temps plein ».
Prudence syndicale
S’ils saluent des «avancées», les syndicats demeurent prudents. « Véran a fait sa com’, mais il s’est gardé de rentrer dans les détails. Il dit qu’une infirmière en fin de carrière pourra toucher 3 000 euros net, soit 543 euros de plus qu’aujourd’hui. C’est vrai pour une infirmière qui vient d’être recrutée, pas forcément pour une infirmière en poste depuis déjà plusieurs années. Pour ces dernières, tout va dépendre de son indice de reclassement dans la nouvelle grille. II va falloir regarder de près comment la Direction générale de l’offre de soin (DGOS) va interpréter la copie du gouvernement » souligne Didier Birig (Force Ouvrière).
De son côté, Evelyne Rescanières (CFDT) pointe « 89 % des aides soignants sont des aides soignantes, c’est une profession très féminisée, et très impactées par les ruptures d’activité, les temps partiels, les congés maternité ou parentaux. En moyenne, il y a sept ans d’écart de carrière entre une femme et un homme. Il va falloir regarder combien d’entre elles peuvent réellement espérer bénéficier de l’indice maximal…».
A suivre dans le détail…
Gabriel Poteau
Paramédicaux de la fonction publique hospitalière : une nouvelle revalorisation en octobre
Paris, le 13 avril 2021 – A l’ occasion d’une réunion du comité de suivi du Ségur de la santé, Olivier Véran a annoncé, hier, une nouvelle revalorisation pour les personnels paramédicaux de la fonction publique hospitalière, qui entrera en vigueur en octobre.
Une progression qui doit permettre de « donner des perspectives aux soignants déjà dans le système de santé » et d’« améliorer l’attractivité de ces métiers ». Une enveloppe de 740 millions d’euros est prévue en année pleine pour déployer la mesure.
Cette révision des grilles s’ajoute à l’augmentation de 183 euros nets par mois attribuée aux personnels paramédicaux et non médicaux des établissements de santé et des Ehpad (1,5 million de personnes), mise en œuvre en deux temps en septembre puis en décembre, grâce à une enveloppe de 7,6 milliards d’euros.
3 398 euros brut par mois pour un infirmier
Avec cette nouvelle augmentation, selon les calculs du ministère, pour les 153 000 infirmiers en soins généraux, cette revalorisation représentera 107 euros nets de plus par mois après un an de carrière, 152 euros après cinq ans ou encore 278 euros après vingt ans.
Le traitement de fin de carrière passera de 2 863 euros à 3 398 euros par mois, en combinant la première augmentation de 183 euros ainsi que la revalorisation.
Pour 200 000 aides-soignants, il s’agira d’une progression de 45 euros nets après un an en exercice, 78 euros après cinq ans, et 468 euros en fin de carrière, pour atteindre une rémunération de 2 954 euros brut mensuel.
Prochaine étape : des hausses vont également être discutées pour les personnels paramédicaux des fonctions publiques d’État et territoriale (15 000 à 20 000 « équivalents temps plein »), ainsi que du secteur privé lucratif et non lucratif, soit 250 000 « équivalents temps plein ».
Prudence syndicale
S’ils saluent des «avancées», les syndicats demeurent prudents. « Véran a fait sa com’, mais il s’est gardé de rentrer dans les détails. Il dit qu’une infirmière en fin de carrière pourra toucher 3 000 euros net, soit 543 euros de plus qu’aujourd’hui. C’est vrai pour une infirmière qui vient d’être recrutée, pas forcément pour une infirmière en poste depuis déjà plusieurs années. Pour ces dernières, tout va dépendre de son indice de reclassement dans la nouvelle grille. II va falloir regarder de près comment la Direction générale de l’offre de soin (DGOS) va interpréter la copie du gouvernement » souligne Didier Birig (Force Ouvrière).
De son côté, Evelyne Rescanières (CFDT) pointe « 89 % des aides soignants sont des aides soignantes, c’est une profession très féminisée, et très impactées par les ruptures d’activité, les temps partiels, les congés maternité ou parentaux. En moyenne, il y a sept ans d’écart de carrière entre une femme et un homme. Il va falloir regarder combien d’entre elles peuvent réellement espérer bénéficier de l’indice maximal…».
A suivre dans le détail…
Gabriel Poteau
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Publié le 16/04/2021
SDRA en décubitus ventral, comment prendre position ?
Depuis les premières tentatives en 1976, le rationnel physiopathologique de l’utilisation du décubitus ventral (DV) dans la prise en charge des SDRA (syndromes de détresse respiratoire aiguë) est apparu d’emblée séduisant. Mais il a fallu attendre une trentaine d’années pour que la recherche clinique et fondamentale démontre formellement son bénéfice sur la survie des patients.
Les indications et les modalités du DV
Actuellement, la ventilation en DV est recommandée chez les patients atteints de SDRA (rapport PaO2/FiO2 < 100), mais ne présente aucun intérêt en cas de SDRA légers (PaO2/FiO2 > 200). Lors des SDRA de sévérité intermédiaire (100 < PaO2/FiO2 < 200), la persistance d’un rapport PaO2/FiO2 < 150 avec une PEEP > 5 cmH2O après 12 à 24 heures d’évolution malgré un traitement optimal est un critère d’indication du DV, selon les résultats de l’étude PROSEVA. En outre, le DV doit être débuté au cours des 24 à 48 premières heures du SDRA sévère et pendant de longues séances quotidiennes (> 16 h/j), une relation quasi linéaire existant entre la survie et la durée des séances de ventilation en DV. De plus, la ventilation en DV va de pair avec les principes de ventilation protectrice et du recours à la curarisation à la phase précoce.
Une procédure longue, complexe et risquée
Le retournement des patients du décubitus dorsal en DV et inversement, est une procédure complexe qui requiert au moins quatre personnes et l’application d’un protocole strict afin d’anticiper les besoins matériels, de standardiser la procédure et d’éviter la complication suprême : l’extubation accidentelle. D’où l’idée de proposer un positionnement mécanisé et de l’évaluer par rapport au positionnement manuel classique, dans le cadre d'un projet d'amélioration de la qualité de la mise en DV par une équipe multidisciplinaire américaine.
Une approche rétrospective, descriptive-comparative a été utilisée pour analyser les données de 24 mois d'un protocole de mise en DV. L'étude a porté sur une petite série de 37 patients, dont 16 ont été placés en DV manuellement et 21 de façon automatisée.
Avantage au bon vieux positionnement manuel
Les résultats ont été similaires entre les deux groupes en ce qui concerne le délai de mise en DV et la durée du séjour en service de réanimation. Toutefois, les patients mis en DV manuellement ont eu moins d’interruptions de traitement (p = 0,005) et surtout moins de complications (p = 0,002). Les lésions des zones d’appui ont constitué le type de complication le plus courant. Les localisations les plus fréquentes chez les patients mis en DV de façon mécanisée ont été la tête (p = 0,045), le thorax (p = 0,003) et les extrémités inférieures (p = 0,047), comme si le positionnement mécanique avait été moins personnalisé et moins attentif aux traditionnelles zones de pression.
Détail d’importance : le positionnement manuel en DV a permis d'économiser 78 617 dollars par patient !
Le positionnement manuel en DV a donc démontré des résultats similaires à celui des positionnement en DV mécanisé, mais avec moins de risque d'interruption du traitement, moins de complications et un moindre coût. Des recherches supplémentaires sont nécessaires…
Dr Bernard-Alex Gaüzère
Référence
Morata L, Sole ML, Guido-Sanz F, Ogilvie C, Rich R : Manual vs Automatic Prone Positioning and Patient Outcomes in Acute Respiratory Distress Syndrome. Am J Crit Care, 2021; 30(2):104-112. doi: 10.4037/ajcc2021674. PMID: 33644805.
______
Publié le 23/04/2020
Covid-19 : parfois la RT-PCR est négative mais le scanner ne l’est pas !
Le diagnostic positif du Covid-19 repose sur l’identification du SARS-CoV-2 par RT-PCR au sein de prélèvements habituellement effectués par écouvillonnage au niveau du nasopharynx. Cette méthode sert de « gold standard » en dépit de performances diagnostiques qui sont loin d’être optimales, conditionnées notamment par la qualité du prélèvement et de son transport mais aussi par les caractéristiques des kits, toutes n’étant pas égales. Pour toutes ces raisons, la sensibilité de cette approche est des plus variables avec des valeurs comprises entre 30 % et 60 % selon les séries et le stade de la maladie.
D’aussi piètres performances incitent à renouveler le test quand la probabilité d’un faux-négatif semble élevée ou à se tourner vers d’autres méthodes diagnostiques en fonction du contexte. Le scanner thoracique fait partie de ces options, tout au moins dans les formes relativement sévères et en tout cas cliniquement patentes du Covid-19, notamment quand une hospitalisation est envisagée. Cette imagerie peut en effet révéler des aspects sinon spécifiques du moins évocateurs à type d’opacités en verre dépoli plurifocales ou de foyers de consolidation associés, volontiers bilatéraux et périphériques… alors même que la RT-PCR est bel et bien négative.
Sensibilité élevée du scanner
Une étude transversale et longitudinale réalisée à Wuhan (Chine), entre le 6 janvier et le 6 février 2020 a comparé les deux moyens diagnostiques chez 1 014 patients (âge moyen, 51 ± 15 ans ; sexe masculin : 46 %) soupçonnés d’être atteints de Covid-19. Les images tomodensitométriques ont été interprétées par deux radiologues expérimentés qui n’avaient pas connaissance des résultats du test biologique mais avaient accès aux données épidémiologiques et cliniques. Les signes suivants ont été pris en compte pour poser un diagnostic positif : opacités en verre dépoli, foyers de consolidation, épaississement ou réticulation des septa interlobulaires ainsi que distribution des lésions (uni- ou bilatérales).
La RT-PCR s’est avérée positive chez 601 patients (59 %), alors que le diagnostic a été posé sur le scanner thoracique dans 88 % des cas (888/1014). La sensibilité de ce dernier a été estimée à 97 % (intervalle de confiance à 95 % IC95%, 95-98 %), versus la RT-PCR en tant que référence. Dans le sous-groupe caractérisé par une RT-PCR négative, le scanner thoracique s’est avéré positif dans 75 % des cas (308/413) : près d’une fois sur deux (48 %), le diagnostic de Covid-19 était hautement probable et vraisemblable une fois sur trois (33 %).
Un intérêt pour le suivi des patients
Une analyse complémentaire a porté sur les examens répétés après les explorations initiales. Il apparaît que le délai moyen entre une première RT-PCR négative et un résultat positif est de 5,1 ± 1,5 jours tandis que le délai moyen avant la négativation d’une première RT-PCR positive est de 6,9±2,3 jours. Dans 60 % à 93 % des cas, le scanner thoracique était en faveur du diagnostic de Covid-19, avant -ou en même temps- que la RT-PCR ne devienne positive. Les images pulmonaires se sont améliorées près d’une fois sur deux (42 % ; 24/57) avant que le dosage biologique ne se négative. L’intérêt du scanner dans le suivi doit cependant être précisé compte tenu de la faiblesse de l’effectif étudié (n=57).
Cette étude qui porte sur plus de 1 000 patients souligne la haute sensibilité (88 % à 97 %, selon le mode de calcul) du scanner thoracique dans le diagnostic positif du Covid-19. Dans ces conditions, face à une forme sévère de la maladie, cet examen dont les résultats sont immédiats mérite d’être utilisé en première intention parallèlement à la RT-PCR dont les résultats sont à la fois plus tardifs et… plus aléatoires. Les performances du scanner ont peut-être été quelque peu surestimées compte tenu… du nombre élevé de faux-négatifs de la RT-PCR initiale. La stratégie doit in fine tenir compte de la probabilité plus ou moins élevée du diagnostic a priori et des infrastructures locales, notamment l’accès au scanner.
Il faut aussi souligner qu’au sein de cette cohorte chinoise explorée au plus fort de l’épidémie, la prévalence de la maladie était proche de 100 %, une notion qui doit être présente à l’esprit quand il s’agit d’évaluer les performances diagnostiques d’un examen. En l’occurrence, il s’agissait d’un cluster et les résultats ont tout lieu d’être reproductibles d’un cluster à l’autre, mais plus discutables en dehors de ces derniers. L’imagerie semble, par ailleurs, être intéressante dans le suivi de la maladie.
Dr Philippe Tellier
Référence
Ai T et coll. : Correlation of Chest CT and RT-PCR Testing in Coronavirus Disease 2019 (COVID-19) in China: A Report of 1014 Cases. Radiology. 2020 (26 février) : publication avancée en ligne. doi: 10.1148/radiol.2020200642.
jim.fr
SDRA en décubitus ventral, comment prendre position ?
Depuis les premières tentatives en 1976, le rationnel physiopathologique de l’utilisation du décubitus ventral (DV) dans la prise en charge des SDRA (syndromes de détresse respiratoire aiguë) est apparu d’emblée séduisant. Mais il a fallu attendre une trentaine d’années pour que la recherche clinique et fondamentale démontre formellement son bénéfice sur la survie des patients.
Les indications et les modalités du DV
Actuellement, la ventilation en DV est recommandée chez les patients atteints de SDRA (rapport PaO2/FiO2 < 100), mais ne présente aucun intérêt en cas de SDRA légers (PaO2/FiO2 > 200). Lors des SDRA de sévérité intermédiaire (100 < PaO2/FiO2 < 200), la persistance d’un rapport PaO2/FiO2 < 150 avec une PEEP > 5 cmH2O après 12 à 24 heures d’évolution malgré un traitement optimal est un critère d’indication du DV, selon les résultats de l’étude PROSEVA. En outre, le DV doit être débuté au cours des 24 à 48 premières heures du SDRA sévère et pendant de longues séances quotidiennes (> 16 h/j), une relation quasi linéaire existant entre la survie et la durée des séances de ventilation en DV. De plus, la ventilation en DV va de pair avec les principes de ventilation protectrice et du recours à la curarisation à la phase précoce.
Une procédure longue, complexe et risquée
Le retournement des patients du décubitus dorsal en DV et inversement, est une procédure complexe qui requiert au moins quatre personnes et l’application d’un protocole strict afin d’anticiper les besoins matériels, de standardiser la procédure et d’éviter la complication suprême : l’extubation accidentelle. D’où l’idée de proposer un positionnement mécanisé et de l’évaluer par rapport au positionnement manuel classique, dans le cadre d'un projet d'amélioration de la qualité de la mise en DV par une équipe multidisciplinaire américaine.
Une approche rétrospective, descriptive-comparative a été utilisée pour analyser les données de 24 mois d'un protocole de mise en DV. L'étude a porté sur une petite série de 37 patients, dont 16 ont été placés en DV manuellement et 21 de façon automatisée.
Avantage au bon vieux positionnement manuel
Les résultats ont été similaires entre les deux groupes en ce qui concerne le délai de mise en DV et la durée du séjour en service de réanimation. Toutefois, les patients mis en DV manuellement ont eu moins d’interruptions de traitement (p = 0,005) et surtout moins de complications (p = 0,002). Les lésions des zones d’appui ont constitué le type de complication le plus courant. Les localisations les plus fréquentes chez les patients mis en DV de façon mécanisée ont été la tête (p = 0,045), le thorax (p = 0,003) et les extrémités inférieures (p = 0,047), comme si le positionnement mécanique avait été moins personnalisé et moins attentif aux traditionnelles zones de pression.
Détail d’importance : le positionnement manuel en DV a permis d'économiser 78 617 dollars par patient !
Le positionnement manuel en DV a donc démontré des résultats similaires à celui des positionnement en DV mécanisé, mais avec moins de risque d'interruption du traitement, moins de complications et un moindre coût. Des recherches supplémentaires sont nécessaires…
Dr Bernard-Alex Gaüzère
Référence
Morata L, Sole ML, Guido-Sanz F, Ogilvie C, Rich R : Manual vs Automatic Prone Positioning and Patient Outcomes in Acute Respiratory Distress Syndrome. Am J Crit Care, 2021; 30(2):104-112. doi: 10.4037/ajcc2021674. PMID: 33644805.
______
Publié le 23/04/2020
Covid-19 : parfois la RT-PCR est négative mais le scanner ne l’est pas !
Le diagnostic positif du Covid-19 repose sur l’identification du SARS-CoV-2 par RT-PCR au sein de prélèvements habituellement effectués par écouvillonnage au niveau du nasopharynx. Cette méthode sert de « gold standard » en dépit de performances diagnostiques qui sont loin d’être optimales, conditionnées notamment par la qualité du prélèvement et de son transport mais aussi par les caractéristiques des kits, toutes n’étant pas égales. Pour toutes ces raisons, la sensibilité de cette approche est des plus variables avec des valeurs comprises entre 30 % et 60 % selon les séries et le stade de la maladie.
D’aussi piètres performances incitent à renouveler le test quand la probabilité d’un faux-négatif semble élevée ou à se tourner vers d’autres méthodes diagnostiques en fonction du contexte. Le scanner thoracique fait partie de ces options, tout au moins dans les formes relativement sévères et en tout cas cliniquement patentes du Covid-19, notamment quand une hospitalisation est envisagée. Cette imagerie peut en effet révéler des aspects sinon spécifiques du moins évocateurs à type d’opacités en verre dépoli plurifocales ou de foyers de consolidation associés, volontiers bilatéraux et périphériques… alors même que la RT-PCR est bel et bien négative.
Sensibilité élevée du scanner
Une étude transversale et longitudinale réalisée à Wuhan (Chine), entre le 6 janvier et le 6 février 2020 a comparé les deux moyens diagnostiques chez 1 014 patients (âge moyen, 51 ± 15 ans ; sexe masculin : 46 %) soupçonnés d’être atteints de Covid-19. Les images tomodensitométriques ont été interprétées par deux radiologues expérimentés qui n’avaient pas connaissance des résultats du test biologique mais avaient accès aux données épidémiologiques et cliniques. Les signes suivants ont été pris en compte pour poser un diagnostic positif : opacités en verre dépoli, foyers de consolidation, épaississement ou réticulation des septa interlobulaires ainsi que distribution des lésions (uni- ou bilatérales).
La RT-PCR s’est avérée positive chez 601 patients (59 %), alors que le diagnostic a été posé sur le scanner thoracique dans 88 % des cas (888/1014). La sensibilité de ce dernier a été estimée à 97 % (intervalle de confiance à 95 % IC95%, 95-98 %), versus la RT-PCR en tant que référence. Dans le sous-groupe caractérisé par une RT-PCR négative, le scanner thoracique s’est avéré positif dans 75 % des cas (308/413) : près d’une fois sur deux (48 %), le diagnostic de Covid-19 était hautement probable et vraisemblable une fois sur trois (33 %).
Un intérêt pour le suivi des patients
Une analyse complémentaire a porté sur les examens répétés après les explorations initiales. Il apparaît que le délai moyen entre une première RT-PCR négative et un résultat positif est de 5,1 ± 1,5 jours tandis que le délai moyen avant la négativation d’une première RT-PCR positive est de 6,9±2,3 jours. Dans 60 % à 93 % des cas, le scanner thoracique était en faveur du diagnostic de Covid-19, avant -ou en même temps- que la RT-PCR ne devienne positive. Les images pulmonaires se sont améliorées près d’une fois sur deux (42 % ; 24/57) avant que le dosage biologique ne se négative. L’intérêt du scanner dans le suivi doit cependant être précisé compte tenu de la faiblesse de l’effectif étudié (n=57).
Cette étude qui porte sur plus de 1 000 patients souligne la haute sensibilité (88 % à 97 %, selon le mode de calcul) du scanner thoracique dans le diagnostic positif du Covid-19. Dans ces conditions, face à une forme sévère de la maladie, cet examen dont les résultats sont immédiats mérite d’être utilisé en première intention parallèlement à la RT-PCR dont les résultats sont à la fois plus tardifs et… plus aléatoires. Les performances du scanner ont peut-être été quelque peu surestimées compte tenu… du nombre élevé de faux-négatifs de la RT-PCR initiale. La stratégie doit in fine tenir compte de la probabilité plus ou moins élevée du diagnostic a priori et des infrastructures locales, notamment l’accès au scanner.
Il faut aussi souligner qu’au sein de cette cohorte chinoise explorée au plus fort de l’épidémie, la prévalence de la maladie était proche de 100 %, une notion qui doit être présente à l’esprit quand il s’agit d’évaluer les performances diagnostiques d’un examen. En l’occurrence, il s’agissait d’un cluster et les résultats ont tout lieu d’être reproductibles d’un cluster à l’autre, mais plus discutables en dehors de ces derniers. L’imagerie semble, par ailleurs, être intéressante dans le suivi de la maladie.
Dr Philippe Tellier
Référence
Ai T et coll. : Correlation of Chest CT and RT-PCR Testing in Coronavirus Disease 2019 (COVID-19) in China: A Report of 1014 Cases. Radiology. 2020 (26 février) : publication avancée en ligne. doi: 10.1148/radiol.2020200642.
jim.fr
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Publié le 13/04/2021
Il faut bien une seule dose de vaccin à mARN après une Covid-19
Chez les patients qui ont contracté la Covid-19 dans les mois précédents, des stratégies vaccinales spécifiques semblent pouvoir être envisagées. Pourquoi en effet administrer deux doses espacées de trois semaines alors qu’une dose unique pourrait suffire au vu de la réponse immunitaire naturelle tant humorale que cellulaire induite par l’infection inaugurale ? Certaines petites études récentes qui portent sur des effectifs restreints plaident en faveur de ce choix qui concilie des arguments à la fois immunologiques et économiques.
Un choix qui a déjà été fait par les autorités sanitaires de certains pays, et qui est au demeurant conforté par une étude de cohorte récente dont les résultats viennent d’être publiés en ligne le 1er avril dans Nature Medicine.
La population étudiée se compose de 1 090 professionnels de santé (âge moyen 41,9 ± 12,2 ans ; femmes : 60,7 % ; non-Blancs : 53,3 %) recrutés dans un grand centre hospitalo-universitaire en Californie du sud et tous candidats à la vaccination contre la Covid-19 au moyen d’un vaccin à mARN, en l’occurrence le BNT162b2 (Pfizer–BioNTech). Au sein de cette cohorte, ont été distingués deux sous-groupes : dans l’un (n = 35), les participants avaient été préalablement atteints de la Covid-19, alors que, dans l’autre (n = 228), il n’existait aucun antécédent de ce type. Ces derniers ont reçu deux doses du vaccin, espacées de trois semaines, tandis que les premiers n’ont reçu qu’une dose.
Immunité humorale apparemment optimale avec une dose unique en cas de Covid-19 antérieure
Les concentrations sériques d’anticorps IgG neutralisants, dirigés contre le domaine RBD de la protéine spike virale (IgG [S-RBD]), ont été systématiquement dosées à intervalles réguliers au cours des trois semaines qui ont suivi les injections dans les deux groupes. La comparaison des courbes sériques correspondantes et des taux d’anticorps IgG [S-RBD] n’a révélé aucune différence intergroupe significative.
Si l’on se fixe un seuil quantitatif > 4 160 UA ml−1 pour ces concentrations -lequel correspond à une immunité jugée optimale in vitro à partir du test de séroneutralisation par réduction des plaques- il s’avère qu’il a été atteint moins fréquemment dans le groupe des patients infectés et vaccinés avec un dose unique (p < 0,001 versus l’autre groupe). Ce critère d’efficacité est cependant secondaire par rapport à l’évaluation de la réponse immunitaire humorale précédemment évoqvitrouée qui a par ailleurs été complétée par une étude de la neutralisation du récepteur ACE2 par ces anticorps : aucune différence n’a été corrélée au nombre de doses administrées, certains participants déjà infectés ayant bénéficié finalement de la vaccination en deux temps.
Cette étude de cohorte a le mérite de porter sur un effectif conséquent plutôt hétérogène quant aux stratégies vaccinales adoptées en fonction de l’exposition antérieure éventuelle à la Covid-19. Les résultats tendent à conforter le choix d’ores et déjà effectué par certaines autorités sanitaires : en cas d’antécédent confirmé de de la maladie, une dose unique de vaccin à ARN semble suffisante pour déclencher une réponse immunitaire humorale qui équivaut à celle obtenue avec deux injections chez des sujets qui n’ont jamais été exposés au SARS-CoV-2. Parmi les limites de cette étude, il faut souligner la durée de la période d’observation post-vaccinale qui n’excède pas trois semaines et qui pose la question de la durée de la protection conférée par le vaccin.
Dr Philippe Tellier
Référence
Ebinger JE et coll. : Antibody responses to the BNT162b2 mRNA vaccine in individuals previously infected with SARS-CoV-2. Nat Med., 2021 ; publication avancée en ligne le 1er avril. doi: 10.1038/s41591-021-01325-6.
_____
Publié le 16/04/2021
Echappement vaccinal : sortez vos cahiers de maths !
L’échappement vaccinal en cette période de pandémie interminable prend désormais des proportions inquiétantes dans certains pays comme le Brésil ou l’Afrique du sud. L’apparition de variants du SARS-CoV-2 et la durée limitée de l’immunité qu’elle soit naturelle ou post-vaccinale sont deux facteurs largement impliqués dans ce phénomène. Mais il en est un autre qui pourrait intervenir comme le suggère l’intuition épidémiologique et biologique. La probabilité de l’échappement aux vaccins est en effet également conditionnée par la circulation du virus : plus elle est importante, plus les mutations s’accumulent, le nombre de ces dernières étant positivement corrélé au nombre gigantesque des copies du génome viral lorsque virus passe d’un hôte à l’autre. La sélection darwinienne vient compléter l’ouvrage en favorisant les variants les plus résistants et c’est ce qui se passe en ce moment avec le risque de mettre les politiques vaccinales en échec.
Une équation simple et quelques (mutations) inconnues
Une modélisation mathématique peut permettre de quantifier ce processus. Il suffit de mettre au point une équation probabiliste « simple » qui établit une relation non linéaire entre la probabilité de l’échappement vaccinal et le nombre de cas quotidiens de la Covid-19 (N).
La démonstration ou plutôt l’illustration vaut pour le Royaume-Uni où un modèle a été utilisé pour aboutir à la formule suivante qui ne tombe pas du ciel mais sort d’instituts spécialisés dans les mathématiques appliquées :
Risque d’échappement vaccinal au cours d’une période donnée = 1- (1-p) N
où p représente la probabilité d’une mutation décisive par infection et N le nombre de cas quotidiens observés pendant cette période.
Il apparaît en effet que le risque est positivement corrélé au nombre de cas quotidiens, étant entendu que la probabilité d’une mutation décisive est supposée constante, certainement à tort. La représentation graphique (Figure) est particulièrement éclairante en révélant une superposition de courbes représentatives de l’échappement viral : on voit que la probabilité de celui-ci augmente assez nettement avec le nombre de cas de l’infection.
Figure : risque qu’au moins un variant échappant au vaccin apparaisse par mois en fonction de différents nombres de cas quotidiens

Diminuer le nombre de cas pour réduire le risque de mutation
Il n’est pas question de juger de l’exactitude de la formulation mathématique du problème qui vaut ce qu’elle vaut face à la complexité de la réalité épidémiologique du moment et de l’augmentation des capacités vaccinales. Plus simplement, cette approche réductrice a le mérite de confirmer que la baisse du nombre de cas n’a pas pour seul effet de limiter la pression sur les systèmes de santé : c’est aussi l’un des meilleurs moyens pour diminuer le risque d’échappement vaccinal.
Si les vaccins permettent de réduire le nombre de cas notamment graves de la maladie, il ne faut pas pour autant oublier les autres mesures dites non pharmacologiques qui visent à compléter leur action sanitaire. Parmi les questions les plus brûlantes dans le contexte épidémique actuel, il en est une qui devrait trouver une réponse dans le cadre de cette réflexion autour d’une équation simplificatrice : faut-il vacciner le plus de monde possible en espaçant au maximum les injections ou moins de monde en gardant le rythme défini par les essais randomisés qui ont conduit au développement des vaccins ?
Et donc procurer une protection même moyenne au plus grand nombre de personnes possible
La réponse ne coule pas de source, mais intuitivement, il semble qu’une protection même moyenne du plus grand nombre (stratégie qu’a choisie la Grande Bretagne dès la mise à disposition des vaccins) soit à court terme plus efficace qu’une protection totale d’un nombre en théorie deux fois moindre, dès lors que la stratégie vaccinale est complétée par le maintien des mesures de restriction sanitaire et des gestes barrières. Les deux moyens conjugués doivent contenir la propagation de l’épidémie à court terme en sachant que la deuxième injection du vaccin répond aux besoins à long terme.
Face à une épidémie qui flambe, la rapidité de l’action est à l’évidence déterminante pour couper court au déploiement du virus en lui enlevant l’opportunité de muter à sa guise et de se transmettre avec une puissance croissante au gré des variants les plus adaptés à sa survie.
Il faut cependant admettre que l’équation commentée est plus propice à la réflexion qu’à la prédiction. En effet, pour être plus exact, il faudrait l’enrichir de variables complexes prenant en compte la fréquence des mutations décisives en plus de leur probabilité, ce qui se heurte à des processus tout aussi stochastiques que les autres, qu’il s’agisse de la susceptibilité individuelle à l’infection ou encore de la pathogénicité des variants. Ce qui va au-delà de la puissance des mathématiques et de la modélisation de tels processus.
Dr Philippe Tellier
Référence
Thompson RN et coll. : SARS-CoV-2 incidence and vaccine escape. Lancet Infect Dis 2021 (13 avril) : publication avancée en ligne le 13 avril. doi.org/10.1016/ S1473-3099(21)00202-4.
Il faut bien une seule dose de vaccin à mARN après une Covid-19
Chez les patients qui ont contracté la Covid-19 dans les mois précédents, des stratégies vaccinales spécifiques semblent pouvoir être envisagées. Pourquoi en effet administrer deux doses espacées de trois semaines alors qu’une dose unique pourrait suffire au vu de la réponse immunitaire naturelle tant humorale que cellulaire induite par l’infection inaugurale ? Certaines petites études récentes qui portent sur des effectifs restreints plaident en faveur de ce choix qui concilie des arguments à la fois immunologiques et économiques.
Un choix qui a déjà été fait par les autorités sanitaires de certains pays, et qui est au demeurant conforté par une étude de cohorte récente dont les résultats viennent d’être publiés en ligne le 1er avril dans Nature Medicine.
La population étudiée se compose de 1 090 professionnels de santé (âge moyen 41,9 ± 12,2 ans ; femmes : 60,7 % ; non-Blancs : 53,3 %) recrutés dans un grand centre hospitalo-universitaire en Californie du sud et tous candidats à la vaccination contre la Covid-19 au moyen d’un vaccin à mARN, en l’occurrence le BNT162b2 (Pfizer–BioNTech). Au sein de cette cohorte, ont été distingués deux sous-groupes : dans l’un (n = 35), les participants avaient été préalablement atteints de la Covid-19, alors que, dans l’autre (n = 228), il n’existait aucun antécédent de ce type. Ces derniers ont reçu deux doses du vaccin, espacées de trois semaines, tandis que les premiers n’ont reçu qu’une dose.
Immunité humorale apparemment optimale avec une dose unique en cas de Covid-19 antérieure
Les concentrations sériques d’anticorps IgG neutralisants, dirigés contre le domaine RBD de la protéine spike virale (IgG [S-RBD]), ont été systématiquement dosées à intervalles réguliers au cours des trois semaines qui ont suivi les injections dans les deux groupes. La comparaison des courbes sériques correspondantes et des taux d’anticorps IgG [S-RBD] n’a révélé aucune différence intergroupe significative.
Si l’on se fixe un seuil quantitatif > 4 160 UA ml−1 pour ces concentrations -lequel correspond à une immunité jugée optimale in vitro à partir du test de séroneutralisation par réduction des plaques- il s’avère qu’il a été atteint moins fréquemment dans le groupe des patients infectés et vaccinés avec un dose unique (p < 0,001 versus l’autre groupe). Ce critère d’efficacité est cependant secondaire par rapport à l’évaluation de la réponse immunitaire humorale précédemment évoqvitrouée qui a par ailleurs été complétée par une étude de la neutralisation du récepteur ACE2 par ces anticorps : aucune différence n’a été corrélée au nombre de doses administrées, certains participants déjà infectés ayant bénéficié finalement de la vaccination en deux temps.
Cette étude de cohorte a le mérite de porter sur un effectif conséquent plutôt hétérogène quant aux stratégies vaccinales adoptées en fonction de l’exposition antérieure éventuelle à la Covid-19. Les résultats tendent à conforter le choix d’ores et déjà effectué par certaines autorités sanitaires : en cas d’antécédent confirmé de de la maladie, une dose unique de vaccin à ARN semble suffisante pour déclencher une réponse immunitaire humorale qui équivaut à celle obtenue avec deux injections chez des sujets qui n’ont jamais été exposés au SARS-CoV-2. Parmi les limites de cette étude, il faut souligner la durée de la période d’observation post-vaccinale qui n’excède pas trois semaines et qui pose la question de la durée de la protection conférée par le vaccin.
Dr Philippe Tellier
Référence
Ebinger JE et coll. : Antibody responses to the BNT162b2 mRNA vaccine in individuals previously infected with SARS-CoV-2. Nat Med., 2021 ; publication avancée en ligne le 1er avril. doi: 10.1038/s41591-021-01325-6.
_____
Publié le 16/04/2021
Echappement vaccinal : sortez vos cahiers de maths !
L’échappement vaccinal en cette période de pandémie interminable prend désormais des proportions inquiétantes dans certains pays comme le Brésil ou l’Afrique du sud. L’apparition de variants du SARS-CoV-2 et la durée limitée de l’immunité qu’elle soit naturelle ou post-vaccinale sont deux facteurs largement impliqués dans ce phénomène. Mais il en est un autre qui pourrait intervenir comme le suggère l’intuition épidémiologique et biologique. La probabilité de l’échappement aux vaccins est en effet également conditionnée par la circulation du virus : plus elle est importante, plus les mutations s’accumulent, le nombre de ces dernières étant positivement corrélé au nombre gigantesque des copies du génome viral lorsque virus passe d’un hôte à l’autre. La sélection darwinienne vient compléter l’ouvrage en favorisant les variants les plus résistants et c’est ce qui se passe en ce moment avec le risque de mettre les politiques vaccinales en échec.
Une équation simple et quelques (mutations) inconnues
Une modélisation mathématique peut permettre de quantifier ce processus. Il suffit de mettre au point une équation probabiliste « simple » qui établit une relation non linéaire entre la probabilité de l’échappement vaccinal et le nombre de cas quotidiens de la Covid-19 (N).
La démonstration ou plutôt l’illustration vaut pour le Royaume-Uni où un modèle a été utilisé pour aboutir à la formule suivante qui ne tombe pas du ciel mais sort d’instituts spécialisés dans les mathématiques appliquées :
Risque d’échappement vaccinal au cours d’une période donnée = 1- (1-p) N
où p représente la probabilité d’une mutation décisive par infection et N le nombre de cas quotidiens observés pendant cette période.
Il apparaît en effet que le risque est positivement corrélé au nombre de cas quotidiens, étant entendu que la probabilité d’une mutation décisive est supposée constante, certainement à tort. La représentation graphique (Figure) est particulièrement éclairante en révélant une superposition de courbes représentatives de l’échappement viral : on voit que la probabilité de celui-ci augmente assez nettement avec le nombre de cas de l’infection.
Figure : risque qu’au moins un variant échappant au vaccin apparaisse par mois en fonction de différents nombres de cas quotidiens

Diminuer le nombre de cas pour réduire le risque de mutation
Il n’est pas question de juger de l’exactitude de la formulation mathématique du problème qui vaut ce qu’elle vaut face à la complexité de la réalité épidémiologique du moment et de l’augmentation des capacités vaccinales. Plus simplement, cette approche réductrice a le mérite de confirmer que la baisse du nombre de cas n’a pas pour seul effet de limiter la pression sur les systèmes de santé : c’est aussi l’un des meilleurs moyens pour diminuer le risque d’échappement vaccinal.
Si les vaccins permettent de réduire le nombre de cas notamment graves de la maladie, il ne faut pas pour autant oublier les autres mesures dites non pharmacologiques qui visent à compléter leur action sanitaire. Parmi les questions les plus brûlantes dans le contexte épidémique actuel, il en est une qui devrait trouver une réponse dans le cadre de cette réflexion autour d’une équation simplificatrice : faut-il vacciner le plus de monde possible en espaçant au maximum les injections ou moins de monde en gardant le rythme défini par les essais randomisés qui ont conduit au développement des vaccins ?
Et donc procurer une protection même moyenne au plus grand nombre de personnes possible
La réponse ne coule pas de source, mais intuitivement, il semble qu’une protection même moyenne du plus grand nombre (stratégie qu’a choisie la Grande Bretagne dès la mise à disposition des vaccins) soit à court terme plus efficace qu’une protection totale d’un nombre en théorie deux fois moindre, dès lors que la stratégie vaccinale est complétée par le maintien des mesures de restriction sanitaire et des gestes barrières. Les deux moyens conjugués doivent contenir la propagation de l’épidémie à court terme en sachant que la deuxième injection du vaccin répond aux besoins à long terme.
Face à une épidémie qui flambe, la rapidité de l’action est à l’évidence déterminante pour couper court au déploiement du virus en lui enlevant l’opportunité de muter à sa guise et de se transmettre avec une puissance croissante au gré des variants les plus adaptés à sa survie.
Il faut cependant admettre que l’équation commentée est plus propice à la réflexion qu’à la prédiction. En effet, pour être plus exact, il faudrait l’enrichir de variables complexes prenant en compte la fréquence des mutations décisives en plus de leur probabilité, ce qui se heurte à des processus tout aussi stochastiques que les autres, qu’il s’agisse de la susceptibilité individuelle à l’infection ou encore de la pathogénicité des variants. Ce qui va au-delà de la puissance des mathématiques et de la modélisation de tels processus.
Dr Philippe Tellier
Référence
Thompson RN et coll. : SARS-CoV-2 incidence and vaccine escape. Lancet Infect Dis 2021 (13 avril) : publication avancée en ligne le 13 avril. doi.org/10.1016/ S1473-3099(21)00202-4.
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Les infirmiers seront enregistrés au répertoire RPPS par l’Ordre dès la fin septembre
19 mai 2021
Les infirmiers seront enregistrés au répertoire partagé des professionnels de santé (RPPS) par l'Ordre national des infirmiers (ONI) à partir de la fin septembre.
Les infirmiers seront enregistrés au répertoire RPPS par l'Ordre dès la fin septembre
Cette nouvelle modalité d'enregistrement sera "similaire aux autres professions à ordre (médecins, chirurgiens-dentistes, sages-femmes, pharmaciens, masseurs-kinésithérapeutes et pédicure-podologues)", fait savoir l'ONI.
Elle n'impliquera plus de démarches d'enregistrement auprès des Agences régionales de santé (ARS) pour les infirmiers.
Pour les infirmiers déjà inscrits à l'ONI, la transition sera automatique : leur numéro national RPPS (11 chiffres) leur sera communiqué par l'ONI et ils pourront le trouver dans l'annuaire santé. Ils pourront mentionner ce numéro RPPS sur les différents documents qu'ils éditent et l'utiliser pour toutes leurs démarches. rpp
Pour les infirmiers non encore inscrits à l'ONI, "c'est l'occasion de s'y inscrire sur le portail dédié", indique l'instance. Ces derniers pourront, par exemple, utiliser FranceConnect, qui a récemment été implanté sur le site de l'Ordre.
Les identifiants départementaux ADELI des infirmiers ne seront plus utilisés. En revanche, le numéro d'Assurance Maladie, dit "AM", à vocation de facturation, ne changera pas.
Outils numériques
L'enregistrement au RPPS avec les bonnes coordonnées de contact (numéro de mobile et adresse électronique) permet aux infirmiers d'activer une application mobile 'e-CPS' sur leur smartphone, fait savoir l'ONI.
"Avec cette application, simple et sécurisée, ils pourront accéder en mobilité à de multiples services numériques en santé ayant déjà intégré Pro Santé Connect (fédérateur permettant de se connecter soir avec sa carte CPS, soit avec son application mobile e-CPS)."
Grâce à une procédure anticipée, plus de 35 000 infirmiers ont déjà téléchargé et activé leur application mobile e-CPS, principalement pour la connexion aux services Vaccin Covid (permettant de réaliser la traçabilité vaccinale" et SI-DEP (permettant de renseigner les résultats des tests antigéniques).
Pour les infirmiers transmettant des feuilles de soins électroniques, ceux qui travaillent dans des établissements qui ont systématisé l'usage de la carte CPS, et ceux qui manifestent leur intérêt à en être dotés, l'inscription au RPPS "permet aussi d'obtenir une carte CPS", précise l'ONI.
Rédaction ActuSoins
19 mai 2021
Les infirmiers seront enregistrés au répertoire partagé des professionnels de santé (RPPS) par l'Ordre national des infirmiers (ONI) à partir de la fin septembre.
Les infirmiers seront enregistrés au répertoire RPPS par l'Ordre dès la fin septembre
Cette nouvelle modalité d'enregistrement sera "similaire aux autres professions à ordre (médecins, chirurgiens-dentistes, sages-femmes, pharmaciens, masseurs-kinésithérapeutes et pédicure-podologues)", fait savoir l'ONI.
Elle n'impliquera plus de démarches d'enregistrement auprès des Agences régionales de santé (ARS) pour les infirmiers.
Pour les infirmiers déjà inscrits à l'ONI, la transition sera automatique : leur numéro national RPPS (11 chiffres) leur sera communiqué par l'ONI et ils pourront le trouver dans l'annuaire santé. Ils pourront mentionner ce numéro RPPS sur les différents documents qu'ils éditent et l'utiliser pour toutes leurs démarches. rpp
Pour les infirmiers non encore inscrits à l'ONI, "c'est l'occasion de s'y inscrire sur le portail dédié", indique l'instance. Ces derniers pourront, par exemple, utiliser FranceConnect, qui a récemment été implanté sur le site de l'Ordre.
Les identifiants départementaux ADELI des infirmiers ne seront plus utilisés. En revanche, le numéro d'Assurance Maladie, dit "AM", à vocation de facturation, ne changera pas.
Outils numériques
L'enregistrement au RPPS avec les bonnes coordonnées de contact (numéro de mobile et adresse électronique) permet aux infirmiers d'activer une application mobile 'e-CPS' sur leur smartphone, fait savoir l'ONI.
"Avec cette application, simple et sécurisée, ils pourront accéder en mobilité à de multiples services numériques en santé ayant déjà intégré Pro Santé Connect (fédérateur permettant de se connecter soir avec sa carte CPS, soit avec son application mobile e-CPS)."
Grâce à une procédure anticipée, plus de 35 000 infirmiers ont déjà téléchargé et activé leur application mobile e-CPS, principalement pour la connexion aux services Vaccin Covid (permettant de réaliser la traçabilité vaccinale" et SI-DEP (permettant de renseigner les résultats des tests antigéniques).
Pour les infirmiers transmettant des feuilles de soins électroniques, ceux qui travaillent dans des établissements qui ont systématisé l'usage de la carte CPS, et ceux qui manifestent leur intérêt à en être dotés, l'inscription au RPPS "permet aussi d'obtenir une carte CPS", précise l'ONI.
Rédaction ActuSoins
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Des scientifiques ont fait « respirer » des animaux par l'anus !
La ventilation artificielle est une procédure invasive qui peut causer des lésions aux poumons et mobilise beaucoup de personnel. Des chercheurs japonais proposent d'administrer l'oxygène par l'anus comme un simple lavement. Une technique apparemment très efficace et sans danger.
À l'instar de la Covid-19, de nombreuses pathologies engendrent une insuffisance respiratoire nécessitant une ventilation artificielle. Cette dernière s'effectue via une sonde d'intubation délivrant l'oxygène dans les poumons. Le problème, c'est que cette procédure invasive peut elle-même causer des dommages aux poumons, sans parler des risques de contamination par des bactéries provenant de la bouche et de l'impossibilité de s'alimenter.
Ryo Okabe et ses collègues de l'Université médicale et dentaire de Tokyo (TMDU) ont donc pensé à une autre piste : injecter l'oxygène... via le rectum. Certains animaux, comme les loches (un poisson d'eau douce), les tortues, les concombres de mer ont en effet développé un mode respiratoire alternatif lorsque la disponibilité en oxygène est limitée : ils absorbent l'air par l'anus, qui va ensuite distribuer l'oxygène dans l'organisme via la paroi intestinale.
Une technique inspirée des suppositoires
« Le rectum possède un maillage de vaisseaux sanguins très fins juste sous la surface de sa muqueuse, ce qui signifie que les médicaments administrés par l'anus sont facilement absorbés dans la circulation sanguine », explique Ryo Okabe. C'est sur ce principe que s'appuient les suppositoires « nous nous sommes donc demandé si l'oxygène pouvait être délivré de la même manière ».
Les chercheurs ont d'abord pensé à administrer l'oxygène dans le rectum sous forme gazeuse. Mais, bien que la procédure s'avère efficace chez la souris, elle nécessite de « frotter » la paroi du rectum pour augmenter le flux sanguin et favoriser les échanges gazeux. On imagine que ça ne doit pas être franchement agréable. Ryo Okabe a alors pensé à une autre méthode, à savoir la diffusion par le rectum de perfluorodécaline oxygénée, un liquide semblable à celui que l'on utilise chez les bébés prématurés et pouvant transporter de grandes quantités d'oxygène et de dioxyde de carbone. Ils ont placé des cobayes animaux (souris, porc et rat) sous hypoxie, puis ont appliqué leur traitement.
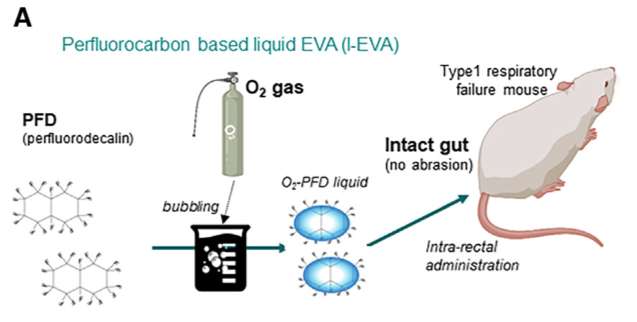
La perfluorodécaline oxygénée est injectée dans l’anus comme pour un lavement. © Ryo Okabe et al, mes, 2021
Aucun effet secondaire
Les animaux n'exprimaient plus de détresse respiratoire et ont vu leur oxygénation sanguine améliorée. « Il est intéressant de constater que la ventilation par voie rectale nécessite deux à trois fois moins de liquide que si on l'injectait par les poumons », écrivent aussi les auteurs dans leur étude publiée dans la revue Med. Les chercheurs ont aussi précisé que la petite proportion de liquide absorbée en même temps que l'oxygène n'avait causé aucun effet nocif et n'avait pas perturbé les bactéries intestinales, indiquant que la méthode était sûre.
Moins de personnel et de matériel coûteux
« C'est une idée qui peut paraître provocante, mais qui doit être prise très au sérieux », juge Caleb Kelly, de l'École de médecine de l'université de Yale, dans un commentaire accompagnant l'étude. Cette méthode, qui s'apparente à un simple lavement, pourrait ainsi grandement faciliter la guérison des patients en insuffisance respiratoire ou pour remplacer l'oxygénation par membrane extracorporelle (EMCO), utilisée notamment dans les cas graves de Covid. Elle mobiliserait également moins de personnel soignant et de matériel coûteux. Voilà qui aurait bien été utile ces derniers mois dans les services de réanimation.
-----
Un vaccin contre (presque) tous les coronavirus ?
Publiés en accéléré dans la revue Nature, des résultats d'une expérience récente effectuée sur des singes suggèrent qu'un vaccin multimérique à nanoparticules pourrait s'avérer efficace contre les coronavirus qui se lient aux récepteurs ACE2.
Dans une récente étude publiée dans la revue Nature qui a fait l'objet d'une relecture accélérée par les pairs, des chercheurs américains expliquent comment ils ont mis au point un vaccin multimérique efficace contre tous les coronavirus qui expriment le site de liaison permettant au virus de « s'accrocher » sur nos récepteurs ACE2.
Une publication un peu trop ambitieuse
Dans leur article, les chercheurs suggèrent que leur vaccin pourrait être un vaccin « pan-coronavirus », c'est-à-dire, lutter contre tous les coronavirus. Une dénomination qui n'a pas manqué de surprendre Branka Horvat, directrice de l'équipe Immunobiologie des infections virales au Centre international de recherche en infectiologie (Ciri) à Lyon : « Cette équipe est parvenue à mettre au point un vaccin qui contient une région de la protéine Spike des coronavirus (RBD, pour recepteur-binding domaine) qui se lie à nos récepteurs ACE2. Bien que ce travail présente la preuve de concept de faisabilité de la mise en place d'un vaccin qui protège contre plusieurs coronavirus, je trouve un peu prétentieux l'appellation pan-coronavirus. Un tel vaccin, par exemple, ne pourra pas être utile contre le MERS-CoV étant donné que ce dernier ne se lie pas à ACE2 et possède la région RBD différente, ni contre des autres coronavirus "pré-émergents", qui utilisent d'autres récepteurs pour entrer dans la cellule ».
Grâce à la ferritine nanoparticulaire obtenue à partir d'une bactérie, les scientifiques ont pu élaborer leur vaccin qui contient une région multimérique de la protéine Spike contenant 200 acides aminés. En plus de cela, le vaccin contient des agonistes de certains récepteurs cruciaux du système immunitaire inné absorbé dans de l'aluminium. « Ce vaccin est immunogène car il utilise la stimulation des récepteurs TL7 et 8, ce qui va induire une réponse immunitaire globale plus forte. Il n'en reste pas moins que la région peptidique présente dans le vaccin est courte et reste spécifique pour les coronavirus se liant à ACE2 », explique Branka Horvat.
La durée de l'immunité : l'angle mort de l'étude
Dans l'expérience, les singes vaccinés avec le vaccin à nanoparticules développent beaucoup plus d'anticorps neutralisants que ceux ayant reçu un vaccin ARN ou que des patients avec Covid-19. Après une infection intranasale ou intratrachéale à des coronavirus, le matériel génétique des virus ainsi que le virus infectieux sont absents des voies respiratoires inférieures et supérieures chez le groupe vacciné avec des nanoparticules. Enfin, lors d'analyses histologiques, on constate également une accumulation des cellules inflammatoires bien moindres dans des poumons chez ce groupe vacciné.
Malgré tout, un élément crucial n'est pas étudié par les investigateurs : la durée de l'immunité. « La question de la durée de l'immunité reste mitigée concernant les vaccins contre la Covid-19. Ici, les chercheurs n'étudient l'immunité des singes que pendant dix semaines suite à la première injection d'un vaccin. Cela aurait été intéressant de poursuivre l'étude pour mieux cerner la protection immunitaire conférée par ce vaccin », précise Branka Horvat.
L'ambition de cette équipe ne peut que rendre enthousiaste. Pour autant, Branka Horvat prévient que, avec la pandémie actuelle, « il est devenu très à la mode de survendre des résultats concernant les coronavirus ». Et la chercheuse de tempérer son propos : « Leur plateforme de développement vaccinale est très intéressante mais il faudra encore que ce type de vaccins montre son efficacité dans d'autres tests avant de pouvoir être accepté pour des tests cliniques chez l'Homme et constater s'ils sont plus avantageux que les vaccins déjà disponibles ou en cours de développement. Néanmoins, c'est une bonne chose que les essais se multiplient. Plus nous avons d'études, plus nous avons de chance de trouver des solutions efficaces contre les virus connus et émergents ».
Alors que les différents variants du SARS-CoV-2 font craindre une baisse d'efficacité des vaccins actuels, plusieurs start-up travaillent sur un vaccin universel, capable de produire une réponse immunitaire quelles que soient les mutations. Tour d'horizon des différentes technologies et de leur état d'avancement.
L'apparition de plusieurs variantes du SARS-CoV-2 nous a appris que le virus peut muter d'un moment à l'autre. Pour l'instant, ces mutations ne semblent pas menacer l'efficacité des vaccins actuels, mais d'autres, plus importantes, pourraient annihiler les efforts des campagnes de vaccination en cours. Plusieurs start-up planchent donc sur des vaccins universels, capables de fournir une protection quelle que soit la souche de coronavirus.
Osivax : de la grippe au coronavirus
Parmi ces biotechs, la société lyonnaise Osivax, qui travaillait jusqu'ici sur un vaccin universel contre la grippe. Sa cible : la nucléocapside, un antigène interne du virus qui est très bien conservé entre les différentes souches de coronavirus. « La nucléocapside est conservée à plus de 89 % entre le SARS-CoV-1 apparu en 2003 et le SARS-CoV-2 actuel », assure la start-up. Le problème, c'est que cet antigène, comme il se situe à l'intérieur du virus, n'est pas visible par les anticorps comme les protéines de pointe S, situées à la surface du virus et qui sont la cible des vaccins classiques. Ce type de vaccin repose donc sur la seule réponse immunitaire cellulaire des lymphocytes T. Cette dernière est déclenchée par une protéine contenue dans le vaccin. « Ce qui est assez unique dans notre technologie, c'est qu'on arrive à stimuler l'immunité cellulaire avec un vaccin protéique, sans utiliser les technologies d'ARN messager ou de vecteurs viraux », insiste la jeune pousse, qui espère entrer dans la phase d'essai clinique fin 2021 en collaboration avec l'AP-HP.
Phylex BioSciences : un pseudo-virus piqué d’antigènes
D'autres start-up ont adopté une approche différente. C'est le cas de Phylex BioSciences, une biotech installée en Californie mais dont le patron, Pascal Brandys, est français, à l'instar de celui de Moderna. Ce dernier s'est associé à Jens Herold, un spécialiste des coronavirus, qui dirige l'unité biopharmaceutique Boehringer Ingelheim. Les deux hommes avaient déjà cofondé en 2003 une start-up pour développer un vaccin contre le SARS-CoV-1, mais dont les recherches n'avaient pas été menées à leur terme du fait de la disparition du virus. Les deux associés ont donc recréé une nouvelle société, en mars 2020, spécialement pour répondre à la pandémie de SARS-CoV-2.
Un vaccin universel est la seule réponse durable étant donné que les mutations vont s’accumuler au fil du temps
Comme les vaccins classiques, Phylex BioSciences utilise la protéine S du virus, mais uniquement sur sa partie stable. Une soixantaine de ces fragments sont ensuite assemblés sur une structure 3D imitant la protéine entière dans une particule pseudo-virale. « Les épitopes sont ainsi présentés aux anticorps dans la même configuration que la vraie protéine de pointe, explique Pascal Brandys. Nous avons environ un an de retard sur les vaccins comme Moderna », reconnaît le dirigeant, qui mise sur un essai clinique de phase 3 fin 2021. Mais son vaccin sera efficace sur tous les futurs variants. « Un vaccin universel basé sur les régions conservées du virus est la seule réponse durable de vaccination, étant donné que les mutations vont s'accumuler au fil du temps », assure-t-il. Phylex Bioscience a d'ores et déjà signé un partenariat avec la société californienne Atum pour la fabrication de son vaccin en grande quantité.
eTheRNA, un vaccin en spray nasal
Une autre biotech belge, eTheRNA, travaille sur un projet similaire à celui de Phylex Bioscience. Comme elle, elle utilise la partie conservée de la protéine de pointe, identique chez tous les coronavirus. Mais son vaccin serait commercialisé sous forme de spray nasal. « Cela présente l'avantage d'être facile à administrer. Et ne nécessite pas d'injection », explique Bernard Sagaert, directeur de production chez eTheRNA. Un laboratoire pharmaceutique chinois a récemment investi dans la société, ce qui devrait lui ouvrir le marché chinois et permettre une fabrication à grande échelle.
VBI Vaccines, un vaccin multipotent
Enfin, la société canadienne VBI Vaccines joue une carte encore différente, même si elle recourt comme Phylex à une particule pseudo-virale. La start-up conçoit un vaccin trivalent contre le SARS-CoV-1, le SARS-CoV-2 et le MERS, en multipliant les antigènes à la surface de son faux virus. Plutôt que de sélectionner la partie fixe, elle inclut donc le plus grand nombre possible d'antigènes connus. Rien ne permet cependant de dire que ce vaccin multiple répondra aux futures mutations.
Course de vitesse contre les mutants
Un vaccin universel contre le coronavirus a-t-il des chances de voir le jour rapidement ? Rien n'est moins sûr : les scientifiques s'échinent depuis des années à mettre au point un tel vaccin contre la grippe (qui doit aujourd'hui être renouvelé chaque année). Mais après tout, la pandémie a montré qu'il était possible de produire un vaccin entièrement nouveau en moins de neuf mois contre une dizaine d'années en temps normal. En attendant l'aboutissement de tous ces projets, Moderna assure qu'il est capable de fabriquer un nouveau vaccin en moins de six semaines, simplement en modifiant son code source. Mais cela suppose de relancer tout le processus de fabrication et de revacciner toutes les personnes ayant déjà reçu l'ancien vaccin. Une opération terriblement coûteuse.
source futura sciences.
La ventilation artificielle est une procédure invasive qui peut causer des lésions aux poumons et mobilise beaucoup de personnel. Des chercheurs japonais proposent d'administrer l'oxygène par l'anus comme un simple lavement. Une technique apparemment très efficace et sans danger.
À l'instar de la Covid-19, de nombreuses pathologies engendrent une insuffisance respiratoire nécessitant une ventilation artificielle. Cette dernière s'effectue via une sonde d'intubation délivrant l'oxygène dans les poumons. Le problème, c'est que cette procédure invasive peut elle-même causer des dommages aux poumons, sans parler des risques de contamination par des bactéries provenant de la bouche et de l'impossibilité de s'alimenter.
Ryo Okabe et ses collègues de l'Université médicale et dentaire de Tokyo (TMDU) ont donc pensé à une autre piste : injecter l'oxygène... via le rectum. Certains animaux, comme les loches (un poisson d'eau douce), les tortues, les concombres de mer ont en effet développé un mode respiratoire alternatif lorsque la disponibilité en oxygène est limitée : ils absorbent l'air par l'anus, qui va ensuite distribuer l'oxygène dans l'organisme via la paroi intestinale.
Une technique inspirée des suppositoires
« Le rectum possède un maillage de vaisseaux sanguins très fins juste sous la surface de sa muqueuse, ce qui signifie que les médicaments administrés par l'anus sont facilement absorbés dans la circulation sanguine », explique Ryo Okabe. C'est sur ce principe que s'appuient les suppositoires « nous nous sommes donc demandé si l'oxygène pouvait être délivré de la même manière ».
Les chercheurs ont d'abord pensé à administrer l'oxygène dans le rectum sous forme gazeuse. Mais, bien que la procédure s'avère efficace chez la souris, elle nécessite de « frotter » la paroi du rectum pour augmenter le flux sanguin et favoriser les échanges gazeux. On imagine que ça ne doit pas être franchement agréable. Ryo Okabe a alors pensé à une autre méthode, à savoir la diffusion par le rectum de perfluorodécaline oxygénée, un liquide semblable à celui que l'on utilise chez les bébés prématurés et pouvant transporter de grandes quantités d'oxygène et de dioxyde de carbone. Ils ont placé des cobayes animaux (souris, porc et rat) sous hypoxie, puis ont appliqué leur traitement.

La perfluorodécaline oxygénée est injectée dans l’anus comme pour un lavement. © Ryo Okabe et al, mes, 2021
Aucun effet secondaire
Les animaux n'exprimaient plus de détresse respiratoire et ont vu leur oxygénation sanguine améliorée. « Il est intéressant de constater que la ventilation par voie rectale nécessite deux à trois fois moins de liquide que si on l'injectait par les poumons », écrivent aussi les auteurs dans leur étude publiée dans la revue Med. Les chercheurs ont aussi précisé que la petite proportion de liquide absorbée en même temps que l'oxygène n'avait causé aucun effet nocif et n'avait pas perturbé les bactéries intestinales, indiquant que la méthode était sûre.
Moins de personnel et de matériel coûteux
« C'est une idée qui peut paraître provocante, mais qui doit être prise très au sérieux », juge Caleb Kelly, de l'École de médecine de l'université de Yale, dans un commentaire accompagnant l'étude. Cette méthode, qui s'apparente à un simple lavement, pourrait ainsi grandement faciliter la guérison des patients en insuffisance respiratoire ou pour remplacer l'oxygénation par membrane extracorporelle (EMCO), utilisée notamment dans les cas graves de Covid. Elle mobiliserait également moins de personnel soignant et de matériel coûteux. Voilà qui aurait bien été utile ces derniers mois dans les services de réanimation.
-----
Un vaccin contre (presque) tous les coronavirus ?
Publiés en accéléré dans la revue Nature, des résultats d'une expérience récente effectuée sur des singes suggèrent qu'un vaccin multimérique à nanoparticules pourrait s'avérer efficace contre les coronavirus qui se lient aux récepteurs ACE2.
Dans une récente étude publiée dans la revue Nature qui a fait l'objet d'une relecture accélérée par les pairs, des chercheurs américains expliquent comment ils ont mis au point un vaccin multimérique efficace contre tous les coronavirus qui expriment le site de liaison permettant au virus de « s'accrocher » sur nos récepteurs ACE2.
Une publication un peu trop ambitieuse
Dans leur article, les chercheurs suggèrent que leur vaccin pourrait être un vaccin « pan-coronavirus », c'est-à-dire, lutter contre tous les coronavirus. Une dénomination qui n'a pas manqué de surprendre Branka Horvat, directrice de l'équipe Immunobiologie des infections virales au Centre international de recherche en infectiologie (Ciri) à Lyon : « Cette équipe est parvenue à mettre au point un vaccin qui contient une région de la protéine Spike des coronavirus (RBD, pour recepteur-binding domaine) qui se lie à nos récepteurs ACE2. Bien que ce travail présente la preuve de concept de faisabilité de la mise en place d'un vaccin qui protège contre plusieurs coronavirus, je trouve un peu prétentieux l'appellation pan-coronavirus. Un tel vaccin, par exemple, ne pourra pas être utile contre le MERS-CoV étant donné que ce dernier ne se lie pas à ACE2 et possède la région RBD différente, ni contre des autres coronavirus "pré-émergents", qui utilisent d'autres récepteurs pour entrer dans la cellule ».
Grâce à la ferritine nanoparticulaire obtenue à partir d'une bactérie, les scientifiques ont pu élaborer leur vaccin qui contient une région multimérique de la protéine Spike contenant 200 acides aminés. En plus de cela, le vaccin contient des agonistes de certains récepteurs cruciaux du système immunitaire inné absorbé dans de l'aluminium. « Ce vaccin est immunogène car il utilise la stimulation des récepteurs TL7 et 8, ce qui va induire une réponse immunitaire globale plus forte. Il n'en reste pas moins que la région peptidique présente dans le vaccin est courte et reste spécifique pour les coronavirus se liant à ACE2 », explique Branka Horvat.
La durée de l'immunité : l'angle mort de l'étude
Dans l'expérience, les singes vaccinés avec le vaccin à nanoparticules développent beaucoup plus d'anticorps neutralisants que ceux ayant reçu un vaccin ARN ou que des patients avec Covid-19. Après une infection intranasale ou intratrachéale à des coronavirus, le matériel génétique des virus ainsi que le virus infectieux sont absents des voies respiratoires inférieures et supérieures chez le groupe vacciné avec des nanoparticules. Enfin, lors d'analyses histologiques, on constate également une accumulation des cellules inflammatoires bien moindres dans des poumons chez ce groupe vacciné.
Malgré tout, un élément crucial n'est pas étudié par les investigateurs : la durée de l'immunité. « La question de la durée de l'immunité reste mitigée concernant les vaccins contre la Covid-19. Ici, les chercheurs n'étudient l'immunité des singes que pendant dix semaines suite à la première injection d'un vaccin. Cela aurait été intéressant de poursuivre l'étude pour mieux cerner la protection immunitaire conférée par ce vaccin », précise Branka Horvat.
L'ambition de cette équipe ne peut que rendre enthousiaste. Pour autant, Branka Horvat prévient que, avec la pandémie actuelle, « il est devenu très à la mode de survendre des résultats concernant les coronavirus ». Et la chercheuse de tempérer son propos : « Leur plateforme de développement vaccinale est très intéressante mais il faudra encore que ce type de vaccins montre son efficacité dans d'autres tests avant de pouvoir être accepté pour des tests cliniques chez l'Homme et constater s'ils sont plus avantageux que les vaccins déjà disponibles ou en cours de développement. Néanmoins, c'est une bonne chose que les essais se multiplient. Plus nous avons d'études, plus nous avons de chance de trouver des solutions efficaces contre les virus connus et émergents ».
Alors que les différents variants du SARS-CoV-2 font craindre une baisse d'efficacité des vaccins actuels, plusieurs start-up travaillent sur un vaccin universel, capable de produire une réponse immunitaire quelles que soient les mutations. Tour d'horizon des différentes technologies et de leur état d'avancement.
L'apparition de plusieurs variantes du SARS-CoV-2 nous a appris que le virus peut muter d'un moment à l'autre. Pour l'instant, ces mutations ne semblent pas menacer l'efficacité des vaccins actuels, mais d'autres, plus importantes, pourraient annihiler les efforts des campagnes de vaccination en cours. Plusieurs start-up planchent donc sur des vaccins universels, capables de fournir une protection quelle que soit la souche de coronavirus.
Osivax : de la grippe au coronavirus
Parmi ces biotechs, la société lyonnaise Osivax, qui travaillait jusqu'ici sur un vaccin universel contre la grippe. Sa cible : la nucléocapside, un antigène interne du virus qui est très bien conservé entre les différentes souches de coronavirus. « La nucléocapside est conservée à plus de 89 % entre le SARS-CoV-1 apparu en 2003 et le SARS-CoV-2 actuel », assure la start-up. Le problème, c'est que cet antigène, comme il se situe à l'intérieur du virus, n'est pas visible par les anticorps comme les protéines de pointe S, situées à la surface du virus et qui sont la cible des vaccins classiques. Ce type de vaccin repose donc sur la seule réponse immunitaire cellulaire des lymphocytes T. Cette dernière est déclenchée par une protéine contenue dans le vaccin. « Ce qui est assez unique dans notre technologie, c'est qu'on arrive à stimuler l'immunité cellulaire avec un vaccin protéique, sans utiliser les technologies d'ARN messager ou de vecteurs viraux », insiste la jeune pousse, qui espère entrer dans la phase d'essai clinique fin 2021 en collaboration avec l'AP-HP.
Phylex BioSciences : un pseudo-virus piqué d’antigènes
D'autres start-up ont adopté une approche différente. C'est le cas de Phylex BioSciences, une biotech installée en Californie mais dont le patron, Pascal Brandys, est français, à l'instar de celui de Moderna. Ce dernier s'est associé à Jens Herold, un spécialiste des coronavirus, qui dirige l'unité biopharmaceutique Boehringer Ingelheim. Les deux hommes avaient déjà cofondé en 2003 une start-up pour développer un vaccin contre le SARS-CoV-1, mais dont les recherches n'avaient pas été menées à leur terme du fait de la disparition du virus. Les deux associés ont donc recréé une nouvelle société, en mars 2020, spécialement pour répondre à la pandémie de SARS-CoV-2.
Un vaccin universel est la seule réponse durable étant donné que les mutations vont s’accumuler au fil du temps
Comme les vaccins classiques, Phylex BioSciences utilise la protéine S du virus, mais uniquement sur sa partie stable. Une soixantaine de ces fragments sont ensuite assemblés sur une structure 3D imitant la protéine entière dans une particule pseudo-virale. « Les épitopes sont ainsi présentés aux anticorps dans la même configuration que la vraie protéine de pointe, explique Pascal Brandys. Nous avons environ un an de retard sur les vaccins comme Moderna », reconnaît le dirigeant, qui mise sur un essai clinique de phase 3 fin 2021. Mais son vaccin sera efficace sur tous les futurs variants. « Un vaccin universel basé sur les régions conservées du virus est la seule réponse durable de vaccination, étant donné que les mutations vont s'accumuler au fil du temps », assure-t-il. Phylex Bioscience a d'ores et déjà signé un partenariat avec la société californienne Atum pour la fabrication de son vaccin en grande quantité.
eTheRNA, un vaccin en spray nasal
Une autre biotech belge, eTheRNA, travaille sur un projet similaire à celui de Phylex Bioscience. Comme elle, elle utilise la partie conservée de la protéine de pointe, identique chez tous les coronavirus. Mais son vaccin serait commercialisé sous forme de spray nasal. « Cela présente l'avantage d'être facile à administrer. Et ne nécessite pas d'injection », explique Bernard Sagaert, directeur de production chez eTheRNA. Un laboratoire pharmaceutique chinois a récemment investi dans la société, ce qui devrait lui ouvrir le marché chinois et permettre une fabrication à grande échelle.
VBI Vaccines, un vaccin multipotent
Enfin, la société canadienne VBI Vaccines joue une carte encore différente, même si elle recourt comme Phylex à une particule pseudo-virale. La start-up conçoit un vaccin trivalent contre le SARS-CoV-1, le SARS-CoV-2 et le MERS, en multipliant les antigènes à la surface de son faux virus. Plutôt que de sélectionner la partie fixe, elle inclut donc le plus grand nombre possible d'antigènes connus. Rien ne permet cependant de dire que ce vaccin multiple répondra aux futures mutations.
Course de vitesse contre les mutants
Un vaccin universel contre le coronavirus a-t-il des chances de voir le jour rapidement ? Rien n'est moins sûr : les scientifiques s'échinent depuis des années à mettre au point un tel vaccin contre la grippe (qui doit aujourd'hui être renouvelé chaque année). Mais après tout, la pandémie a montré qu'il était possible de produire un vaccin entièrement nouveau en moins de neuf mois contre une dizaine d'années en temps normal. En attendant l'aboutissement de tous ces projets, Moderna assure qu'il est capable de fabriquer un nouveau vaccin en moins de six semaines, simplement en modifiant son code source. Mais cela suppose de relancer tout le processus de fabrication et de revacciner toutes les personnes ayant déjà reçu l'ancien vaccin. Une opération terriblement coûteuse.
source futura sciences.
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Publié le 22/07/2021
Recertification : ça commence aujourd’hui
Paris, le jeudi 22 juillet 2021 – Attendue ou plutôt crainte, la recertification dorénavant intitulé « certification périodique » est gravée dans le marbre par la publication d’une ordonnance au journal officiel.
6 professions concernées, une obligation même pour les anciens diplômés
Cette nouvelle obligation faite à 6 professions de santé (médecin, pharmacien, infirmier, sage-femme, kiné et pédicure-podologue) consiste en la réalisation d’un « programme d'actions » visant à actualiser les connaissances et compétences, renforcer la qualité des pratiques professionnelles, améliorer les relations avec les patients et mieux prendre en compte sa santé personnelle.
Tous ces professionnels, y compris ceux qui sont déjà diplômés, devront se soumettre à cette obligation. Une seule dérogation accordée à ceux qui sont déjà entrés dans la carrière : ils auront 9 ans pour réaliser leur premier programme de certification contre 6 pour ceux qui seront diplômés à partir du 1er janvier 2023.
En pratique, les actions prises en compte seront celles « réalisées au titre du développement professionnel continu, de la formation continue et de l'accréditation* ».
Une nouvelle institution
La certification sera chapeautée par une nouvelle instance : le «Conseil national de la certification périodique » chargé de définir « la stratégie, le déploiement et la promotion » ainsi que les orientations scientifiques de la certification périodique.
Il veillera également à ce que les « acteurs intervenant dans la procédure de certification périodique » soient indépendants de tout lien d'intérêt et à ce que la certification réponde aux critères d'objectivité des connaissances professionnelles, scientifiques et universitaires et aux règles déontologiques des professions concernées.
Chaque profession se verra déterminer une liste d’actions valables pour la recertification qui constituera le « référentiel de certification périodique ».
Notons que les actions de certification seront librement choisies par le professionnel de santé parmi le référentiel de certification périodique, le cas échéant en lien avec son employeur.
Ces référentiels seront élaborés par les conseils nationaux professionnels, sur la base d'une méthode arrêtée par le ministre chargé de la santé sur proposition de la Haute Autorité de santé et après avis du Conseil national de la certification périodique. Ces référentiels seront enfin approuvés par arrêté du ministre chargé de la santé, qui pourra saisir au préalable pour avis la Haute Autorité de santé.
Les actions réalisées par les professionnels de santé au titre de leur obligation de certification périodique seront retracées dans un compte individuel dont le contenu et les modalités d'utilisation et d'accès seront définis par décret en Conseil d’État. La gestion des comptes individuels sera assurée par une autorité administrative désignée par décret.
Des sanctions jusqu’à l’interdiction d’exercice
Il reviendra aux ordres professionnels de contrôler le respect par les professionnels de santé de leur obligation de certification périodique.
Or, le fait pour un professionnel de santé de ne pas satisfaire à cette obligation constituera une faute susceptible d'entraîner une sanction disciplinaire prononcée après une éventuelle « suspension temporaire d'exercice pour insuffisance professionnelle ». Une sanction qui pourra aller jusqu’à une suspension définitive d’exercice pour les professionnels les plus récalcitrants.
Prochaine étape : la publication des décrets mentionnés dans l’ordonnance, le détail des obligations qui incomberont aux organismes formateurs et la définition de la place d’instance déjà existante comme l’agence nationale du développement professionnel continu (ANDPC).
*L’accréditation ne concerne que certaines spécialités, notamment chirurgicales, exercées en établissement de santé.
F.H.
jim.fr
Recertification : ça commence aujourd’hui
Paris, le jeudi 22 juillet 2021 – Attendue ou plutôt crainte, la recertification dorénavant intitulé « certification périodique » est gravée dans le marbre par la publication d’une ordonnance au journal officiel.
6 professions concernées, une obligation même pour les anciens diplômés
Cette nouvelle obligation faite à 6 professions de santé (médecin, pharmacien, infirmier, sage-femme, kiné et pédicure-podologue) consiste en la réalisation d’un « programme d'actions » visant à actualiser les connaissances et compétences, renforcer la qualité des pratiques professionnelles, améliorer les relations avec les patients et mieux prendre en compte sa santé personnelle.
Tous ces professionnels, y compris ceux qui sont déjà diplômés, devront se soumettre à cette obligation. Une seule dérogation accordée à ceux qui sont déjà entrés dans la carrière : ils auront 9 ans pour réaliser leur premier programme de certification contre 6 pour ceux qui seront diplômés à partir du 1er janvier 2023.
En pratique, les actions prises en compte seront celles « réalisées au titre du développement professionnel continu, de la formation continue et de l'accréditation* ».
Une nouvelle institution
La certification sera chapeautée par une nouvelle instance : le «Conseil national de la certification périodique » chargé de définir « la stratégie, le déploiement et la promotion » ainsi que les orientations scientifiques de la certification périodique.
Il veillera également à ce que les « acteurs intervenant dans la procédure de certification périodique » soient indépendants de tout lien d'intérêt et à ce que la certification réponde aux critères d'objectivité des connaissances professionnelles, scientifiques et universitaires et aux règles déontologiques des professions concernées.
Chaque profession se verra déterminer une liste d’actions valables pour la recertification qui constituera le « référentiel de certification périodique ».
Notons que les actions de certification seront librement choisies par le professionnel de santé parmi le référentiel de certification périodique, le cas échéant en lien avec son employeur.
Ces référentiels seront élaborés par les conseils nationaux professionnels, sur la base d'une méthode arrêtée par le ministre chargé de la santé sur proposition de la Haute Autorité de santé et après avis du Conseil national de la certification périodique. Ces référentiels seront enfin approuvés par arrêté du ministre chargé de la santé, qui pourra saisir au préalable pour avis la Haute Autorité de santé.
Les actions réalisées par les professionnels de santé au titre de leur obligation de certification périodique seront retracées dans un compte individuel dont le contenu et les modalités d'utilisation et d'accès seront définis par décret en Conseil d’État. La gestion des comptes individuels sera assurée par une autorité administrative désignée par décret.
Des sanctions jusqu’à l’interdiction d’exercice
Il reviendra aux ordres professionnels de contrôler le respect par les professionnels de santé de leur obligation de certification périodique.
Or, le fait pour un professionnel de santé de ne pas satisfaire à cette obligation constituera une faute susceptible d'entraîner une sanction disciplinaire prononcée après une éventuelle « suspension temporaire d'exercice pour insuffisance professionnelle ». Une sanction qui pourra aller jusqu’à une suspension définitive d’exercice pour les professionnels les plus récalcitrants.
Prochaine étape : la publication des décrets mentionnés dans l’ordonnance, le détail des obligations qui incomberont aux organismes formateurs et la définition de la place d’instance déjà existante comme l’agence nationale du développement professionnel continu (ANDPC).
*L’accréditation ne concerne que certaines spécialités, notamment chirurgicales, exercées en établissement de santé.
F.H.
jim.fr
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Les chiffres clés quotidiens de l’épidémie COVID-19 en France
Le dernier tableau de bord publié par Santé publique France fait état de
6 398 983 cas confirmés d’infection par SARS-CoV-2 (dont 28 554 dans les 24 dernières heures).
Le taux de positivité des tests est de 4,1 %.
On a déploré 112 533 décès, dont 77 en 24 heures.
Au cours des sept derniers jours, 5 198 personnes ont été hospitalisées. 1 181 admissions en soins critiques, dont 869 en réanimation ont été par ailleurs recensées.
Un point de situation dans le monde
Selon les données de l'université John Hopkins de Baltimore, 205 611 601 infections par SARS-Cov-2 (vs 201 040 616 le 6/08) 4 270 895 décès liés à cette maladie. Les trois pays qui ont identifié et déclaré le plus de cas sont les États-Unis (36 306 963 vs 35 443 290), l’Inde (32 117 826 VS 31 856 757), le Brésil (20 285 067 vs 20 066 587). Les trois pays les plus endeuillés en valeur absolue sont les États-Unis (619 093 vs 615 341 décès), le Brésil (566 896 vs 560 706 décès) et l’Inde (430 254 vs 426 754 décès).
Le dernier tableau de bord publié par Santé publique France fait état de
6 398 983 cas confirmés d’infection par SARS-CoV-2 (dont 28 554 dans les 24 dernières heures).
Le taux de positivité des tests est de 4,1 %.
On a déploré 112 533 décès, dont 77 en 24 heures.
Au cours des sept derniers jours, 5 198 personnes ont été hospitalisées. 1 181 admissions en soins critiques, dont 869 en réanimation ont été par ailleurs recensées.
Un point de situation dans le monde
Selon les données de l'université John Hopkins de Baltimore, 205 611 601 infections par SARS-Cov-2 (vs 201 040 616 le 6/08) 4 270 895 décès liés à cette maladie. Les trois pays qui ont identifié et déclaré le plus de cas sont les États-Unis (36 306 963 vs 35 443 290), l’Inde (32 117 826 VS 31 856 757), le Brésil (20 285 067 vs 20 066 587). Les trois pays les plus endeuillés en valeur absolue sont les États-Unis (619 093 vs 615 341 décès), le Brésil (566 896 vs 560 706 décès) et l’Inde (430 254 vs 426 754 décès).
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
-
Arnaud BASSEZ
- Administrateur - Site Admin
- Messages : 2506
- Enregistré le : sam. nov. 04, 2006 4:43 pm
- Localisation : Paris
- Contact :
Re: Articles sur la santé
Publié le 24/08/2021
La HAS recommande un rappel vaccinal pour les plus de 65 ans
Paris, le mardi 24 août 2021 - À quoi sert la Haute autorité de Santé (HAS) ? À plusieurs reprises depuis le début de la pandémie de Covid, quelques esprits malins n’ont pu s’empêcher de se poser la question. Les autorités politiques ont en effet régulièrement devancé ses interventions, ne pouvant qu’influencer ses avis. Ainsi, concernant l’administration d’une vaccination de rappel contre la Covid aux personnes présentant un schéma vaccinal complet, afin de renforcer leur immunité vaccinale, amoindrie par le temps et face au variant Delta, un avis de la HAS était attendu cette semaine. Il a été effectivement publié aujourd’hui.
Cependant, dès dimanche et hier, le responsable du Conseil d’orientation de la stratégie vaccinale, Alain Fischer et le ministre de la Santé, Olivier Véran ont présenté les contours d’une campagne qui concernera tous les plus de 65 ans. Une préconisation qui va au-delà de ce que recommandait la HAS en juillet, qui suggérait de cibler les plus de 80 ans et les personnes immunodéprimées.
Tout est déjà décidé… mais la HAS arbitrera
Sans donc attendre le nouvel avis de la HAS, le ministre de la Santé, Olivier Véran, invité hier de BFM-TV a indiqué que la campagne de rappel vaccinal devrait être d’abord recommandée à toutes les personnes âgées de 65 ans et plus. Dores et déjà, il a « demandé à ses services de mettre en place le programme pour ceux et celles qui en relèvent ». De fait, il y a urgence, puisque l’opération pourrait débuter en septembre, a encore précisé Olivier Véran, alors que la veille, le docteur Alain Fischer avait avancé la date d’octobre. Le ministre a encore précisé qu’il « y aura un délai d’au moins six mois entre la deuxième et la troisième injection ».
Néanmoins, il a affirmé que l’ensemble des arbitrages (âge, délai, date, pertinence de la vaccination hétérologue…) appartenait à la HAS …et au président de la République !
Etudes observationnelles
L’arbitrage de la HAS a donc été publié ce matin et signale lui-même qu’il devra être complété par les recommandations de l’Agence européenne du médicament (EMA), puisque pour l’heure l’AMM des vaccins ne prévoit pas de rappel vaccinal. « Après avoir analysé les données disponibles, la HAS propose une dose de rappel avec un vaccin à ARNm pour les personnes de 65 ans et plus, ainsi que pour les personnes présentant des comorbidités qui augmentent le risque de formes graves de Covid-19. Cette dose de rappel doit être administrée après un délai d’au moins 6 mois suivant la primovaccination complète » écrit l’institution qui détaille : « En effet les études récentes suggèrent une réduction de l’efficacité de tous les vaccins, en particulier contre le variant delta. Cette baisse de la protection concerne essentiellement l’infection et les formes symptomatiques.
On observe également une légère baisse d’efficacité sur les formes graves qui restent globalement bien couvertes par les vaccins ». Néanmoins, la HAS reconnaît qu’il s’agit d’études observationnelles non exemptes de biais.
Nul besoin de préférer Moderna à Pfizer
Concernant les vaccins à utiliser, la HAS préconise une dose de rappel avec un vaccin à ARNm pour toutes les personnes primovaccinées avec Janssen (à partir de quatre semaines après l’injection).
Cependant, pour les personnes primovaccinées par les vaccins de Pfizer/BioNTech et Moderna, « la HAS estime qu’il n’y a pas d’argument suffisant, à ce jour, pour recommander préférentiellement un vaccin par rapport à l’autre pour la dose de rappel, les deux vaccins à ARNm disponibles (Comirnaty® et Spikevax®) étant tous les deux très efficaces contre les formes graves de Covid-19, y compris celles liées au variant Delta ».
Ainsi, l’institution ne voit pas dans les données récemment pré-publiées par la MayoClinic suggérant une plus grande efficacité de Moderna vis-à-vis du risque d’infection et de transmission du variant Delta, une raison de préférer ce vaccin. Cela peut s’expliquer par le fait que ces travaux sont encore préliminaires, tandis que la forte contagiosité du variant Delta rend en tout état de cause difficilement atteignable l’objectif d’immunité collective et invite donc à privilégier la protection individuelle contre les formes graves. En outre, pragmatiquement, on ne peut oublier que les moyens de production et les livraisons de Moderna sont plus restreints que ceux de Pfizer/BioNTech. Enfin, la HAS préconise que cette campagne de rappel vaccinal soit associée à la campagne de vaccination contre la grippe, afin de simplifier le parcours, puisque les sujets éligibles sont les mêmes, soit à une date un peu ultérieure de celle préconisée par le ministre de la Santé.
Vers une remise en question de l’avis à peine publié ?
Sans revenir sur les facteurs de décrédibilisation que comporte cet avis (en particulier sa publication en aval des annonces politiques), on relève que la HAS semble donc exclure que la campagne soit généralisée à toute la population. Cependant, on sait que la position des autorités pourrait rapidement évoluer (et que la HAS pourrait donc devoir reconsidérer son évaluation). D’abord, en raison de l’évolution constante des connaissances sur l’efficacité des vaccins et sur le virus. D’ailleurs la HAS remarque : « La baisse [de la protection NDLR] ne touche pas seulement les personnes âgées et les populations à risque de formes graves, mais ces dernières demeurent les plus affectées ».
Une Europe encore attentiste
Surtout, il n’est pas impossible que les exemples étrangers conduisent rapidement la France à repenser sa campagne de rappel vaccinal. En Israël, en effet, la « troisième dose » concerne désormais tous les plus de 40 ans, tandis que l’ensemble de la population sera visé par une recommandation de rappel vaccinal aux États-Unis. De la même manière, une campagne généralisée mais échelonnée se prépare en Grande-Bretagne.
Cependant, pour l’heure, dans la majorité des autres pays, les autorités politiques et scientifiques considèrent que les données sont encore trop restreintes pour pouvoir se prononcer.
Beaucoup de pays ont donc ainsi choisi de s’en remettre à l’avis de l’Agence européenne du médicament qui est attendu dans les semaines qui viennent. C’est le cas par exemple de l’Espagne, du Portugal ou de la Bulgarie. D’autres s’en tiennent enfin à des préconisations qui ne visent que les plus âgés et les personnes immunodéprimées (tel l’Italie ou l’Allemagne).
Considérations éthiques ?
La diversité des positions et l’attentisme de certains états s’expliquent tant par des raisons médicales et scientifiques qu’éthiques. La question de l’utilité de la troisième dose, qui plus est en population générale, reste en effet discutée, d’autant plus que les informations en vie réelle pour évaluer l’évolution de la réponse immunitaire des personnes vaccinées font souvent défaut. Par ailleurs, beaucoup sont sensibles aux vives critiques émises par l’Organisation mondiale de la Santé, que cette dernière a encore répétées récemment peu après l’annonce par les États-Unis de leur programme de rappel vaccinal. « Nous pensons clairement que les données actuelles n'indiquent pas que les rappels sont nécessaires » a ainsi martelé la scientifique en chef de l’OMS Soumya Swaminathan. De son côté, le conseiller du directeur général de l’agence, Bruce Aylward a déploré : « Il y a suffisamment de vaccins dans le monde mais ils ne vont pas aux bons endroits, dans le bon ordre ».
Léa Crébat
jim.fr
La HAS recommande un rappel vaccinal pour les plus de 65 ans
Paris, le mardi 24 août 2021 - À quoi sert la Haute autorité de Santé (HAS) ? À plusieurs reprises depuis le début de la pandémie de Covid, quelques esprits malins n’ont pu s’empêcher de se poser la question. Les autorités politiques ont en effet régulièrement devancé ses interventions, ne pouvant qu’influencer ses avis. Ainsi, concernant l’administration d’une vaccination de rappel contre la Covid aux personnes présentant un schéma vaccinal complet, afin de renforcer leur immunité vaccinale, amoindrie par le temps et face au variant Delta, un avis de la HAS était attendu cette semaine. Il a été effectivement publié aujourd’hui.
Cependant, dès dimanche et hier, le responsable du Conseil d’orientation de la stratégie vaccinale, Alain Fischer et le ministre de la Santé, Olivier Véran ont présenté les contours d’une campagne qui concernera tous les plus de 65 ans. Une préconisation qui va au-delà de ce que recommandait la HAS en juillet, qui suggérait de cibler les plus de 80 ans et les personnes immunodéprimées.
Tout est déjà décidé… mais la HAS arbitrera
Sans donc attendre le nouvel avis de la HAS, le ministre de la Santé, Olivier Véran, invité hier de BFM-TV a indiqué que la campagne de rappel vaccinal devrait être d’abord recommandée à toutes les personnes âgées de 65 ans et plus. Dores et déjà, il a « demandé à ses services de mettre en place le programme pour ceux et celles qui en relèvent ». De fait, il y a urgence, puisque l’opération pourrait débuter en septembre, a encore précisé Olivier Véran, alors que la veille, le docteur Alain Fischer avait avancé la date d’octobre. Le ministre a encore précisé qu’il « y aura un délai d’au moins six mois entre la deuxième et la troisième injection ».
Néanmoins, il a affirmé que l’ensemble des arbitrages (âge, délai, date, pertinence de la vaccination hétérologue…) appartenait à la HAS …et au président de la République !
Etudes observationnelles
L’arbitrage de la HAS a donc été publié ce matin et signale lui-même qu’il devra être complété par les recommandations de l’Agence européenne du médicament (EMA), puisque pour l’heure l’AMM des vaccins ne prévoit pas de rappel vaccinal. « Après avoir analysé les données disponibles, la HAS propose une dose de rappel avec un vaccin à ARNm pour les personnes de 65 ans et plus, ainsi que pour les personnes présentant des comorbidités qui augmentent le risque de formes graves de Covid-19. Cette dose de rappel doit être administrée après un délai d’au moins 6 mois suivant la primovaccination complète » écrit l’institution qui détaille : « En effet les études récentes suggèrent une réduction de l’efficacité de tous les vaccins, en particulier contre le variant delta. Cette baisse de la protection concerne essentiellement l’infection et les formes symptomatiques.
On observe également une légère baisse d’efficacité sur les formes graves qui restent globalement bien couvertes par les vaccins ». Néanmoins, la HAS reconnaît qu’il s’agit d’études observationnelles non exemptes de biais.
Nul besoin de préférer Moderna à Pfizer
Concernant les vaccins à utiliser, la HAS préconise une dose de rappel avec un vaccin à ARNm pour toutes les personnes primovaccinées avec Janssen (à partir de quatre semaines après l’injection).
Cependant, pour les personnes primovaccinées par les vaccins de Pfizer/BioNTech et Moderna, « la HAS estime qu’il n’y a pas d’argument suffisant, à ce jour, pour recommander préférentiellement un vaccin par rapport à l’autre pour la dose de rappel, les deux vaccins à ARNm disponibles (Comirnaty® et Spikevax®) étant tous les deux très efficaces contre les formes graves de Covid-19, y compris celles liées au variant Delta ».
Ainsi, l’institution ne voit pas dans les données récemment pré-publiées par la MayoClinic suggérant une plus grande efficacité de Moderna vis-à-vis du risque d’infection et de transmission du variant Delta, une raison de préférer ce vaccin. Cela peut s’expliquer par le fait que ces travaux sont encore préliminaires, tandis que la forte contagiosité du variant Delta rend en tout état de cause difficilement atteignable l’objectif d’immunité collective et invite donc à privilégier la protection individuelle contre les formes graves. En outre, pragmatiquement, on ne peut oublier que les moyens de production et les livraisons de Moderna sont plus restreints que ceux de Pfizer/BioNTech. Enfin, la HAS préconise que cette campagne de rappel vaccinal soit associée à la campagne de vaccination contre la grippe, afin de simplifier le parcours, puisque les sujets éligibles sont les mêmes, soit à une date un peu ultérieure de celle préconisée par le ministre de la Santé.
Vers une remise en question de l’avis à peine publié ?
Sans revenir sur les facteurs de décrédibilisation que comporte cet avis (en particulier sa publication en aval des annonces politiques), on relève que la HAS semble donc exclure que la campagne soit généralisée à toute la population. Cependant, on sait que la position des autorités pourrait rapidement évoluer (et que la HAS pourrait donc devoir reconsidérer son évaluation). D’abord, en raison de l’évolution constante des connaissances sur l’efficacité des vaccins et sur le virus. D’ailleurs la HAS remarque : « La baisse [de la protection NDLR] ne touche pas seulement les personnes âgées et les populations à risque de formes graves, mais ces dernières demeurent les plus affectées ».
Une Europe encore attentiste
Surtout, il n’est pas impossible que les exemples étrangers conduisent rapidement la France à repenser sa campagne de rappel vaccinal. En Israël, en effet, la « troisième dose » concerne désormais tous les plus de 40 ans, tandis que l’ensemble de la population sera visé par une recommandation de rappel vaccinal aux États-Unis. De la même manière, une campagne généralisée mais échelonnée se prépare en Grande-Bretagne.
Cependant, pour l’heure, dans la majorité des autres pays, les autorités politiques et scientifiques considèrent que les données sont encore trop restreintes pour pouvoir se prononcer.
Beaucoup de pays ont donc ainsi choisi de s’en remettre à l’avis de l’Agence européenne du médicament qui est attendu dans les semaines qui viennent. C’est le cas par exemple de l’Espagne, du Portugal ou de la Bulgarie. D’autres s’en tiennent enfin à des préconisations qui ne visent que les plus âgés et les personnes immunodéprimées (tel l’Italie ou l’Allemagne).
Considérations éthiques ?
La diversité des positions et l’attentisme de certains états s’expliquent tant par des raisons médicales et scientifiques qu’éthiques. La question de l’utilité de la troisième dose, qui plus est en population générale, reste en effet discutée, d’autant plus que les informations en vie réelle pour évaluer l’évolution de la réponse immunitaire des personnes vaccinées font souvent défaut. Par ailleurs, beaucoup sont sensibles aux vives critiques émises par l’Organisation mondiale de la Santé, que cette dernière a encore répétées récemment peu après l’annonce par les États-Unis de leur programme de rappel vaccinal. « Nous pensons clairement que les données actuelles n'indiquent pas que les rappels sont nécessaires » a ainsi martelé la scientifique en chef de l’OMS Soumya Swaminathan. De son côté, le conseiller du directeur général de l’agence, Bruce Aylward a déploré : « Il y a suffisamment de vaccins dans le monde mais ils ne vont pas aux bons endroits, dans le bon ordre ».
Léa Crébat
jim.fr
La santé est un état précaire qui ne laisse augurer rien de bon.
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
https://www.facebook.com/SOFIA-soci%C3% ... _todo_tour
https://mobile.twitter.com/SOFIA_iade
