par Anna Froger, Arnaud Bassez
Connaître son ignorance est la meilleure part de la connaissance.
Proverbe chinois
— -

à lire en complément
- Docs en stock 2 Anesthésie-Cardiologie-Femme enceinte-Médicaments-Pédiatrie-Respiration-Samu-Système nerveux central-Traumatologie
- Docs en stock 3 SFAR 2009 et 2010
- Docs en stock 4 SFMU 2009
- Docs en stock 5 Physiologie de la plaque motrice-Les canaux ioniques-Le système endocrinien- Anatomie physiologie de l’appareil cardiovasculaire-Éléments de base pour la pharmacologie-Phase per et post opératoire
- Docs en stock 6 SFAR 2011
- Docs en stock 7 SFAR 2012
- Docs en stock 8 SFMU 2010-2011-2012
- Docs en stock 9 MAPAR 2008 ->2018
- Docs en stock 10 ICAR 1994 -> de nos jours
- Docs en stock 11 SFAR 2013
- Docs en stock 12 Asspro 2011 à 2018
- Docs en stock 13 SFAR 2014
- Docs en stock 14 Le préhospitalier
- Docs en stock 15 Médecine militaire
- Docs en stock 16 Agora 2010-2011-2012-2013
- Docs en stock 17 SFAR 2015
- Résumé du MAPAR 2014
- Docs en stock 18 JLAR 1997 à 2016
- Docs en stock 19 SFAR 2016
- Docs en stock 20 Caen 2013 à 2016
- Docs en stock 21 SFAR 2017 IADE-IDE de réanimation et urgences & congrès de l’ALIADE 2008->2017
- Docs en stock 22 SFAR 2018
- Docs en stock 23 SFAR 2019
- Docs en stock 24 Médecine des forces spéciales 2022
Soit plus de 2525 documents en téléchargement, incluant cet article.
A lire aussi compil utile (on n’en sait jamais assez)
– AFISAR 2013 et 2014, les publications
Et les nouveautés dans les produits, matériels vus sur le congrès 2013.
Sans oublier la rubrique Olympiade
– Sécurité : sanitaire, incendie, fluides médicaux, médicaments, solutions hydro alcoolique
§§§
Voici quelques documents que je vous propose, ils ne sont que le reflet d’une formation, mais peuvent apporter des informations sur divers sujets de notre métier.
Les sujets sont donc variés, mais toujours en relation avec le rôle IADE.
La plupart sont de moi, mais quelques uns m’ont été donnés par des médecins (vous retrouverez leurs nom dans le document).
– Médicament cardio actif (pps)
– Médicament en cardiologie (doc)
– Picco (pps)
– Swan ganz 2006 (pps)
– Traitement de l’embolie pulmonaire (doc)
– « anesthésie du brûlé et suite (pps) d’après les cours papiers du Dc Gartner du CHU de Montpellier.
– pédiatrie : physio, urgence ...
– neuro (pps, doc)
– état de choc
– intoxication médicamenteuse
– Réveil
– Dialyse
– BMR
– Hypoxies
– Surveillance et sevrage ventilation...
Anna Froger.
IADE
ps : Je mets en ligne les documents fournis par Anna, au fur et à mesure de leur réception.
Cet article ne comporte pas tous les documents cités.
Il s’enrichira donc progressivement, au rythme des envois.
Anna reconnait avoir l’autorisation de l’auteur, pour diffuser librement ses travaux, et dégage la responsabilité de l’administrateur.
Si l’auteur, toutefois, souhaite voir ses travaux retirés du site, merci de me contacter par mail sofianesth chez gmail.com.
— -
J’enrichi la base de données ci-dessus, par les référentiels de la société française d’études et de traitement des brûlés. (AB)
Référentiels et Fiches de recommandations SFETB (1)
1. TRAITEMENT LOCAL DES BRULURES SUIVIES EN CONSULTATION EXTERNE
OU EN VILLE (fiche de recommandation SFETB - 2005 -)
A - RAPPEL :
Le risque principal de ce type de brûlures est l’aggravation des lésions par infections susceptibles d’entraîner la formation de séquelles indues.
B - LES PRODUITS UTILISABLES :
Catégorie A : les pommades ou crèmes sans antibactérien
Elles ont comme objectifs de calmer et de "favoriser" la cicatrisation :
ex : Biafine, pommades à la vitamine A…..
Catégorie B : Les pansements membranes sans antibactérien (associés ou non à des moyens de contention)
- Ils couvrent la brûlure, la protègent, absorbent éventuellement les exsudats et maintiennent un milieu humide, favorable à la cicatrisation.
- Plusieurs sous-catégories : hydrocolloïdes, hydrocellulaires, membranes plus ou moins perméables, Alginates etc..
Catégorie C : les interfaces sans antibactérien
- Ils doivent être associés à un pansement secondaire absorbant (compresses) et à des moyens de contention.
- Ils évitent la macération et drainent les exsudats.
- Ex : tulles vaselinés, avec ou sans additifs, tulles siliconés, tulles avec hydrocolloïdes.
Catégorie D : les pansements avec produits antibactériens
Ils ont une action préventive et, éventuellement, curative sur l’infection des brûlures.
2 sous-catégories :
- Catégorie D1 : Crèmes ou pommades (Flammazine , Sicazine , Ialuset + , crème à la Bétadine , Sulfamylon …)
- Catégorie D2 : Pansements imprégnés d’antiseptiques (Urgotulle SAg , Ialuset + compresses , Acticoat, Aquacel Ag…)
NB : le tulle bétadiné et l’Antibiotulle ne doivent pas être classés dans la catégorie D car insuffisamment imprégnés et donc, peu ou pas efficaces. Le Corticotulle possède une action anti-inflammatoire puissante et ne doit être utilisé que pour cette indication (fin de cicatrisation d’une lésion hypertrophique et/ou inflammatoire).
C - RECOMMANDATIONS S.F.E.T.B
TOUTE BRULURE DU 2EME OU DU 3EME DEGRE DOIT ETRE MEDICALEMENT SURVEILLEE A LA RECHERCHE DE SIGNES D’INFECTION.
TOUTE BRULURE QUI, APRES 10 JOURS D’EVOLUTION, NE PRESENTE PAS DE SIGNES PATIENTS DE CICATRISATION DOIT ETRE EVALUEE PAR UN BRULOLOGUE.
Brûlure du 1er degré (rougeur cutanée sans phlyctène)
pansement catégorie A (pommade ou crème non antiseptique).
Brûlure du 2ème degré (présence de phlyctènes, exposition, après excision des phlyctènes, du derme superficiel ou profond)
Brûlures superficielles et, à priori, propres :
- Catégorie C (interface)
- Catégorie B (membranes sans antibactérien avec surveillance étroite)
- Catégorie D (D1 ou D2 : pommades ou pansements + antibactériens) si doute sur l’hygiène, zones très algiques, (faces palmaires des mains ou plantaires des pieds), ou si brûlures étendues.
- JAMAIS de pansement de catégorie A (risques d’infection).
Brûlures profondes ou brûlures superficielles à priori contaminées ou infectées :
TOUJOURS catégorie D
brûlures du 3ème degré justifient toujours d’un avis spécialisé pour traitement chirurgical.
Référentiels et Fiches de recommandations SFETB (2)
2. COMPRESSION DES BRULURES (fiche de recommandations SFETB 2006)
A - Rappels
Pour rétablir l’apoptose des myofibroblastes, cellules dermiques, dont l’inhibition est responsable des complications cicatricielles des brûlures, il faut appliquer une hypoxie locale.
Cette hypoxie est obtenue par l’application sur la cicatrice d’une pression au minimum de 10 hPa.
En pratique, il faut appliquer cette pression par des matériaux en tissu souple et élastique sur la plupart des cicatrices ou des matériaux rigides en thermoplastique.
Les vêtements compressifs industriels, matériaux en tissu élastique, sont inscrits dans la Liste des Prestations et Produits Remboursables. Les thermoplastiques, bien que sur empreinte et sur mesure, ne donnent pas lieu à une prise en charge par les organismes sociaux.
B - Vêtements compressifs sur mesure pour grands brûlés
Définition :
Les vêtements compressifs pour grands brûlés sont destinés à éviter l’apparition de cicatrices hypertrophiques ou rétractiles ou en améliorer l’aspect. Seuls les vêtements compressifs exécutés sur mesure donnent lieu à prise en charge.
Indications :
Le vêtement compressif doit être appliqué après l’épithélialisation d’une plaie de deuxième degré profond, et de troisième degré, sur un épiderme solide, c’est à dire entre quinze jours et trois semaines après l’épithélialisation.
La durée du port est, quotidiennement, de 23 h / 24 et ceci jusqu’à la maturation cicatricielle, autrement dit, jusqu’à la fin de l’inflammation locale, entre 9 et 18 mois selon les individus.
Pour déterminer le moment de la suppression du vêtement, le test de la vitropression ou une pression digitale de l’examinateur sur la cicatrice peut être appliqué : la recoloration des téguments en plus de trois secondes signe la maturation cicatricielle.
Les complications iatrogènes et l’intolérance du vêtement :
– lésions du nouvel épiderme : phlyctène et/ou plaie, si le vêtement compressif est mis en place trop tôt et avec difficultés.
– œdème en amont si la pression du vêtement est trop importante au niveau d’un membre.
– douleur et/ou plaies au niveau des plis de flexion (creux axillaire, coude, poignet, cou de pied).
– douleur par la fermeture à glissière placée sur une cicatrice.
– réaction allergique au tissu synthétique.
– difficulté de mise en place de la fermeture à glissière du gilet (personne âgée, main brûlée).
– difficulté, voire impossibilité, de mise en place de la chaussette quand elle est solidaire d’une jambe longue ou du gant solidaire d’une manche longue.
– intolérance psychologique devant le regard des autres (cagoule, gants, mentonnière).
– intolérance nocturne et l’été en raison de la chaleur ambiante.
Généralités :
- 1. La fourniture des vêtements compressifs est assurée par des professionnels agréés dans les conditions prévues par la réglementation ou, à titre dérogatoire, par des fabriquants dont les vêtements sont conformes aux spécifications techniques dans le cadre de consultations de services spécialisés pour le traitement des grands brûlés ou de centres de rééducation fonctionnelle.
- 2. Le délai de livraison et de réparation des vêtements ne peut excéder dix jours à compter de la réception de la commande par le fournisseur.
- 3. La garantie (fournitures et main d’œuvre) relative à la fabrication, à la finition et à la qualité s’étend sur une période de six mois à compter de la date de livraison.
Nomenclature et tarifs :
Ces vêtements sont pris en charge pour les brûlures étendues, du deuxième degré profond et du troisième degré, lorsque la surface totale est supérieure à 10% de la surface corporelle ou lorsque la lésion siège sur les mains, le visage, le cou ou les plis de flexion.
Leur prise en charge est assurée à raison d’un jeu de deux vêtements par malade, par période de 6 mois, renouvelable trois fois.
Toutefois, dans les deux cas suivants :
– pour les enfants de moins de 16 ans quelle que soit la localisation,
– et pour les brûlures des mains quel que soit l’âge du patient.
Leur prise en charge est assurée à raison d’un jeu de deux vêtements par malade, par période de 3 mois.
La nomenclature comporte deux rubriques :
1. Les vêtements compressifs : le gilet sans manche, le short, la mitaine, le gant, la chaussette haute, la cagoule, la mentonnière et le collier.
2. Les suppléments ou adjonctions aux vêtements compressifs : la manche courte, la manche longue, la patte sous-cuisse, la confection poitrine, la jambe courte, la jambe longue, le pied, la manchette (pour mitaine ou gant), le séparateur digital et le conformateur sternal.
Chaque vêtement ou supplément est assorti d’un numéro de code correspondant à un tarif en euros.
Les prescriptions médicales doivent obligatoirement respecter la nomenclature pour donner lieu à remboursement. Les prescriptions fantaisistes, telles que tee-shirt, pantalon, panty, bermuda ou caleçon ne donnent pas lieu à remboursement.
Les vêtements compressifs pour grand brûlé sont du "petit appareillage" et donc remboursés à 65% si le patient ne bénéficie pas de l’exonération du ticket modérateur.
Exemple d’ordonnance :
Pour une patiente brûlée (2ème degré profond et 3ème) au niveau du dos, du membre supérieur gauche dont la main, avec prise de greffe sur la cuisse gauche :
(en rédigeant cette prescription ainsi, le gant n’est pas solidaire de la manche longue du gilet).
Mme " X " ALD (ou non)
– un gilet, une manche courte à droite et une manche longue à gauche.
– une confection poitrine.
– un gant bouts ouverts et une manchette à gauche.
– un short et une jambe courte à gauche.
En double exemplaire
3. Premiers secours (SFETB 1992)

A - Vérification et contrôle des fonctions vitales
- Respiratoire
– assurer la liberté des voies aériennes
– oxygénothérapie au masque
– évaluation du risque de lésions respiratoires (voir chapitre 4)
- Hémodynamique - choc
– traiter immédiatement l’hypovolémie des brûlés graves (voir chapitre 4)
– Les brûlures ne saignent jamais, penser aux lésions associées (hémorragie interne).
- Neurologiques
– La brûlure seule n’altère pas la conscience.
- Température centrale
B - Recherche des lésions associées
Un hématocrite normal ou bas chez le brûlé est suspect.
C - Premiers soins locaux
Enlever les vêtements
Refroidir la brûlure
– immédiatement
– Eau du robinet, température 8° à 25°C pendant au moins cinq minutes.
– sauf si état de choc ou hypothermie ou brûlure depuis plus d’une heure
– Le refroidissement par l’eau diminue la douleur et la profondeur de la brûlure.
– Il peut être poursuivi tant que la brûlure est douloureuse et doit être interrompu en cas
de sensation de froid, surtout chez l’enfant.
Protéger et réchauffer le brûlé
– draps stériles, draps propres, couverture de survie.
4. Estimation de la gravité de la brûlure : surface et profondeur de la brûlure
(SFETB 1992 et 2006)
5. Traitement des brûlures bénignes (SFETB 1992)
A- Traiter la douleur
B- Traitement local
Excisions des phlyctènes
Pansement
- antiseptique non alcoolisé
- Pansement gras ou substitut cutané
- Pas de colorant
- Pansement non compressif
- Doigts et orteils séparés
- Le pansement sera contrôlé et renouvelé tous les 2 jours
Avis spécialisé
6. Traitement des brûlures graves (SFETB 2006)
Tout brûlé grave doit être pris en charge en centre spécialisé. Les soins de réanimation sont débutés dès l’étape pré-hospitalière. Ils sont poursuivis au cours de l’hospitalisation initiale, des éventuels transports inter-hospitaliers, puis dans l’unité de réanimation spécialisée. Ils ne doivent pas interférer avec la réalisation du bilan traumatique initial, et avec les éventuelles interventions chirurgicales d’urgence.
A - Réanimation hydroélectrolytique
Toute brûlure de plus de 10% de la surface corporelle doit être perfusée immédiatement.
Protocoles de remplissage (fiche de recommandation SFETB 2006) :
Chez l’adulte
- L’apport hydroélectrolytique, reconnu comme indispensable, doit être précoce et adapté.
- Il n’y a pas consensus vis-à-vis de la composition qualitative et quantitative des apports.
- La supériorité d’une formule de remplissage vasculaire sur les autres n’est pas établie.
Deux grandes options peuvent être proposées :
– apport exclusif en cristalloïdes, par exemple règle du Parkland Hospital : apport de 4 ml/kg/% surface corporelle brûlée de ringer lactate, la moitié en 8 heures, l’autre moitié sur les 16 heures suivantes.
– apport intégrant des colloïdes, par exemple règle d’Evans : apport de 1 ml/kg/% surface corporelle brûlée de sérum salé isotonique, plus 1 ml /kg/% de surface corporelle brûlée de colloïdes, plus 2000 ml de sérum glucosé isotonique le premier jour. Il est classiquement admis que les apports du 2ème jour correspondent à la moitié de ceux apportés le 1er jour. Quelque soit la composition retenue, il y a accord pour considérer ces formules comme un schéma indicatif initial qui doit être réévalué et amendé selon les objectifs thérapeutiques cliniques et/ou biologiques retenus.
Leur liste est non exhaustive mais peut comprendre :
- • une diurèse de 0,5 à 1,5 ml/kg/heure (+++)
- • une pression artérielle moyenne supérieure à 70 mm de mercure
- • une optimisation du débit cardiaque, de la précharge du ventricule gauche, du transport et de la consommation d’oxygène, du volume d’eau extra-vasculaire intra-pulmonaire.L’objectif de cette réanimation hydroélectrolytique est de prévenir un défaut de remplissage vasculaire (responsable d’un état de choc, d’une insuffisance rénale aiguë, de défaillances des circulations régionales) comme un excès de remplissage (responsable d’une aggravation des oedèmes, d’une altération de l’hématose pulmonaire, d’une augmentation de la pression intra-abdominale).
- Chez l’enfant (SFETB 1992)
- de nombreux protocoles sont utilisés voici l’exemple du protocole de Carvajal :
- • 5000 ml/m² surface brûlée/24h de ringer lactate
- • + 2000 ml/m² surface corporelle de besoins de base (serum glucosé à 5%)
- • la moitié pendant les 8 premières heures suivant la brûlure
- • l’autre moitié dans les 16 heures suivantes
- • objectif = maintenir une diurèse supérieure ou égale à 0,5 ml/kg/h et un hématocrite <50% ainsi qu’une fréquence cardiaque <140 et une PA systolique >100 mmHg
fichier excel pour programmer le remplissage.
B - Réanimation respiratoire
La dette d’oxygène est constante. L’oxygénothérapie est toujours recommandée.
L’indication d’intubation trachéale et de mise sous ventilation assistée doit être discutée en cas de :
- • détresse respiratoire avérée,
- • brûlure grave de la tête et du cou,
- • brûlures très étendues (> 50 % surface corporelle brûlée).
- • troubles de conscience.
C - Analgésie
Les antalgiques de niveau 1 et 2 de la classification de l’OMS employés seuls sont inefficaces.
Morphiniques et morphinomimétiques doivent être prescrits selon titration, évaluation de l’efficacité, et sous surveillance des effets secondaires.
D - Traitements associés
- • L’équilibre thermique doit être maintenu.
- • La nutrition entérale précoce prévient l’ulcère de stress, maintient l’intégrité de la muqueuse digestive, préserve le rôle immunomodulateur de l’intestin.
- • La supplémentation précoce en vitamines et éléments traces anti-oxydants vise à contrôler le stress oxydatif.
- • Les anticoagulants à posologies préventives sont prescrits lorsque l’hypocoagulabilité initiale est amendée.
- • La vaccination anti-tétanique est vérifiée, et mise à jour le cas échéant.
- • Les éventuelles intoxications associées, oxycarbonée et cyanhydrique notamment, doivent être dépistées et traitées.
- • Il n’y a pas d’indication d’antibiothérapie systématique à visée préventive.
E - Soins locaux (SFETB 1992)
Ne constituent pas une priorité et ne doivent être entrepris qu’une fois les perturbations générales contrôlées.
Si transfert immédiat vers le centre de brûlés >> champs stériles et couverture de survie
Si transfert différé >> désinfection et pansement
Les BRULURES PROFONDES CIRCONFERENTIELLES des membres peuvent nécessiter des INCISIONS DE DECHARGE jusqu’au tissu sain en respectant les trajets vasculo-nerveux et les plis de flexion.
7. Cas particuliers (recommandations SFETB 1992)
A - Brûlures électriques
- . La majorité des lésions est invisible
- . Le risque immédiat est : musculaire, cardiaque (ECG), rénal (hyperkaliémie, myoglobinurie), neurologique.
- . En cas de myoglobinurie :
- Alcaliniser le patient (soluté bicarbonaté isotonique)
- Assurer une diurèse de 2 ml/kg/h
- . Souvent, nécessité d’une exploration chirurgicale précoce.
A - Brûlures chimiques
Lavage prolongé à grande eau (30 minutes)
- . Pas de neutralisation sauf amphotères
- . Cas particulier : lésions par acide fluorhydrique
Toujours très profondes et douloureuses
Risque létal par hypocalcémie si brûlures de plus de 2% de la surface corporelle
Traitement spécifique local :
- Gluconate de calcium 10% sous cutané (0,5 ml/cm² SB)
- Gel de gluconate de calcium à 2,5%
C - Brûlures par produits adhérents (goudron, cire...)
Ne pas chercher à enlever les produits adhérents
8. Critères d’infection chez le brulé (SFETB 2006)
A - Définitions générales :
Pas de valeur prédictive d’infection :
Critères de SIRS (syndrome inflammatoire à réponse systémique) : au moins 2 critères présents sur les 4 ci-dessous.
– T°C > 38,5°C ou < 36°C
– FC > 90/mn
– FR > 20/mn ou capnie < 25 mmHg
– Leucocytes > 12 G ou < 4 G ou > 10 %de formes immatures.
Toute Brûlure > 20 % de la SCT et/ou toute brûlure avec lésion d’inhalation de fumée est susceptible de présenter les critères de SIRS en dehors de tout processus infectieux.
Valeurs prédictives d’infection :
SIRS d’apparition, d’évolution ou avec associations non justifiées par la brûlure
– Apparition des critères de SIRS chez un patient dont les lésions sont < 15 ou 20 % de la SCT et n’ayant pas de lésions d’inhalation de fumées.
– Présence d’au moins 2 des 4 critères ci-dessous chez un patient porteur d’une
Brûlure > 20 % de la SCT et/ou de lésions d’inhalation de fumée :
– T°C > 39, 5°C ou < 35,5°C
– augmentation de 50 % FC basale
– augmentation de 50 % FR basale
– augmentation de ou diminution de 100 % du nombre de leucocytes
– Défaillance hémodynamique nécessitant l’instauration ou l’augmentation des posologies d’un traitement par les catécholamines
B - Définitions des criteres d’infection des brulures :
Le diagnostic d’une infection cutanée est clinique
Infection cutanée bactérienne : signes locaux positifs
• Présence d’une réaction infl ammatoire locale ou loco-régionale
et/ou
• Une évolution locale défavorable et inattendue
– Au niveau des brûlures
– Présence de pus
– Détersion et séparation rapides
– Apparition de tâches noirâtres (nécrose ouhémorragie)
– Conversion inexpliquée d’une lésionsuperficielle en profonde (> 48e heure)
– Au niveau des prises de greffe
– Présence de pus
– Retard de cicatrisation inexpliqué
– Escarre
– Au niveau des greffes
– Présence de pus
– Lyse des greffes
– Nécrose de la graisse située sous la greffe
– Au niveau des zones cicatrisées
– Impétigo
– Lyse des zones guéries
Prélévements bactériologiques cutanés
Ils sont destinés à connaître le(s) germe(s) en cause
- • Le plus souvent un simple écouvillonnage suffit
- • La biopsie n’est jamais systématique, dans les cas diffi ciles une biopsie peut être réalisée ; on peut alors faire :
- - Un examen microbiologique
- - Apposition d’une empreinte sur lame avec coloration et mesure semi-quantitative des germes
- - Quantifi cation des germes présents par gramme de tissu après broyat : seuil de 105 CFU/g retenu comme significatif du risque de dissémination hématogène
- - Un examen anatomopathologiqueextemporané après congélation permettant d’apprécier la notion d’invasivité
- - Colonisation : germes dans les tissus non vascularisés
- - Infection : germes dans les tissus vivants et au contact des vaisseaux
L’infection cutanée accompagnée de signes généraux est une infection systémique d’origine cutanée.
Infection cutanée fungique :
La diagnostic peut être confirmé par biopsie
Infection cutanée herpétique :
Le diagnostic est clinique et peut être confirmé par la survenue d’une conversion sérologique et la présence de virus dans les prélèvements locaux
C - Définitions des criteres d’infection pour les autres sites :
Les définitions par sites (ci-dessous) sont issues de celles retenues par les C.CLIN pour les enquêtes du réseau de surveillance REA-REACAT /RAISIN 2006.
Ces définitions sont reprises dans " le guide de définition des infections nosocomiales " du C.CLIN Paris-Nord (1995), elles mêmes adaptées des définitions des CDC de 1988 (CDC definitions for nosocomial infections, Gardner JS, Jarvis WR, Emori TG et al., Am J Infect Control 1988 ; 16 : 128-40.) et du CSHPF de 1992 (100 recommandations pour la surveillance et la prévention des infections, BEH juin 1992).
Infection Pulmonaire : Pneumopathie
signes généraux + signes spécifiques d’organe ± critères microbiologiques :
• Deux clichés radiographiques au moins, avec une nouvelle image évocatrice de pneumopathie ou la modification d’une image précédente
• Et au moins un des signes suivants ou deux en l’absence de critères microbiologiques :
– Apparition de secretions purulentes ou modifi cation des caracteristiques (couleur, odeur, consistance, quantite)
– Dyspnee, tachypnee ou toux (si non ventile)
– Hypoxemie d’apparition ou d’aggravation recente
• ± Diagnostic microbiologique (un des criteres suivants) :
– LBA avec seuil de 104 CFU/ml ou au moins 5 % de cellules avec inclusion bacteriennes au direct
– Brosse de Wimberley avec seuil de 103 CFU/ml
– PDP avec seuil de 103 CFU/ml
– Aspiration bronchique quantitative avec seuil de 106 CFU/ml
– Hemoculture ou prelevement de tissu bronchique (histologie) ou de liquide pleural positif en l’absence d’autre source infectieuse
– Examens specifi ques pour les pneumopathies virales ou dues a des micro-organismes particuliers (Ag ou Ac dans les secretions bronchiques, examens directs ou cultures positives des secretions bronchiques, antigenes urinaires ou conversions serologiques)
Bronchite :
signes généraux, toux, modification récente des expectorations ou aspirations bronchiques, râles bronchiques ET isolement de germe(s) dans les aspirations bronchiques ET absence de foyer radiologique
Bactériémie :
Signes généraux + hémoculture(s) positive(s)
Au moins une hémoculture positive à un germe réputé pathogène prélevée au pic thermique
Deux hémocultures positives (à 48 heures d’intervalle maximum) prélevées au pic thermique pour les germes suivants : Staphylococcus à coagulase négative, Bacillus sp, Corynébacterium sp, Propionobacterium sp, Micrococcus sp, Acinetobacter sp.
Une bactériémie peut être primitive sans foyer infectieux identifié ou secondaire avec un foyer infectieux identifié (poumon, urines, brûlure…). Le diagnostic associera donc les signes de bactériémie à ceux de l’organe considéré. Dans le cas particulier d’une bactériémie lié au cathéter veineux central, il faudra :
• Un diagnostic de bactériémie avec hémoculture positive survenant dans les 48 heures encadrant le retrait du KT en l’absence d’autre foyer infectieux au même germe
• ET l’un des critères suivants :
– Culture quantitative du cathéter au même germe : au moins 103 CFU/ml
– Hémocultures différentielles avec CVC/périphau moins = 5 ou délai de positivité CVC/périph au moins = 2 h au même germe
Infection du cathéter central :
Infection locale ou générale non bactériémique avec TOUS les critères suivants :
- • Absence d’hémoculture au même germe
- • Absence de signes généraux
- • CVC positif 103 CFU/ml
- • Régression du syndrome infectieux dans les 48 heures suivant retrait du KT
Infection urinaire :
ECBU positif
Asymptomatique (sans signes généraux) :
- • Uroculture avec au moins 105 CFU/ml si le patient a été sondé dans les
- 7 jours précédents.
- • En l’absence de sondage, 2 urocultures consécutives avec au moins 105 CFU/ml au(x) mêmes germes sans qu’il y ait plus de deux espèces
- Symptomatique (avec signes généraux) :
- • Uroculture avec au moins 105 CFU/ml (2 espèces max)
- ou au moins 103 CFU/ml avec au moins104 leucocytes/ml
ET des signes généraux
9. Recommandations relatives à l’utilisation des antibiotiques
chez le brûlé à la phase aigue (mars 2008)
Critères d’Hospitalisation d’un brûlé dans un Centre de Brûlés
Hospitalisation à la phase aigüe :
Adultes :
– Surface brûlée > 20%
– Surface brûlée >10% AVEC brûlures profondes (2e degré profond ou 3e degré)
– Surface brûlée < 10% ET critères de gravité :
Atteinte d’une zone à risque fonctionnel
– • Mains
– • Pieds
– • Face
– • Périnée
– • Plis de flexion
Signes de gravité
- • Inhalation de fumées (suspectée ou avérée)
- • Lésions circulaires
Pathologie(s) associée(s) – liste non exhaustive
- • Polytraumatisme
- • Insuffisance respiratoire chronique
- • Cardiopathie / coronaropathie (sévère et /ou instable)
- • Diabète
Difficultés à mettre en œuvre un traitement ambulatoire :
- • Hyperalgésie (nécessité de recourir aux antalgiques de palier 3)
- • Conditions de vie défavorables (SDF, manque d’hygiène)
- • Impossibilité à se rendre à la consultation (domicile éloigné …)
Mécanisme lésionnel :
- • Brûlures électriques (électrocution)
- • Brûlures chimiques par acide fluorhydrique ou phosphorique
Age :
- • Adulte > 70 ans
Enfants :
- Enfant de moins de 5 ans si Surface brûlée > 5 % et/ou brûlures profondes
- Enfant de plus de 5 ans si Surface brûlée ≥ 10 %
- Enfant de plus de 5 ans si Surface brûlée < 10 % et mêmes critères de gravité que pour l’adulte
Hospitalisation à la phase secondaire :
– Pour surinfection des brûlures
– Pour la réalisation des greffes dermo - épidermiques
Les brûlures n’ayant pas cicatrisé après 15 jours d’évolution doivent faire l’objet d’un avis spécialisé auprès d’un service de brûlés.

Dans tous les autres cas de l’organigramme ci-dessus, la prise en charge ambulatoire est possible.
Dans le doute, il est recommandé de contacter un spécialiste de la brûlure

– A lire
Sagediagram Ce programme en ligne (ou a la vente) vous aidera pour déterminer les surfaces brûlées ou greffées (en % et en cm2) chez l’adulte ou chez l’enfant. Lire l’évaluation dans le numéro de février 2002 du "Journal of Burn Care and Rehabilitation"
(Vol 23 n°1 pp 55-59).
BurnCase 3D est un logiciel qui est capable de simplifier et d’améliorer le diagnostic, le traitement médical et la documentation des brûlures humaines.
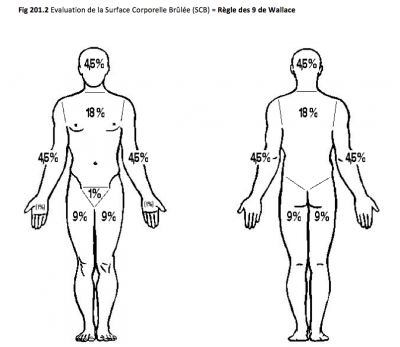
– La règle des 9 de Wallace

La règle des 9 de Wallace permet d’évaluer l’étendue d’une brûlure sur le corps.
C’est une méthode qui propose de procéder rapidement à une première estimation de l’étendue de la brûlure en associant 9% (ou multiples de 9) de surface totale à chaque partie du corps, pour un total de 100, avec 1% pour la zone des parties génitales.
Pour un adulte, la règle est :
- 9% pour la tête et le cou ;
- 9% pour chaque bras (dont la main ; la paume de main représentant à elle seule 1%) ;
- 18% pour la face avant du tronc ;
- 18% par la face arrière du tronc ;
- 18% pour chaque jambe ;
- 1% pour le périnée.
Pour un enfant, la table diffère :
- 17% pour la tête et le cou ;
- 9% pour chaque bras ;
- 18% pour la face avant du tronc ;
- 18% par la face arrière du tronc ;
- 14% pour chaque jambe ;
- 1% pour le périnée.
Cette règle des 9 de Wallace reste très approximative, la table de Berkow étant bien plus précise puisqu’elle prend en considération l’âge du patient, ainsi que celles de Browder et Lund, mais permet toutefois, grâce à sa facilité de mémorisation, de rapidement évaluer la SCB (surface corporelle brûlée) et de procéder à la meilleure prise en charge du patient.
– Table de Berkow
Tableau indiquant la surface corporelle segment par segment utilisée pour apprécier l’étendue des lésions chez un brûlé.
Créé par Samuel gordon Berkow, un chirurgien américain.
– Tableau de Lund et Browder

– UNITE DE BRÛLURE STANDARD (UBS)
Il prend en compte 2 paramètres : l’étendue et la profondeur
Son mode de calcul est le suivant :
UBS = SCBT + 3 x SCB en 3ème degré
Le score maximum est celui d’un patient brûlé à 100% de SCBT.L’ensemble des lésions est en 3ème degré :
UBS = 100 + 3(100) = 400
En fonction de l’UBS, les brûlures sont classées en 3 groupes de gravité croissante :
– UBS > 50 : brûlures graves
– UBS > 100 : brûlures très graves
– UBS > 150 : pronostic vital engagé
– UBS > 200 : survie impossible
Exemple
Un patient brûlé à 60% dont 40% sont au 3ème degré aura un score UBS = 60 + (40 x 3 ) = 180 correspondant à une brûlure très grave.
– INDEX DE BAUX MODIFIE
Les patients âgés de moins de 20 sont exclus de ce système.
Il est très rudimentaire et prend en compte 2 paramètres : la surface et l’âge.
Score de Baux = SCB (Surface Cutanée Brûlée) + âge
– Baux > 75 Brûlures graves
– Baux > 100 90% de décès
Grave si score de Baux > 50
§§§
Quelle probabilité de survie pour les grands brûlés aujourd’hui ?
Publié le 20/03/2015
Les lésions par brûlure ont comme particularité d’être visuellement quantifiables, avec la mise au point depuis les années 1950, de scores pronostiques. Ces formules, basées sur la surface cutanée brûlée, et pouvant de plus prendre en compte le mécanisme de la brûlure et les variables biologiques, restent-elles actuellement fiables pour établir un pronostic ? Des auteurs ont examiné les facteurs associés à un risque accru de mortalité et de morbidité en cas de brûlures étendues afin d’identifier les patients pouvant tirer bénéfice de thérapies expérimentales.
Les patients brûlés ont été inclus de façon prospective dans le cadre d’une étude de cohorte multicentrique (6 centres de grands brûlés en Amérique du Nord). Les critères d’inclusion suivants ont été retenus : âge de 0 à 99 ans, admission dans les 96 heures suivant la brûlure, plus de 20 % de la surface totale du corps brûlée avec nécessité d’au moins une intervention chirurgicale. Les données évolutives recueillies ont pris en considération la taille des zones brûlées, les infections des plaies, l’existence d’une septicémie, d’une pneumonie, d’un syndrome de détresse respiratoire aiguë, et le nombre de défaillances multiviscérales.
Un total de 573 patients a été inclus, dont 226 enfants (âge de moins de 16 ans), 325 patients adultes (âge de 16 à 65 ans) et 23 patients âgés (plus de 65 ans). Les données générales sont résumées dans le tableau 1.
Chez les enfants, la taille de la brûlure déterminant la mortalité, ou un risque accru de complications (septicémie, infection de la plaie, défaillance multiviscérale) est d’environ 60 % de la surface du corps. Chez les adultes, le seuil pour ces résultats est plus faible, à environ 40 % de la surface corporelle totale. Chez les enfants, les auteurs notent une plus grande prévalence des infections ou des contaminations des plaies par rapports aux patients adultes (93 % contre 55 %, p < 0,0001), mais en revanche moins de pneumonies et de sepsis (9 et 2 % vs. 45 et 10 %, p < 0,0001, respectivement). La mortalité globale est de 8 % chez les moins de 16 ans, de 17 % de 16 à 65 ans et de 57 % chez les plus de 65 ans (p < 0,0001).
Les résultats de cette étude montrent donc que les adultes avec plus de 40 % de la surface totale du corps brûlé et les enfants avec un taux de brulure plus de 60 % du total de la surface corporelle sont à risque élevé de morbidité et de mortalité, même dans des centres hautement spécialisés. Le faible effectif de la population des plus de 65 ans rend les conclusions plus difficiles, mais on peut dire que le pronostic chez les malades âgés est réservé.
Dr Béatrice Jourdain (jim.fr)
Références
Jeschke M et coll. : Morbidity and Survival Probability in Burn Patients in Modern Burn Care*
Crit Care Med 2015 ; 43 : 808-815
Quand le patient prend feu au bloc opératoire
16 août 2017, par Marc Gozlan, source : realitesbiomedicales.blog.lemonde.fr
Il peut se passer bien des choses imprévues au cours d’une intervention chirurgicale. J’avais relaté dans deux précédents billets les cas de chutes accidentelles de la table d’opération ou encore les cas où le chirurgien oublie compresses et autres textiles dans le corps du malade. Ici, je vous raconte l’histoire de ce que les spécialistes appellent « un feu de patient ». Ce cas clinique est rapporté par des anesthésistes-réanimateurs américains dans un article paru en ligne le 3 août 2017 dans A&A Case Reports, revue d’anesthésie et d’analgésie.
Chez ce patient de 79 ans, les voies aériennes se sont littéralement embrasées au cours d’une trachéotomie, intervention consistant à pratiquer une ouverture dans la partie haute de la trachée, au niveau du cou, afin de faciliter le passage de l’air au niveau des voies aériennes et donc aider le patient à respirer.
L’histoire commence lorsque ce malade est hospitalisé pour de graves problèmes respiratoires et cardiaques au Mount Sinai Medical Center de Miami (Floride). Il subit trois gestes chirurgicaux cardiaques : réparation de la valve mitrale, remplacement de la valve aortique, ainsi qu’une procédure destinée à corriger un trouble du rythme cardiaque responsable de battements de cœur très rapides et irréguliers (fibrillation atriale).
Les suites opératoires sont compliquées par une insuffisance respiratoire. Celle-ci nécessite de multiples intubations, geste consistant à introduire une sonde tubulaire dans la trachée afin de permettre la ventilation. De même, il est nécessaire de pratiquer de fréquentes bronchoscopies, examen permettant de dégager la trachée et les grosses voies respiratoires des poumons (bronches) encombrées par d’épaisses sécrétions. Devant la difficulté à réaliser l’ablation de la sonde d’intubation (extubation) à plusieurs reprises et la dépendance prolongée à la ventilation du patient, les médecins décident de réaliser une trachéotomie afin d’assurer une perméabilité permanente des voies aériennes.
Une sonde d’intubation est introduite dans la trachée. Ce malade, insuffisant respiratoire, est ventilé avec une fraction inspirée d’oxygène (FiO2) de 40 %. Autrement dit, l’air que le patient inspire est enrichi en oxygène à hauteur de 40 %, alors que celui que l’on respire normalement en contient moitié moins (20,9 %). L’anesthésie générale peut alors débuter.
Une flamme de 3 cm
Lors de l’incision au niveau du cou, le chirurgien utilise un bistouri électrique monopolaire pour l’électrocoagulation (contrôle du saignement des tissus). Une fois la trachée exposée, la FiO2 (pourcentage d’oxygène dans l’air inspiré) est augmentée à 100 % afin d’apporter une oxygénation suffisante avant de procéder à l’incision. Dès l’ouverture de la trachée au bistouri monopolaire, une flamme de 3 cm jaillit de l’orifice de trachéotomie. Du sérum physiologique est immédiatement versé sur le champ opératoire, ce qui permet l’extinction de la flamme. La sonde d’intubation trachéale est immédiatement retirée et la FiO2 est abaissée au niveau de l’air ambiant. Les voies aériennes supérieures sont ensuite inondées avec du sérum physiologique afin d’éteindre le feu et refroidir les tissus. Le chirurgien réintube alors le patient avec une nouvelle sonde. L’état du malade stabilisé, le feu éteint, la FiO2 est de nouveau portée à 100 % durant la poursuite de la trachéotomie.
La bronchoscopie, qui permet de visualiser l’intérieur des bronches, révèle des lésions de la muqueuse du poumon droit (lobes supérieur et moyen). Par ailleurs, à l’examen de la région située au-dessus de la glotte (segment du larynx comprenant les cordes vocales), les médecins observent que la muqueuse est rouge, enflammée et le siège d’un œdème (gonflement). Chez ce patient, il y a eu donc embrasement des voies aériennes au cours d’une trachéotomie chirurgicale.
Les bronchoscopies répétées vont révéler une muqueuse noircie dans le segment de la trachée situé sous la zone où se situait la sonde d’intubation qui a pris feu. Le patient, qui présente un risque d’infection du fait des brûlures de la trachée et des sécrétions purulentes dans le lobe supérieur du poumon gauche, reçoit des antibiotiques en unité de soins intensifs. La semaine suivante, les bronchoscopies montrent des sécrétions purulentes plus fréquentes avec un affaissement du poumon gauche. Les médecins constatent de surcroît la persistance de la fibrillation atriale, associée à une hypotension artérielle. Finalement, le patient décède d’une défaillance du cœur, des poumons et des reins.

Sonde d’intubation carbonisée à sa partie inférieure. Embrasement des voies aériennes au cours d’une trachéotomie. P. Gorphe, et al. Eur Ann Otorhinolaryngol Head Neck Dis. 2014 Jun ;131(3):197-9.
« Triangle de feu »
Trois éléments sont nécessaires pour déclencher un feu au bloc opératoire : un matériau combustible (ou carburant), un agent oxydant (ou comburant), et une source de chaleur ou d’énergie (bistouri électrique, laser). Cette association constitue le « triangle de feu ».
Au bloc opératoire, les comburants sont représentés par deux gaz administrés par les anesthésistes dans les voies aériennes : l’oxygène et le protoxyde d’azote (N2O). Dans le cas rapporté dans la revue A&A Case Reports, le comburant est l’oxygène. Le combustible est, lui, représenté par la sonde d’intubation trachéale en PVC, matériau dont la combustion est possible dès que la fraction inspirée d’oxygène (FiO2) est supérieure à 25 %. En effet, l’oxygène est inflammable à partir d’une concentration FiO2 de 25 %. Dès lors, pourquoi utiliser une FiO2 à 100 % lors d’une trachéotomie ? Parce que ventiler un patient en air ambiant alors que l’on entreprend d’exposer par voie chirurgicale la trachée fait courir au patient (souvent insuffisant respiratoire ou dans un état critique) le risque d’avoir un taux insuffisant d’oxygène dans le sang et de fournir une mauvaise oxygénation (hypoxie) aux organes. Enfin, le bistouri électrique est la source de chaleur.
Mesures de prévention

La région carbonisée de la sonde d’intubation trachéale correspond à l’orophrynx. Akhtar N, et al. J Anaesthesiol Clin Pharmacol. 2016 Jan-Mar ;32(1):109-11.
La survenue d’un feu de patient (sur ou à l’intérieur du corps du malade, comme dans le cas d’un embrasement des voies aériennes) est un événement rare, mais potentiellement gravissime. Au total, 20 % des victimes souffrent de lourdes séquelles (brûlures graves, visage défiguré), ou en décèdent.
Il n’existe actuellement pas de mode de ventilation, ni aucune de sonde de ventilation, permettant une prévention absolue contre les événements d’embrasement des voies aériennes. En revanche, il importe pour les médecins anesthésistes-réanimateurs d’adopter des mesures de sécurité et de prévention, à commencer par renforcer la coordination et la communication entre l’équipe d’anesthésie et le chirurgien.
Il convient d’utiliser un bistouri électrique bipolaire lorsque le chirurgien réalise l’électrocoagulation. En effet, la diffusion de la chaleur est moindre avec cet instrument qu’avec un bistouri unipolaire qui, lui, délivre une source d’énergie générant un pic de température de 910 °C. Lors d’une trachéotomie, il est donc recommandé d’utiliser un bistouri électrique bipolaire plutôt qu’unipolaire. Surtout, lors de l’incision de la trachée, il ne faut pas utiliser la coagulation électrique mais un bistouri froid. Dans le cas rapporté par les anesthésistes de Miami, l’événement déclencheur du feu de patient a été l’utilisation d’un bistouri électrique monopolaire en présence d’une ventilation avec une concentration en oxygène inspirée de 100 %.
Un environnement enrichi en oxygène
Il est recommandé d’utiliser la fraction inspirée d’oxygène (Fi02) la plus basse possible pour ventiler le patient pendant l’incision de la trachée. En présence d’une étincelle, comme lorsqu’un arc électrique se produit entre le bistouri électrique et un écarteur chirurgical métallique, le risque d’incendie est en effet moindre avec une FiO2 inférieure à 50 %. Un feu de patient a cependant déjà été rapporté lorsque la concentration en oxygène délivrée est abaissée à 30 %, voire à 25 %. L’utilisation de protoxyde d’azote (N2O) est à proscrire en cas de chirurgie à haut risque de feu.
La concentration en oxygène au niveau du site opératoire dépend notamment de son mode d’administration. Ainsi, lorsque le patient porte des « lunettes à oxygène » (sondes nasales) ou un masque facial, une accumulation d’oxygène peut se produire. En effet, ces dispositifs ne sont pas étanches, ce qui peut favoriser un feu de patient. De même, la disposition des champs opératoires (textiles recouvrant le patient) peut favoriser l’accumulation progressive d’oxygène, créant localement une situation propice au déclenchement d’un feu en cas de communication avec un bistouri électrique activé.
Dans un bloc opératoire, de nombreux matériaux peuvent servir de combustibles, notamment les compresses, les champs opératoires en textile, la sonde d’intubation, sans oublier les sourcils, les cheveux, la barbe, les gaz intestinaux du patient, mais également la solution antiseptique à base d’alcool utilisée sur la peau de la zone à opérer. En effet, les vapeurs risquent de s’enflammer si un temps de séchage suffisant n’est pas respecté. Il est généralement de l’ordre de trois minutes mais peut varier selon la pilosité du patient et la nature du produit utilisé.
Gaz intestinaux
La trachéotomie et autres interventions chirurgicales sur la tête et le cou ne résument cependant pas la totalité des situations des feux de patient au bloc opératoire. Des embrasements des voies digestives, par déclenchement d’un feu intra-abdominal du fait d’une insufflation d’oxygène au lieu de dioxyde de carbone, ont été rapportés lors d’une chirurgie de la prostate robotisée et d’une cœlioscopie (chirurgie non invasive).
Enfin, en octobre 2016, le quotidien japonais Asahi Shimbun a rapporté que la Tokyo Medical University a publié un rapport expliquant que les flatulences d’une patiente ont provoqué un feu au bloc opératoire. Le cas concerne une trentenaire dont l’émission de gaz intestinaux (qui contiennent du méthane inflammable) a provoqué un départ de flammes lors d’une intervention au laser sur le col utérin. Les draps chirurgicaux s’étaient consumés dans l’incendie. La patiente avait été brûlée sur une grande partie du corps, notamment à la taille et sur les jambes.
Feux de patient et chirurgie de la tête et du cou
Environ 550 à 650 cas de feux au bloc opératoire surviennent lors des 65 millions interventions chirurgicales pratiquées chaque année aux Etats-Unis, indiquent le Dr Osman Nawazish Salaria et ses collègues anesthésistes du Mount Sinai Medical Center de Miami (Floride) dans leur article paru dans A&A Case Reports.
En France, deux cas de feux de patient au cours d’une trachéotomie ont été rapportés en 2013 par des anesthésistes et chirurgiens ORL du CHU de La Réunion (Saint-Pierre) et en 2014 par des chirurgiens et anesthésistes du département de cancérologie cervico-faciale de l’Institut de cancérologie Gustave-Roussy (Villejuif).
La grande majorité des cas des feux de patients surviennent lors de procédures chirurgicales telle qu’une trachéotomie, l’ablation des amygdales, la réalisation d’une fibroscopie bronchique, l’opération de la cataracte, et plus généralement lors d’un acte de chirurgie de la tête, du visage, du cou, des voies aériennes supérieures, de la partie supérieure du thorax. La chirurgie ORL est ainsi souvent concernée dans la survenue de ces incendies du fait de la proximité entre la zone opératoire et les voies respiratoires dans lesquelles circule l’oxygène administré au patient pendant l’acte chirurgical.
Pour en savoir plus :
- Salaria ON, Suthar R, Abdelfattah S, Hoyos J. Intraoperative and Postoperative Management of a Case of an Airway Fire. A A Case Rep. 2017 Aug 3. doi : 10.1213/XAA.0000000000000620
- Akhtar N, Ansar F, Baig MS, Abbas A. Airway fires during surgery : Management and prevention. J Anaesthesiol Clin Pharmacol. 2016 Jan-Mar ;32(1):109-11. doi : 10.4103/0970-9185.175710
- Kim MS, Lee JH, Lee DH, Lee YU, Jung TE. Electrocautery-Ignited Surgical Field Fire Caused by a High Oxygen Level during Tracheostomy. Korean J Thorac Cardiovasc Surg. 2014 Oct ;47(5):491-3. doi : 10.5090/kjtcs.2014.47.5.491
- Gorphe P, Sarfati B, Janot F, Bourgain JL, Motamed C, Blot F, Temam S. Airway fire during tracheostomy. Eur Ann Otorhinolaryngol Head Neck Dis. 2014 Jun ;131(3):197-9. doi : 10.1016/j.anorl.2013.07.001
- Lopez S, Marchand JH, Fossier T, Wu D, Inglès M. Feu de patient au cours d’une trachéotomie : un évènement rare, mais potentiellement gravissime. Ann Fr Anesth Reanim. 2013 May ;32(5):375-6. doi : 10.1016/j.annfar.2013.02.023
- Eichhorn JH. A burning issue : preventing patient fires in the operating room. Anesthesiology. 2013 Oct ;119(4):749-51. doi : 10.1097/ALN.0b013e3182a34de5
- Apfelbaum JL, Caplan RA, Barker SJ, Connis RT, Cowles C, Ehrenwerth J, Nickinovich DG, Pritchard D, Roberson DW, Caplan RA, Barker SJ, Connis RT, Cowles C, de Richemond AL, Ehrenwerth J, Nickinovich DG, Pritchard D, Roberson DW, Wolf GL ; American Society of Anesthesiologists Task Force on Operating Room Fires. Practice advisory for the prevention and management of operating room fires : an updated report by the American Society of Anesthesiologists Task Force on Operating Room Fires. Anesthesiology. 2013 Feb ;118(2):271-90. doi : 10.1097/ALN.0b013e31827773d2
- Crumière PP, Albaladejo R, De Saint Maurice G, Trabold F, Mc Nelis U, Boileau S, Bouaziz H ; les membres du bureau de l’institut lorrain d’anesthésie et de réanimation (ILAR). Feu d’un patient au bloc opératoire : sommes-nous prêts à gérer ce type d’incident ? Résultats d’une enquête faite auprès des médecins anesthésistes-réanimateurs lorrains. Ann Fr Anesth Reanim. 2012 Oct ;31(10):773-7. doi : 10.1016/j.annfar.2012.04.026
- Shin YD, Lim SW, Bae JH, Yim KH, Sim JH, Kwon EJ. Wire-reinforced endotracheal tube fire during tracheostomy-A case report. Korean J Anesthesiol. 2012 Aug ;63(2):157-60. doi : 10.4097/kjae.2012.63.2.157
- Bouaziz H. La prévention des feux de patient au bloc opératoire. Société Française des Infirmier(e)s Anesthésistes. Avril 2012.
- Smith LP, Roy S. Operating room fires in otolaryngology : Risk factors and prevention. Am J Otolaryngol. 2011 ;32:109–14.
Faire feu de tout bois pour prévenir les intoxications au CO
Publié le 18/10/2018
Gaz inodore et incolore, le monoxyde de carbone (CO) est produit lorsqu’un combustible fossile est brûlé dans un four, un véhicule, un groupe électrogène ou un gril. Il s’accumule dans des espaces clos ou semi-fermés et intoxique les personnes et les animaux qui s’y trouvent, sans que ceux-ci en aient conscience. Le CO est responsable d’environ 21 000 admissions aux Urgence (hors incendies et tentatives de suicide), de 2 300 hospitalisations et de 500 décès par an aux États-Unis. Chaque année s’y ajoutent 2 000 décès par suicide au CO. L’intoxication au CO non intentionnelle et non liée à un incendie demeure la deuxième cause la plus fréquente de décès par empoisonnement non médical aux États-Unis. Bon nombre des intoxications involontaires au CO se produisent à l’intérieur des habitations par négligence de l’entretien des sources les plus courantes de CO (appareils de chauffage au gaz, chauffe-eaux, sèche-linge) et toute l’année, avec un pic au décours des catastrophes naturelles qui causent des pannes d’électricité, lors de la mise en route de groupes électrogènes, d’appareils de chauffage d’appoint et d’outils électriques. De 1975 à 1996, après l’introduction des premiers convertisseurs catalytiques et autres dispositifs antipollution pour automobiles aux États-Unis, le taux annuel de décès non intentionnels liés aux véhicules automobiles a diminué de 21,3 %.
Toutefois, ces informations sont fragmentaires et pour y voir plus clair, les données de 10 années provenant de deux programmes de surveillance ont été analysées dans 17 États entre 2005 et 2014.
De la négligence dans l’entretien des équipements
Au cours de ces dix années, les 17 États ont recensé 1 795 incidents liés au CO dont 897 ayant occasionné des pathologies. Sur les 3 414 personnes ayant développé des pathologies au CO, 61,0 % appartenaient au grand public ; 27,7 % étaient des employés, 7,6 % des étudiants et 2,2 % des secouristes ; 78 % de ces personnes ont dû être hospitalisées ou recevoir des soins pré-hospitaliers et 4,3 % sont décédées ; 39,9 % de ces personnes se trouvaient dans des maisons ou des appartements, et 10,0 % dans des établissements d’enseignement. Parmi les 2 694 personnes intoxiquées au CO dont l’âge était connu, 743 (27,6 %) avaient moins de 18 ans, dont 211 se trouvaient dans leur école lorsqu’elles ont été intoxiquées.
Les trois sources les plus courantes de CO étaient les systèmes de chauffage, de ventilation et de climatisation, les groupes électrogènes et les véhicules automobiles. La défaillance de l’équipement a été le principal facteur contributif de la plupart des incidents liés au CO.
Les 17 États ont utilisé ces données pour mettre en place des actions ciblées de santé publique. L’idée est de mettre en place une déclaration obligatoire de l’intoxication et d’exiger des alarmes au CO dans toutes les écoles et les logements.
Dr Bernard-Alex Gaüzère
Référence
Mukhopadhyay S, Hirsch A, Etienne S, Melnikova N, Wu J, Sircar K, Orr M : Surveillance of carbon monoxide-related incidents - Implications for prevention of related illnesses and injuries, 2005-2014. Am J Emerg Med., 2018 ; 36(10):1837-1844. doi : 10.1016/j.ajem.2018.02.011.
Source : jim.fr
— -
– En complément :
Fire Safety VIDEO (Anesthesia Patient Safety Foundation)
Prevention and Management of Operating Room Fires (Anesthesia Patient Safety Foundation)
§§§
Arnaud BASSEZ
IADE
administrateur