Décret n° 2023-368 du 13 mai 2023 relatif à la suspension de l’obligation de vaccination contre la covid-19 des professionnels et étudiants
Le décret lève l’obligation vaccinale des soignants et permet le retour en poste des soignants non -vaccinés contre le Covid, qui étaient suspendus de leur fonction depuis août 2021. Les conditions de ce retour, qui prévoient que la personne suspendue se voie réintégrée dans le même poste ou un poste « équivalent », ont été définie dans une instruction ministérielle.
Arrêté du 17 août 2021 portant diverses dispositions relatives à l’indemnisation des professionnels de santé en exercice, retraités ou en cours de formation réquisitionnés dans le cadre de l’épidémie de covid-19
LOI n° 2021-1040 du 5 août 2021 relative à la gestion de la crise sanitaire
Décret n° 2021-384 du 2 avril 2021 modifiant les décrets n° 2020-1262 du 16 octobre 2020 et n° 2020-1310 du 29 octobre 2020 prescrivant les mesures générales nécessaires pour faire face à l’épidémie de covid-19 dans le cadre de l’état d’urgence sanitaire
Décret n° 2020-1310 du 29 octobre 2020 prescrivant les mesures générales nécessaires pour faire face à l’épidémie de covid-19 dans le cadre de l’état d’urgence sanitaire
Décret n° 2020-1309 du 29 octobre 2020 portant indemnisation et majoration exceptionnelle des heures supplémentaires réalisées dans les établissements mentionnés aux 1°, 2°, 3° et 5° de l’article 2 de la loi n° 86-33 du 9 janvier 1986 portant dispositions statutaires relatives à la fonction publique hospitalière
Décret n° 2020-1262 du 16 octobre 2020 prescrivant les mesures générales nécessaires pour faire face à l’épidémie de covid-19 dans le cadre de l’état d’urgence sanitaire
Arrêté du 24 juillet 2020 modifiant l’arrêté du 10 juillet 2020 prescrivant les mesures générales nécessaires pour faire face à l’épidémie de covid-19 dans les territoires sortis de l’état d’urgence sanitaire et dans ceux où il a été prorogé
– Décret n° 2020-698 du 8 juin 2020 modifiant le décret n° 2020-568 du 14 mai 2020 relatif au versement d’une prime exceptionnelle aux agents des établissements publics de santé et à certains agents civils et militaires du ministère des armées et de l’Institution nationale des invalides dans le cadre de l’épidémie de covid-19
– Décret n° 2020-568 du 14 mai 2020 relatif au versement d’une prime exceptionnelle aux agents des établissements publics de santé et à certains agents civils et militaires du ministère des armées et de l’Institution nationale des invalides dans le cadre de l’épidémie de covid-19
– Arrêté du 28 mars 2020 portant diverses dispositions relatives à l’indemnisation des professionnels de santé en exercice, retraités ou en cours de formation réquisitionnés dans le cadre de l’épidémie covid-19
– Décret n° 2020-314 du 25 mars 2020 complétant le décret n° 2020-293 du 23 mars 2020 prescrivant les mesures générales nécessaires pour faire face à l’épidémie de covid-19 dans le cadre de l’état d’urgence sanitaire
– Décret n° 2020-297 du 24 mars 2020 relatif aux heures supplémentaires et à leur dépassement dans les établissements mentionnés à l’article 2 de la loi n° 86-33 du 9 janvier 1986 portant dispositions statutaires relatives à la fonction publique hospitalière
– Décret n° 2020-293 du 23 mars 2020 prescrivant les mesures générales nécessaires pour faire face à l’épidémie de covid-19 dans le cadre de l’état d’urgence sanitaire
– LOI n° 2020-290 du 23 mars 2020 d’urgence pour faire face à l’épidémie de covid-19 (1)
– Arrêté du 6 mars 2020 autorisant par dérogation la mise à disposition sur le marché et l’utilisation temporaires de certains produits hydro-alcooliques utilisés en tant que biocides désinfectants pour l’hygiène humaine
– Décision du 5 mars 2020 portant application de l’article 15, alinéa 3, du décret n° 2002-9 du 4 janvier 2002 relatif au temps de travail et à l’organisation du travail dans les établissements mentionnés à l’article 2 de la loi n° 86-33 du 9 janvier 1986 portant dispositions statutaires relatives à la fonction publique hospitalière
Afin de faire face à l’épidémie de virus covid-19, cette décision autorise les établissements publics de santé, à titre exceptionnel, pour la période du 1er février au 30 juin 2020, et pour les personnels nécessaires à la prise en charge des patients, à recourir de façon transitoire aux heures supplémentaires au-delà des plafonds fixés à l’article 15 du décret 2002-9.
Elle intervient en application de l’alinéa 3 de l’article précité qui prévoit qu’en cas de crise sanitaire, les établissements de santé peuvent être autorisés, par décision du ministre de la santé, à titre exceptionnel, pour une durée limitée et pour les personnels nécessaires à la prise en charge des patients, à dépasser les bornes horaires fixées par le cycle de travail.
Précisions :
- Cette dérogation ne vaut que pour la période précitée. S’agissant des autres mois de l’année, les plafonds correspondants aux cycles de travail doivent être respectés, conformément à l’alinéa 3 de l’article 15 du décret n°2002-9.
- En tout état de cause, il ne saurait être dérogé à l’article 6 du décret n°2002-9 qui prévoit que la durée hebdomadaire de travail effectif, heures supplémentaires comprises, ne peut excéder 48 heures au cours d’une période de 7 jours.
- A ce jour, les établissements sociaux et médico-sociaux ne sont pas concernés par cette mesure.
– Décret n° 2020-73 du 31 janvier 2020 portant adoption de conditions adaptées pour le bénéfice des prestations en espèces pour les personnes exposées au coronavirus
Lire en complément
- Remets ton masque, on l’a reconnu ! (Masques FFP1, FFP2, FFP3, N95-SRAS-coronavirus-Covid-19)
- Une base de données sur les pratiques et préconisations sur le COVID-19 pour le personnel soignant dans son ensemble
En préambule, le HCSP rappelle que cette prise en charge implique de respecter strictement les règles d’hygiène et les mesures de distance physique contre le SARS-CoV-2 ainsi que les différentes pratiques culturelles et sociales existantes autour du corps d’une personne décédée.
Le HCSP émet des recommandations générales sur les précautions à respecter et les équipements de protection nécessaires pour cette prise en charge ; il précise aussi les conditions pour que les proches puissent voir le visage de la personne décédée et qu’un rituel funéraire puisse être éventuellement effectué en chambre d’hospitalisation, en chambre mortuaire ou funéraire.
Il détaille ensuite les étapes et les précautions à suivre par les différents professionnels intervenant auprès des défunts, selon les lieux de survenue du décès en établissements de santé, en établissements médico-sociaux ou à domicile.
— -
— -
— -
- L’hypothèse
— -
Un médecin d’hôpital britannique ; Le Dr Sarfaraz Munshi décrit une technique respiratoire pour les personnes atteintes du virus Corona Covid-19 qui pourrait empêcher les patients de contracter une pneumonie secondaire. Nous laissons la pertinence du propos à l’appréciation de chacun.
— -
Pour développer les connaissances sur le sujet
Physiotherapy management of the respiratory patient
— -
et le PDF du topo affiché
NB : A la SOFIA nous ne discriminons personne. Nous ne prétendons pas détenir une vérité. Nous disons que lors d’une pandémie ravageuse comme celle du Covid-19, les protocoles randomisés avec une cohorte importante ne sont peut-être pas adaptés à la notion de rapidité pour laquelle nous avons besoin d’être réactif. Il serait curieux de critiquer le manque de masque et de protection personnelle individuelle qui n’arrivent pas assez vite, et de prôner la lenteur face à des traitements qui potentiellement interrogent.
Car enfin, dire d’un côté qu’il faut protéger les soignants rapidement et de l’autre protéger les patients en prenant son temps, apparait nettement comme une schizophrénie de la pensée.
Mais nous ne savons pas tout. Ici, comme ailleurs. (AB)
— -
- Caractéristiques de > 70 000 patients infectés Décembre à Mi-Février dans la province de Wuhan
- Un très bon article qui explique bien les bouleversements et l’évolution de la pandémie.
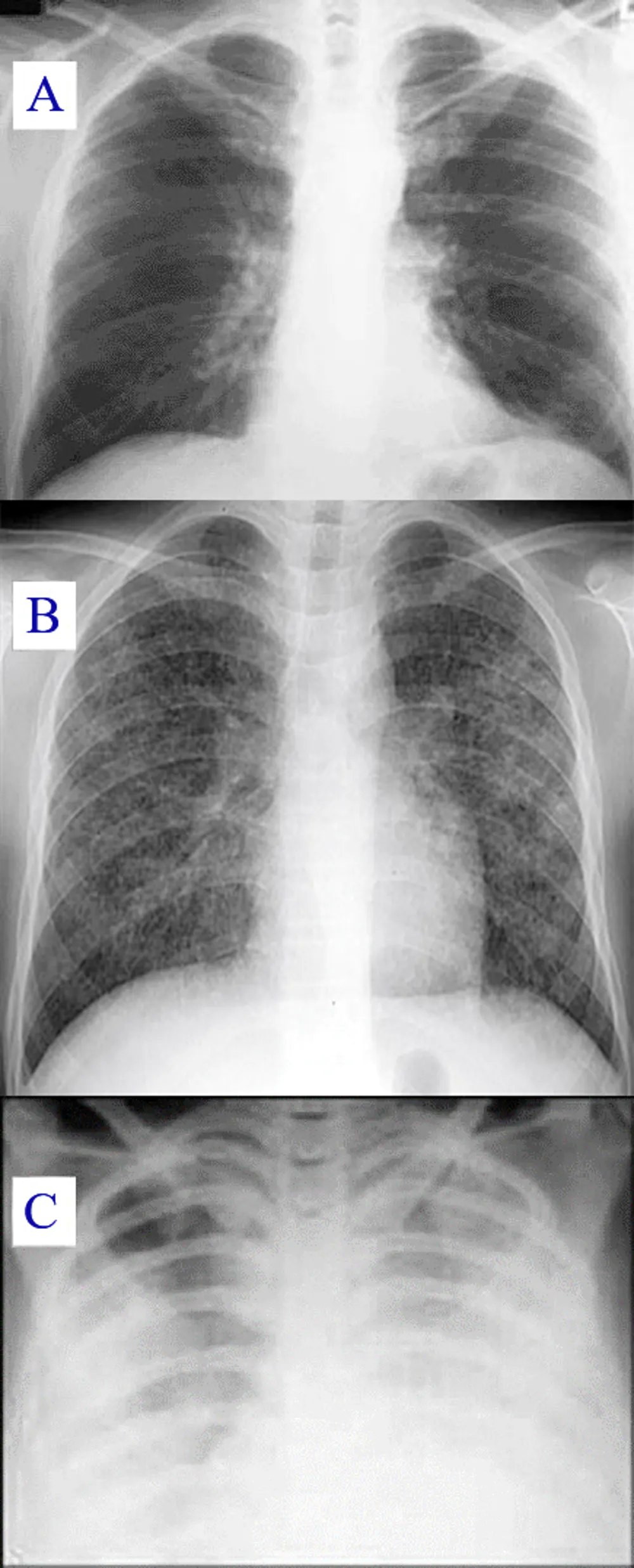
- cliquez sur le rectangle noire, pour voir un comparatif de radios pulmonaires
En haut, une radiographie du thorax normale (A), ɑu milieu, une radiographie du thorax révélant une pneumonie virale (B), et en bas une radiographie du thorax révélant un syndrome de détresse respiratoire aigu (C). DR/APHM, Author provided
- Décret n° 2020-73 du 31 janvier 2020 portant adoption de conditions adaptées pour le bénéfice des prestations en espèces pour les personnes exposées au coronavirus
— -
— -
— -
— -
— -
— -
— -
— -
— -
— -
— -
— -
— -
Quel comportement individuel adopter face au Coronavirus ?
Source : gouvernement.fr
Si je n’ai pas de symptômes j’applique les gestes barrières (je me lave les mains très régulièrement, je tousse et j’éternue dans mon coude, j’utilise des mouchoirs à usage unique, je salue sans serrer la main et j’évite les embrassades Je réduis mes sorties au strict nécessaire : travail (si télétravail impossible), courses et visites médicales indispensables.
Si je n’ai pas de symptômes mais que j’ai eu un contact étroit ou je vis avec une personne malade du COVID-19 : je m’isole à domicile, je réduis strictement mes sorties sauf pour ravitaillement alimentaire, j’applique les gestes barrières (je me lave les mains très régulièrement, je tousse et j’éternue dans mon coude, j’utilise des mouchoirs à usage unique, je salue sans serrer la main et j’évite les embrassades), je prends ma température 2 fois par jour et j’auto-surveille les symptômes de la maladie, je fais du télétravail.
Si je suis un professionnel de santé ne présentant pas de symptômes mais que j’ai eu un contact avec une personne malade du COVID-19 en l’absence de mesures de protection appropriées : je m’auto-surveille en prenant ma température 2 fois par jour, j’applique les gestes barrières (je me lave les mains très régulièrement, je tousse et j’éternue dans mon coude, j’utilise des mouchoirs à usage unique, je salue sans serrer la main et j’évite les embrassades), je porte un masque sur mon lieu de travail et avec les malades pendant 14 jours, je contacte un médecin et me fait tester systématiquement en cas d’apparition de symptômes.
Si j’ai des symptômes évocateurs de COVID 19 (toux, fièvre, difficultés respiratoires) : j’appelle mon médecin traitant ou un médecin par téléconsultation, je n’appelle le 15 que si j’ai des difficultés respiratoires ou si j’ai fait un malaise, je m’isole strictement à domicile. Je me fais tester uniquement si je suis une personne fragile ou à risque, si je présente des signes de gravité, si je suis déjà hospitalisé, si je suis un professionnel de santé, si je suis une personne fragile en structure collective (EPHAD, handicap). Les tests en ambulatoire, avec prélèvements à domicile, sont possibles. Si je n’appartiens à aucune de ces catégories, un médecin effectue le diagnostic sur signes cliniques.
Si je suis testé positif ou si je suis diagnostiqué cliniquement : je reste strictement à domicile, si j’ai un rendez-vous médical indispensable je porte un masque pour m’y rendre. En cas de difficulté respiratoire, j’appelle le 15. Je me fais prescrire un arrêt de travail par mon médecin. Selon ma situation, je m’auto-surveille, ou mon médecin met en place un protocole de surveillance. Mon isolement sera levé 48h après la résolution complète des symptômes.
Si j’ai des symptômes évocateurs de COVID 19 (toux, fièvre, difficultés respiratoires) : j’appelle mon médecin traitant ou un médecin par téléconsultation, je n’appelle le 15 que si j’ai des difficultés respiratoires ou si j’ai fait un malaise, je m’isole strictement à domicile. Je me fais tester uniquement si je suis une personne fragile ou à risque, si je présente des signes de gravité, si je suis déjà hospitalisé, si je suis un professionnel de santé, si je suis une personne fragile en structure collective (EPHAD, handicap). Si je n’appartiens à aucune de ces catégories, un médecin effectue le diagnostic sur signes cliniques. Les tests en ambulatoire sont possibles.
Si je suis testé positif ou si je suis diagnostiqué cliniquement : je reste strictement à domicile, si j’ai un rendez-vous médical indispensable je porte un masque pour m’y rendre. En cas de difficulté respiratoire, j’appelle le 15. Je me fais prescrire un arrêt de travail initial d’une durée de 7 à 14 jours, entre le 6ème et le 8ème jour j’ai un avis médical, à distance, pour faire surveiller mes symptômes. En fonction de mon état je renouvelle cet arrêt pour 7 jours supplémentaires. Mon isolement sera levé 48h après la résolution complète des symptômes.
Si je suis testé négatif, je continue d’appliquer les gestes barrières (je me lave les mains très régulièrement, je tousse et j’éternue dans mon coude, j’utilise des mouchoirs à usage unique, je salue sans serrer la main et j’évite les embrassades) et je limite mes déplacements au strict nécessaire.
Si je suis un professionnel de santé et que je présente des symptômes évocateurs du COVID-19 (toux, fièvre, difficultés respiratoires) : je contacte mon médecin, le médecin de ma structure de soin ou un médecin par téléconsultation. Je n’appelle le 15 que si j’ai des difficultés respiratoires. Je m’isole strictement à domicile et je me fais tester systématiquement. Si je suis positif, je m’isole strictement. Si je suis négatif, je peux continuer le travail.
Dois-je porter un masque ?
Le port du masque chirurgical n’est pas recommandé sans présence de symptômes. Le masque n’est pas la bonne réponse pour le grand public car il ne peut être porté en permanence et surtout n’a pas d’indication sans contact rapproché et prolongé avec un malade.Ce sont les gestes barrières et la distanciation sociale qui sont efficaces.
Les gants sont-ils utiles ?
Non. Les gants peuvent également servir de support au virus après souillage par des gouttelettes (les sécrétions respiratoires qu’on émet quand on tousse, éternue, ou discute), qui sont le moyen de transmission du coronavirus. Porter des gants est donc inutile, sauf dans des situations très spécifiques (personnels soignants réalisant des prélèvements ou gestes à risque). Ce sont les gestes barrières (se laver fréquemment les mains, tousser dans son coude, utiliser des mouchoirs à usage unique et les jeter après utilisation) et les mesures de distanciation socialeFaut-il désinfecter les surfaces ?
Oui. Les produits de nettoyage et désinfectants couramment utilisés sont efficaces contre le COVID-19. En plus du nettoyage régulier, les surfaces qui sont fréquemment touchées avec les mains doivent être nettoyées et désinfectées deux fois par jour, notamment lorsqu’elles sont visiblement souillées. Il s’agit par exemple des poignées de porte, des boutons d’ascenseur, des interrupteurs d’éclairage, des poignées de toilettes, des comptoirs, des mains courantes, des surfaces d’écran tactile et des claviers.
— -
Covid-19 en USI : soignants, protégez-vous !
Covid-19 en USI : soignants, protégez-vous !
Le personnel soignant des unités de soins intensifs (USI) est particulièrement exposé au risque infectieux quand il s’agit de prendre en charge un patient atteint du Covid-19. Les procédures qui vont permettre de faire face à une situation aiguë où le pronostic vital peut être en jeu sont variées mais elles ont toutes en commun le fait de mobiliser le virus au sein des voies aériennes du malade et de l’emmener au contact des médecins et de l’équipe paramédicale travaillant dans de telles structures. La préparation et la mise en place d’aérosols, la ventilation non invasive (VNI), la canule nasale à haut débit, la ventilation au masque ou encore l’intubation endotrachéale sont autant de gestes, de dispositifs ou de techniques qui contribuent à l’exposition du personnel soignant.
Comment se protéger au mieux ? Cette question trouve des éléments de réponse dans une lettre à l’éditeur du Lancet, mise en ligne le 13 février par l’équipe médicale d’une USI située dans l’hôpital de Sheung Shui (Hong Kong). Il faut rappeler que cette région administrative spéciale sous l’emprise de la Chine (depuis 1997) a été très tôt soumise à l’épidémie de Covid-19, déclenchée par les cas directement importés de la province du Hubei. L’expérience de cette équipe s’avère des plus précieuses car elle met en exergue la nécessité de se protéger au mieux tout en maintenant la qualité de la prise en charge à un niveau optimal.
Les précautions propres à toute USI incluent certes l’hygiène des mains qui est cruciale dans la transmission du virus, mais dans le cas précis du Covid-19, des mesures complémentaires spécifiques s’imposent à l’évidence au travers de moyen de protection accrus. Toutes les procédures pour générer un aérosol doivent être effectuées dans une chambre d’isolement spécifique, la pression négative n’étant pas nécessaire.
Prendre des gants (doubles) avec la ventilation
Les mains des soignants doivent être protégées au maximum - double gant de rigueur- afin de minimiser la dissémination du virus par les objets contaminés (fomite, vecteurs de transmission passifs) au sein des équipements environnants, l’exemple de la sonde d’intubation étant particulièrement éclairant. Des expériences menées sur des mannequins ont cependant montré que la VNI ou la canule nasale à haut débit, quand elles étaient utilisées et ajustées de manière optimale, ne conduisaient qu’à une très faible dispersion de l’air ou plus précisément du gaz expiré. Il faut néanmoins reconnaître que de nombreux modèles de ces dispositifs existent qui imposent des modes opératoires variés et les pratiques décrites dans cette étude ne sauraient prétendre à l’universalité au sein de tous les hôpitaux de la planète. Par conséquent et pour éviter toute confusion ou tout effet potentiellement néfaste, les auteurs ne recommandent l’usage de ces derniers que chez les patients considérés comme guéris du Covid-19.
Les respirateurs délivrant des débits de 6 l/mn ou plus sont considérés comme à haut débit et, à ce titre, leur usage doit être évité à moins qu’une chambre d’isolement ne soit disponible pour y recourir en toute tranquillité. Quand elle est nécessaire, l’intubation ne doit être pratiquée que par un expert spécialiste du geste et il ne faut y recourir qu’avec parcimonie à un stade précoce, uniquement quand l’état respiratoire se dégrade trop pour permettre la ventilation spontanée.
Plans B pour moins d’aérosol
Dans tous les autres cas, les plans B sont de rigueur et il est recommandé d’éviter le plus possible la ventilation au masque un tant soit peu prolongée. Il convient d’optimiser le stade d’avant le recours à l’oxygénothérapie par tous les moyens dès lors qu’ils ne passent pas par les aérosols. Par quelles méthodes ? Par exemple en surélevant la tête du lit et en recourant à des manœuvres sur les voies aériennes au travers des valves à pression expiratoire positive ou d’autres dispositifs similaires. Si une ventilation par insufflation manuelle est cependant nécessaire, il importe qu’elle soit douce et qu’elle fasse appel à un dispositif supraglottique au lieu du masque ventilatoire classique. Certes, il n’est pas formellement établi que les dispositifs supraglottiques produisent moins d’aérosol que ce dernier, mais il est clair qu’ils sont plus faciles à insérer et qu’ils permettent d’obtenir une pression de barrage suffisante pour assurer l’étanchéité. Ils exigent aussi moins de main d’œuvre et réduisent l’exposition de l’équipe de l’USI aux contaminants. Par ailleurs, les dispositifs supraglottiques de dernière génération sont dotés d’un conduit qui facilite une intubation non assistée.
Et s’il faut intuber…
La surveillance de la ventilation en situation d’intubation doit reposer sur un système du type capnographe qui mesure en continu les variations de la pression partielle en CO2 dans le gaz expiré sous la forme d’une courbe. La forme de cette dernière permet de s’assurer que la sonde endotrachéale est correctement positionnée. De plus, un tel appareil peut témoigner de manière physiologique de la qualité de l’étanchéité quand un dispositif supraglottique est utilisé en lieu et place d’une sonde d’intubation. Quand cette dernière est requise, il faut que la séquence d’induction soit la plus rapide possible, certains opérateurs préférant le rocuronium au suxamethonium du fait de sa demi-vie plus longue.
De fait, le premier de ces médicaments (1 à 2 mg/kg par voie IV) prévient efficacement la toux et les vomissements qui sont plus fréquents avec le second, le risque étant d’autant plus élevé que les manœuvres d’intubation doivent être répétées en cas d’échec initial. Une fois la sonde en place, son ballonnet doit être gonflé immédiatement pour éviter toute fuite néfaste. Cette sonde doit être reliée au respirateur artificiel au travers d’un filtre, mais avant de débuter la ventilation, il faut vérifier que la sonde est bien positionnée en s’aidant, là encore, d’un capnographe qui est déclenché dès que le ballonnet est gonflé. Ce n’est qu’à ce moment que le clinicien aura recours à l’auscultation pour confirmer l’absence d’intubation bronchique…
Ces mesures de protection mises en œuvre dans une USI d’un hôpital de Hong-Kong (Chine) doivent minimiser le risque de contamination du personnel soignant par le SRAS-CoV2, lequel s’avère maximal au sein de telles structures. Economie de gestes, réflexion et bon sens à chaque étape de la prise en charge, recours à des dispositifs adaptés au risque, ajustement des comportements et du matériel, plans B, une expérience sans doute utile pour les soignants qui ont la lourde tâche de prendre en charge les patients les plus lourds.
Dr Peter Stratford
Référence
Chun-Hei Cheung J et coll. : Protecting health-care workers from subclinical coronavirus infection. Lancet Respir Med., 2020 ; publication avancée en ligne 13 février. doi.org/10.1016/ S2213-2600(20)30066-7.
source jim.fr
— -
— -
source : gouvernement.fr
Les Coronavirus sont une grande famille de virus, qui provoquent des maladies allant d’un simple rhume (certains virus saisonniers sont des Coronavirus) à des pathologies plus sévères comme le MERS-COV ou le SRAS.
Le virus identifié en janvier 2020 en Chine est un nouveau Coronavirus. La maladie provoquée par ce Coronavirus a été nommée COVID-19 par l’Organisation mondiale de la Santé - OMS.
- Quels sont les symptômes du Coronavirus COVID-19 ?
Les symptômes principaux sont la fièvre ou la sensation de fièvre et des signes de difficultés respiratoires de type toux ou essoufflement.
- Existe-t-il un vaccin ?
Il n’existe pas de vaccin contre le Coronavirus COVID-19 pour le moment. Plusieurs traitements sont en cours d’évaluation en France, en lien avec l’OMS pour être utilisés contre le Coronavirus COVID-19. Dans l’attente, le traitement est symptomatique.
Comment se transmet le Coronavirus COVID-19 ?La maladie se transmet par les postillons (éternuements, toux). On considère donc qu’un contact étroit avec une personne malade est nécessaire pour transmettre la maladie : même lieu de vie, contact direct à moins d’un mètre lors d’une toux, d’un éternuement ou une discussion en l’absence de mesures de protection. Un des vecteurs privilégiés de la transmission du virus est le contact des mains non lavées.
- D’où vient le coronavirus COVID-19 ?
Les premières personnes à avoir contracté le virus s’étaient rendues au marché de Wuhan dans la Province de Hubei en Chine. Une maladie transmise par l’animal (zoonose) est donc privilégiée mais l’origine n’a pas été confirmée.
- Le virus a-t-il muté ?
Selon les dernières données scientifiques, il existerait en effet deux souches circulantes du virus (L et S).
La souche S serait plus ancienne que la souche L. À ce stade, rien ne permet de confirmer si la mutation a eu lieu chez l’homme ou chez les hôtes intermédiaires (animal).
La souche L serait la souche circulante la plus sévère et la plus fréquente (70% des échantillons testés dans l’étude), tandis que la souche S serait moins agressive et moins fréquente (30% des échantillons).
Grâce aux moyens de détection et aux mesures de lutte contre le coronavirus, la circulation de la souche L, plus sévère et donc plus facilement détectable, tend à diminuer.
- Peut-on attraper la maladie par l’eau ?
A ce jour, il n’a pas été rapporté de contamination par l’eau. Cette maladie est à transmission respiratoire et probablement de l’animal à l’homme, mais la source n’est pas encore identifiée.
- Peut-on transmettre le virus aux animaux ?
A ce jour, aucun risque de transmission de l’homme à l’animal a été identifié.
Certaines personnes sont-elles plus à risque ?Comme pour beaucoup de maladies infectieuses, les personnes souffrant de maladies chroniques (hypertension, diabète), les personnes âgées ou fragiles présentent un risque plus élevé.
Dans les cas plus sévères, la maladie peut entraîner un décès.
- Quel est le délai d’incubation de la maladie ?
Le délai d’incubation, période entre la contamination et l’apparition des premiers symptômes. Le délai d’incubation du coronavirus COVID-19 est de 3 à 5 jours en général, il peut toutefois s’étendre jusqu’à 14 jours. Pendant cette période le sujet peut être contagieux.
- Où sont faits les tests et quel est le délai pour établir un diagnostic ?
Les tests diagnostic du Coronavirus COVID-19 sont effectués dans tous les établissements de santé de références, plusieurs milliers peuvent être effectués chaque jour.
Le test est réalisé uniquement en cas de suspicion de la maladie, validée par le SAMU et par un infectiologue référent. Il s’agit d’un test de biologie spécifique du Coronavirus COVID-19. Le délai pour avoir un résultat est entre trois et cinq heures.
- Qu’est-ce qu’un établissement de santé de référence - ESR ?
Les ESR sont les hôpitaux référents au niveau régional. Ils sont désignés en fonction de capacités d’accueil spécifiques et des ressources humaines et techniques dont ils disposent :
- service d’aide médicale urgente (il s’agit du SAMU de coordination zonale)
- service d’accueil des urgences
- service de maladies infectieuses doté de chambres d’isolement à pression négative
- service de réanimation doté de chambres d’isolement
- service de pédiatrie doté de chambres d’isolement à pression négative
- service de médecine nucléaire
- laboratoire d’un niveau de confinement L3
- aire permettant de poser un hélicoptère.
Ils fournissent un appui technique aux Agences régionales de santé (ARS) et jouent un rôle d’expertise et de coordination technique auprès des autres établissements de santé pour la gestion des situations sanitaires exceptionnelles.
Qu’est-ce qu’un cas autochtone ?Un cas autochtone est une personne qui développe la maladie et pour laquelle on n’a pas de notion de voyage dans une zone à risque.
- Qu’est-ce qu’un cas contact ?
Le Coronavirus COVID-19 se transmet par des gouttelettes émises par une personne malade, en particulier lors de contacts étroits.
Vous êtes considérés comme cas contact :
- Si vous avez partagé le même lieu de vie que le patient malade lorsque celui-ci présentait des symptômes.
- Si vous avez eu un contact direct, en face à face, à moins d’un mètre du patient malade au moment d’une toux, d’un éternuement ou lors d’une discussion.
- Avec vos flirts et amis intimes.
- Avec vos voisins de classe ou de bureau.
- Si vous êtes voisin direct du sujet malade dans un avion ou un train, ou si vous êtes resté dans un espace confiné avec lui (voiture individuelle par exemple).
Les symptômes peuvent apparaître jusqu’à 14 jours après ce contact, et se manifestent le plus souvent par de la fièvre, accompagnée de toux.
Que se passe-t-il si vous êtes considéré comme un cas contact en France ?Les autorités sanitaires évaluent avec vous votre exposition et votre risque de contamination et vous délivrent une information sur la maladie due au virus et sur le dispositif de suivi. Un premier examen a pour objectif de vérifier que vous n’avez pas été contaminé. En cas de symptômes, un diagnostic sera réalisé pour vous proposer rapidement les meilleurs soins possibles.
Au cours des 14 jours suivant le dernier contact avec un malade, vous devez surveiller l’apparition de tout symptôme de type fièvre ou toux. Les modalités de votre suivi seront précisées par une équipe de professionnels de santé.
Que se passe-t-il si vous êtes considéré comme un cas suspect en France ?
Si vous êtes suspecté d’être atteint du coronavirus COVID-19 par un professionnel de santé et signalé au 15, le SAMU se met en lien avec un infectiologue référent pour avis. A l’issue d’un questionnaire, vous serez classé en cas possible ou exclu.
- Comment s’organise la recherche autour du virus en France ?
Le Président de la République a fait un point avec des médecins, des scientifiques des responsables de laboratoires mobilisés pour la recherche contre le coronavirus et les responsables du consortium REACTing, coordonné par l’INSERM et placé sous l’égide d’Aviesan, l’alliance de recherche en sciences du vivant et santé, et mandaté par le gouvernement pour coordonner l’effort de recherche. Le monde de la recherche est totalement mobilisé. Afin de soutenir l’effort de recherche, le ministère des Solidarités et de la Santé et le ministère de l’Enseignement supérieur, de la Recherche et de l’Innovation ont annoncé le 5 mars 2020 débloquer 5.5 millions d’euros supplémentaires dédiés au soutien et à la coordination de la réponse scientifique à la propagation du virus, portant l’effort global à 8 millions d’euros.
Coronavirus : 1, 2 et 3... que veulent dire les différents stades de l’épidémie ?
- Le stade 1 a pour objet de freiner l’introduction du virus sur le territoire national. C’est dans ce cadre que des « quarantaines » préventives ont été mises en place pour les personnes revenant d’une zone à risque. La priorité est de détecter précocement les premiers cas arrivant dans le pays. Les autorités sanitaires enquêtent sur les cas suspects et s’efforcent d’identifier les « sujets contacts » ayant eu un contact avec un malade.
- Le stade 2 a pour objet d’en freiner la propagation en France. Celui-ci est déclenché par l’identification de zones de circulation du virus sur le territoire national et la multiplication et le regroupement des cas autochtones (les clusters). Les mesures prises dans le cadre du stade 1 continuent de s’appliquer, avec certaines évolutions : des fermetures de crèches ou d’établissements scolaires peuvent désormais être envisagées. Des restrictions de visites peuvent être imposées dans les structures accueillant des populations vulnérables, comme les établissements d’hébergement pour personnes âgées dépendantes (Ehpad). Le plan envisage un appel à limiter ses déplacements, la suspension de certains transports en commun et la restriction des grands rassemblements (spectacles, rencontres sportives, foires, Salons…). Dans les clusters, ces zones de regroupement de cas, le dispositif mis en place est généralement plus contraignant.
- Le stade 3 a pour objet de gérer dans les meilleures conditions les conséquences de l’épidémie et d’en atténuer les effets. Cette étape se caractérise par la circulation du virus sur l’ensemble du territoire. L’organisation prévoit la mobilisation complète du système sanitaire hospitalier et de ville, ainsi que les établissements médico-sociaux pour protéger les populations fragiles, assurer la prise en charge des patients sans gravité en ville, et des patients présentant des signes de gravité en établissement de soins. Les activités collectives sont fortement touchées. En cas de passage au stade 3, celui où l’on constate que le virus circule et qu’il est transmissible sur l’ensemble du territoire.
Lettre APHP coronavirus COVID-19
Dans le contexte de mobilisation forte pour faire face au COVID-19, nous avons besoin d’adapter régulièrement notre dispositif en fonction de l’évolution des connaissances et de l’évolution épidémiologique, en s’appuyant sur l’expertise de nos équipes, notamment des trois centres de référence et en lien permanent avec les autorités sanitaires (Agence régionale de santé Île-de-France et Direction générale de la Santé).
À la suite d’une réunion de travail qui s’est réunie samedi 29 février 2020 avec une dizaine d’experts des disciplines les plus concernées, et sur le fondement de positions consensuelles entre eux, nous avons proposé aux autorités sanitaires que l’AP-HP puisse adapter son dispositif. Les adaptations portent sur les points suivants :1/ Adaptation des recommandations : abandon de l’éviction professionnelle systématique pour les cas contacts hospitaliers à risque modéré
Les professionnels de santé classés comme sujets contacts ne présentant pas de symptôme peuvent poursuivre leur activité. Ceux-ci doivent se signaler auprès de leur cadre et de l’équipe opérationnelle d’hygiène (EOH) de leur hôpital, porter un masque chirurgical en permanence et le changer toutes les quatre heures, et s’auto-surveiller (prise de température deux fois par jour et identification de tout symptôme). En cas de symptômes, même de faible intensité, l’éviction professionnelle doit être immédiate et un prélèvement à visée diagnostique sera réalisé rapidement et prioritairement.
2/ Il est recommandé à tous les personnels d’adopter des gestes simples mais efficaces pour prévenir les transmissions :
● Se désinfecter très régulièrement les mains (notamment avant ou après chaque contact avec une autre personne) ;
● Ne pas se serrer la main, ne pas s’embrasser ;
● Éviter de porter les mains à son visage ;
● Tousser ou éternuer dans son coude ;
● Utiliser un mouchoir à usage unique et le jeter.3/ Les personnels d’accueil en contact direct et rapproché des patients doivent porter un masque chirurgical en continu à changer toutes les 4 heures (entrée de l’hôpital, services d’urgences… ).
Pour les personnels qui ont une pathologie chronique (transplantation pulmonaire, immunodépression…), l’indication de porter un masque chirurgical en continu est à poser en lien avec le service de santé au travail.
Les masques filtrants FFP2 doivent être portés systématiquement par les soignants prenant en charge les patients COVID-19 confirmés ou les cas possibles très symptomatiques. Ces masques restent indiqués pour tous les patients contagieux nécessitant des précautions complémentaires « air » (tuberculose, rougeole…).
Le reste de la population ne doit pas porter de masque.
4/ Les patients positifs au COVID-19 de notre région ne présentant pas de critère de gravité pourront désormais être pris en charge en ambulatoire si leur état de santé le permet. Ils bénéficieront d’un dispositif d’accompagnement pour leur retour à domicile.
5/ Les indications de recherche de COVID-19 par PCR sont posées par les infectiologues selon les définitions des cas mises à jour par Santé Publique France. En cas d’augmentation des besoins de diagnostic, une priorisation des besoins sera effectuée afin de toujours rendre rapidement les résultats nécessaires pour la protection des patients, de leurs proches et des soignants.
6/ Les consignes relatives aux cas groupés (clusters) s’appliquent nationalement.
Afin de lutter contre l’extension de l’épidémie et d’éviter les cas nosocomiaux, votre vigilance est rappelée sur l’importance de repérer dans les délais les plus brefs les situations de découvertes fortuites de cas COVID-19.
7/ Consignes relatives aux personnes revenant de zones de circulation du virus.
Le passage du stade 1 au stade 2 justifie :
● L’abandon de la règle du maintien en « quatorzaine » à domicile pour les personnes revenant des zones de circulation virale à l’étranger. Les soignants revenant de ces zones doivent porter un masque chirurgical en continu à changer toutes les quatre heures. Ils sont invités à limiter leur vie sociale et à s’auto-surveiller (prise de température et apparition éventuelle de symptômes deux fois par jour). Les enfants peuvent être scolarisés.
● Une consigne d’éviter les voyages dans les zones où circule le virus hors de l’Union européenne ou dans les zones à risques en Europe (identifiées sur le site du ministère de l’Europe et des Affaires étrangères), sauf nécessité avérée.
— -
COVID-19. En finir avec les idées reçues
source : OMS 2020
IDÉE REÇUE : Le nouveau coronavirus (2019-nCoV) peut être transmis par les piqûres de moustiques
FAIT ÉTABLI : Le nouveau coronavirus NE peut PAS être transmis par les piqûres de moustiques.
Le nouveau coronavirus est un virus respiratoire qui se propage essentiellement par contact avec une personne infectée, par l’intermédiaire des gouttelettes respiratoires émises lorsqu’une personne, par exemple, tousse ou éternue, ou par l’intermédiaire des gouttelettes de salive ou de sécrétions nasales. À ce jour, il n’existe aucune information ni aucun élément de preuve laissant penser que le 2019-nCov pourrait être transmis par les moustiques. Pour vous protéger, évitez tout contact rapproché avec une personne qui a de la fièvre ou qui tousse, et pratiquez les bons gestes d’hygiène des mains et d’hygiène respiratoire.
IDÉE REÇUE : L’urine des enfants peut protéger contre le nouveau coronavirus (2019-nCoV)
FAIT ÉTABLI : L’urine des enfants NE peut PAS protéger contre le nouveau coronavirus.
L’urine ne tue pas les virus et les bactéries. En fait, l’urine peut contenir des petites quantités de matériel viral ou bactérien. Vous laver les mains avec l’urine d’un enfant ou utiliser cette urine pour frotter les surfaces ne vous protègera pas contre le nouveau coronavirus (2019-nCoV). Nettoyez-vous souvent les mains avec un produit hydroalcoolique ou à l’eau et au savon. Nettoyez les surfaces avec de simples désinfectants ménagers.
IDÉE REÇUE : Le temps froid et la neige peuvent tuer le nouveau coronavirus (2019-nCoV)
FAIT ÉTABLI : Le temps froid et la neige NE peuvent PAS tuer le nouveau coronavirus (2019-nCoV).
La température normale du corps humain reste aux alentours de 36,5 °C et 37 °C, quel que soit la température ou le temps extérieur. Par conséquent, il n’y a aucune raison de croire que le temps froid peut tuer le nouveau coronavirus ou d’autres agents pathogènes. Le moyen le plus efficace pour vous protéger contre le 2019-nCoV est de vous nettoyer fréquemment les mains avec un produit hydroalcoolique ou à l’eau et au savon.
IDÉE REÇUE : La cocaïne peut protéger contre le nouveau coronavirus (2019-nCoV)
FAIT ÉTABLI : La cocaïne NE protège PAS contre le nouveau coronavirus et peut être dangereuse.
La cocaïne est une drogue stimulante addictive. Son usage provoque de graves effets indésirables et est nocif pour la santé des personnes.
IDÉE REÇUE : Le nouveau coronavirus (2019-nCoV) peut être transmis par des objets, tels que les pièces et les billets de banque
FAIT ÉTABLI : Le risque d’être infecté par le nouveau coronavirus (2019-nCoV) en touchant des objets, notamment des pièces de monnaie, des billets de banque ou des cartes de crédit, est très faible.
Des données préliminaires indiquent que le nouveau coronavirus (2019-nCoV) peut survivre sur des surfaces pendant quelques heures ou plus. Il peut arriver qu’un objet soit contaminé par le 2019-nCoV par une personne infectée qui tousse ou éternue ou qui touche l’objet. Avec une bonne hygiène des mains, le risque d’être infecté par le nouveau coronavirus (2019-nCoV) en touchant des objets, notamment des pièces de monnaie, des billets de banque ou des cartes de crédit, est très faible. La meilleure protection consiste à se nettoyer fréquemment les mains avec un produit hydroalcoolique ou à l’eau et au savon.
IDÉE REÇUE : Le nouveau coronavirus (2019-nCoV) peut se projeter jusqu’à 8 mètres d’une personne qui tousse ou éternue
FAIT ÉTABLI : Les gouttelettes respiratoires se projettent à 1 mètre au maximum d’une personne qui tousse ou éternue.
Lorsqu’une personne infectée par le 2019-nCoV tousse ou éternue, le virus est expulsé dans les gouttelettes qui peuvent parcourir une certaine distance à partir de cette personne. Par conséquent, pour vous protéger de n’importe quel virus respiratoire, évitez tout contact rapproché avec une personne qui a de la fièvre ou qui tousse, et nettoyez-vous fréquemment les mains avec un produit hydroalcoolique ou à l’eau et au savon.
IDÉE REÇUE : Le nouveau coronavirus (2019-nCoV) peut se propager sur de longues distances dans l’air
FAIT ÉTABLI : Les coronavirus sont des virus qui NE se propagent PAS sur de longues distances dans l’air.
Le nouveau coronavirus (2019-nCoV) est un virus respiratoire qui se propage essentiellement par l’intermédiaire des gouttelettes émises lorsqu’une personne infectée tousse ou éternue, ou par l’intermédiaire des gouttelettes de salive ou de sécrétions nasales. Ces gouttelettes sont trop lourdes pour voyager loin. Une infection pourrait également se déclarer si vous vous touchez les yeux, la bouche, ou le nez après avoir été en contact avec une surface contaminée. Protégez-vous en vous nettoyant les mains fréquemment avec un produit hydroalcoolique ou à l’eau et au savon.
- Les sèche-mains sont-ils efficaces pour tuer le nCoV 2019 ?
Non. Les sèche-mains ne sont pas efficaces pour tuer le 2019-nCoV. Pour vous protéger contre le nouveau coronavirus, vous devez vous nettoyer fréquemment les mains avec un produit hydroalcoolique ou à l’eau et au savon. Une fois que vos mains sont propres, vous devez les sécher soigneusement à l’aide de serviettes en papier ou d’un séchoir à air chaud.
- Puis-je réutiliser un masque N95 ? Puis-je le laver ? Puis-je le stériliser avec des désinfectants pour les mains ?
Non. Les masques faciaux, y compris les masques médicaux plats ou les masques N95, ne doivent pas être réutilisés. Si vous avez été en contact étroit avec une personne infectée par le nouveau coronavirus ou qui présente une autre infection respiratoire, le devant de votre masque doit être considéré comme contaminé. Vous devez enlever le masque sans toucher sa partie avant et le jeter de manière appropriée. Après avoir enlevé votre masque, vous devez vous nettoyer les mains avec un produit hydroalcoolique ou à l’eau et au savon.
- Une lampe de désinfection à ultraviolets (UV) peut-elle tuer le nouveau coronavirus (nCoV) ?
Les lampes à UV ne doivent pas être utilisées pour se stériliser les mains ou d’autres parties du corps, car les rayons UV peuvent provoquer des érythèmes (irritation de la peau).
Pour vous protéger contre le nouveau coronavirus, tenez-vous au courant de toutes les mesures que vous pouvez adopter. Pour plus de détails, voir le site Web de l’OMS : https://www.who.int/fr/emergencies/diseases/novel-coronavirus-2019/advice-for-public
- La pulvérisation d’alcool ou de chlore sur tout le corps peut-elle tuer le nouveau coronavirus (nCoV) ?
Non. Vaporiser de l’alcool ou du chlore sur tout le corps ne tuera pas les virus qui ont déjà pénétré dans votre corps. La pulvérisation de ces substances peut être nocive pour les vêtements ou les muqueuses (c’est-à-dire les yeux, la bouche). Sachez que l’alcool et le chlore peuvent tous deux être utiles pour désinfecter les surfaces, mais ils doivent être utilisés en suivant les recommandations appropriées.
Il existe plusieurs mesures que vous pouvez adopter pour vous protéger contre le nouveau coronavirus. Commencez par vous nettoyer fréquemment les mains en utilisant un produit hydroalcoolique – comme un gel – ou à l’eau et au savon. Pour connaître les autres mesures
- Est-il sans danger de recevoir une lettre ou un colis de Chine ?
Oui, c’est sans danger. Les personnes qui reçoivent des colis en provenance de Chine ne risquent pas de contracter le nouveau coronavirus. D’après des analyses antérieures, nous savons que les coronavirus ne survivent pas longtemps sur des objets, tels que des lettres ou des colis.
Les animaux domestiques peuvent-ils propager le nouveau coronavirus (2019-nCoV) ?
À l’heure actuelle, rien ne prouve que les animaux de compagnie/animaux domestiques tels que les chiens ou les chats peuvent être infectés par le nouveau coronavirus. Toutefois, il est toujours bon de se laver les mains à l’eau et au savon après un contact avec des animaux domestiques. Cela vous protège contre diverses bactéries courantes comme E.coli et Salmonella qui peuvent passer des animaux de compagnie à l’homme.
- Les vaccins contre la pneumonie protègent-ils contre le nouveau coronavirus ?
Non. Les vaccins contre la pneumonie, tels que le vaccin antipneumococcique et le vaccin contre Haemophilus influenza type B (Hib), n’offrent pas de protection contre le nouveau coronavirus.
Le virus est tellement nouveau et différent qu’il nécessite un vaccin qui lui est propre. Les chercheurs sont en train de travailler à la mise au point d’un vaccin contre le 2019-nCoV et l’OMS les soutient dans leurs travaux.
Bien que ces vaccins ne soient pas efficaces contre le 2019-nCoV, la vaccination contre les maladies respiratoires est fortement recommandée pour protéger votre santé.
- Se rincer régulièrement le nez avec une solution saline peut-il aider à prévenir l’infection par le nouveau coronavirus ?
Non. Rien ne prouve que le fait de se rincer régulièrement le nez avec une solution saline protège les gens contre l’infection par le nouveau coronavirus.
Il existe quelques éléments probants indiquant que cette pratique peut aider les gens à se remettre plus rapidement d’un rhume ordinaire. Cependant, il n’a pas été démontré que le fait de se rincer régulièrement le nez permettait de prévenir les infections respiratoires
Manger de l’ail peut-il aider à prévenir l’infection par le nouveau coronavirus ?
L’ail est un aliment sain qui peut avoir certaines propriétés antimicrobiennes. Cependant, rien ne prouve, dans le cadre de l’épidémie actuelle, que la consommation d’ail protège les gens contre le nouveau coronavirus.
- Le fait de mettre de l’huile de sésame empêche-t-il le nouveau coronavirus de pénétrer dans l’organisme ?
Non. L’huile de sésame ne tue pas le nouveau coronavirus. Il existe des désinfectants chimiques qui peuvent tuer le 2019-nCoV sur les surfaces. Il s’agit notamment de désinfectants à base d’eau de Javel ou de chlore, de solvants, d’éthanol à 75%, d’acide peracétique et de chloroforme.
Cependant, ils ont peu d’impact sinon aucun sur le virus si vous les mettez sur la peau ou sous votre nez. Il peut même être dangereux de se mettre ces produits chimiques sur la peau..
- Le nouveau coronavirus affecte-t-il les personnes âgées ou les jeunes y sont-ils également sensibles ?
Les personnes de tous âges peuvent être infectées par le nouveau coronavirus (2019-nCoV). Les personnes âgées et les personnes souffrant de maladies préexistantes (comme l’asthme, le diabète, les maladies cardiaques) semblent plus susceptibles de tomber gravement malades à cause de ce virus.
L’OMS conseille aux personnes de tous âges de prendre des mesures pour se protéger du virus, par exemple en suivant une bonne hygiène des mains et une bonne hygiène respiratoire.
- Les antibiotiques sont-ils efficaces pour prévenir et traiter l’infection par le nouveau coronavirus ?
-
Non, les antibiotiques n’agissent pas contre les virus, mais seulement contre les bactéries.
Le nouveau coronavirus (2019-nCoV) est un virus et, par conséquent, les antibiotiques ne doivent pas être utilisés comme moyen de prévention ou de traitement.
Cependant, si vous êtes hospitalisé pour une infection par le 2019-nCoV, vous pouvez recevoir des antibiotiques car une co-infection bactérienne est possible.
- Existe-t-il des médicaments spécifiques pour prévenir ou traiter l’infection par le nouveau coronavirus ?
À ce jour, aucun médicament spécifique n’est recommandé pour prévenir ou traiter l’infection par le nouveau coronavirus (2019-nCoV).
Toutefois, les personnes infectées par le virus doivent recevoir des soins appropriés pour soulager et traiter les symptômes, et celles qui sont gravement malades doivent recevoir des soins de soutien optimisés. Certains traitements spécifiques sont à l’étude et seront testés dans le cadre d’essais cliniques. L’OMS contribue à accélérer les efforts de recherche et de développement avec toute une série de partenaires.
Covid-19 chez une femme enceinte, que fait-on ?
Publié le 13/03/2020
Avant que soient publiées des recommandations officielles et alors que les données concernant l’infection à Covid-19 chez la femme enceinte sont encore limitées, une équipe médicale de l’hôpital universitaire de Lausanne (Suisse) propose dans le Lancet Infectious Diseases un algorithme et des recommandations pour la prise en charge des femmes enceintes.
Si une femme enceinte a voyagé dans les deux semaines précédentes dans une région où sévit l’infection à Covid-19, ou si elle a été en contact rapproché avec une personne pour laquelle l’infection a été confirmée, elle doit être testée même si elle est asymptomatique.
Une femme enceinte asymptomatique testée positive au Covid-19 doit rester confinée à son domicile et se surveiller pendant au moins 14 jours. Ces femmes enceintes et celles qui sont guéries d’une infection à Covid-19 légère doivent bénéficier d’une surveillance échographique et doppler bimensuelle de la croissance fœtale, compte-tenu de la suspicion d’un risque de retard de croissance intra-utérin.
Une femme enceinte atteinte d’une pneumonie à Covid-19 doit être prise en charge par une équipe multidisciplinaire dans une unité de soins spécialisés.
Pour une femme enceinte chez qui l’infection à Covid-19 a été confirmée, la date de l’accouchement doit être déterminée en fonction du terme, de l’état de santé maternel, de celui du fœtus, et des conditions de l’accouchement. On préfèrera, si possible, un accouchement par voie basse, après un déclenchement du travail, et une éventuelle extraction instrumentale pour éviter l’épuisement maternel.
Les nouveau-nés des mères infectées par le Covid-19 doivent être isolés pendant au moins 14 jours ou jusqu’à la disparition du portage viral. L’allaitement "direct" n’est pas recommandé durant cette période.
Ces recommandations doivent être adaptées aux conditions médicales locales, et peuvent évoluer au fur et à mesure de l’acquisition de données nouvelles.
Dr Catherine Vicariot
Référence
Favre G et coll. : Guidelines for pregnant women with suspected SARS-CoV-2 infection. Lancet infect dis., 2020 ; publication avancée en ligne le 3 mars. doi.org/10.1016/S1473-3099(20)30157-2
Source : jim.fr
Équipements de protection individuelle
Protections contre les risques biologiques
En milieu de travail, la transmission des agents biologiques à l’homme peut se faire par inhalation, par contact avec la peau ou les muqueuses, par inoculation (blessure, morsure, piqûre d’insecte) ou par ingestion (mains contaminées portées à la bouche).
Les mesures d’élimination du danger et de protection collective sont à envisager en premier lieu. L’utilisation des équipements de protection individuelle (EPI) ne doit être envisagée qu’en complément. C’est à partir de l’évaluation des risques menée dans l’entreprise que doit être engagée la réflexion relative à l’utilisation des EPI.
Selon les expositions et les modes de transmission des agents biologiques, les opérateurs peuvent se protéger en portant notamment des gants, des vêtements de protection, des appareils de protection respiratoire (APR), des lunettes-masques ou des visières.
Gants de protection
Avant de choisir un modèle de gant, il convient d’analyser l’activité de travail pour évaluer les risques et les contraintes des tâches à effectuer.
Tout gant étanche convient pour protéger contre un risque biologique. Les gants de protection microbiologique répondent à la norme NF EN 374. Il existe des gants fins à usage unique, à réserver aux situations de travail exigeant une grande dextérité (travail en laboratoire, soins à des patients…) et des gants plus épais, nécessaires lorsqu’il existe un risque de blessure (travail en station d’épuration, sur des installations industrielles, opérations de nettoyage…).
Dans tous les cas, les gants doivent être enfilés sur des mains propres, sèches et aux ongles courts.
Les gants à usage unique doivent être changés régulièrement, même s’ils ne paraissent pas détériorés. Dans tous les cas, ils doivent être retirés dès qu’ils sont abîmés.
Les gants doivent être retirés en suivant une séquence de gestes précis, de façon à éviter de se contaminer. Un lavage des mains est ensuite indispensable.
Gants et métiers de la santé
Dans les milieux de soins, le port de gants fait partie des précautions « standard » ou précautions universelles pour la prévention de la transmission croisée soignant/soigné. Les gants médicaux répondent à la norme NF EN 455. Le port de gants est indispensable :
- Si l’opérateur risque d’entrer en contact avec les muqueuses ou la peau lésée d’un patient, avec du sang ou tout autre produit d’origine humaine, par exemple lors d’un prélèvement sanguin ou lors de la manipulation de tubes ou de flacons de prélèvements biologiques, de linge ou de matériel souillé ;
- en cas de lésion cutanée des mains de l’opérateur.
Certaines situations peuvent nécessiter des précautions complémentaires :
- port de deux paires de gants, notamment pour les chirurgiens au bloc opératoire ou pour le travail avec des patients très contagieux par contact.
- port de sous-gants résistants aux coupures, pour les gestes particulièrement à risque, notamment en anatomo-pathologie.
Les gants doivent être changés entre deux patients ou deux activités.
Protection du visage
Les muqueuses oculaire, nasale et buccale constituent des portes d’entrée particulièrement vulnérables aux agents biologiques.
En fonction de l’évaluation des risques, différents équipements de protection peuvent être utilisés :
- Les lunettes et lunettes-masques (conformes à la norme NF EN 166) protègent uniquement les yeux. Les lunettes-masques qui s’ajustent parfaitement au visage sont étanches.
- Les écrans faciaux (conformes à la norme NF EN 166) protègent tout le visage et ont l’avantage de pouvoir être retirés en minimisant le risque de toucher le visage.
En milieu de soins, les masques chirurgicaux (conformes à la norme EN 14683) protègent contre les gouttelettes émises par un patient. Lorsqu’ils sont marqués de la lettre R, ils sont résistants aux projections de liquides biologiques (sang…).
Vêtements de protection
Le choix d’un vêtement de protection doit prendre en compte :
- le type d’exposition (aérosols de poussières ou de liquides pulvérisés, jets de liquide sous pression, contact avec des surfaces contaminées…),
- la charge physique,
- la durée de la tâche.
La norme européenne NF EN 14126 « Vêtements de protection - Exigences de performances et méthodes d’essai pour les vêtements de protection contre les agents infectieux » définit 6 types de vêtements de protection, du type 1B (protection la plus complète) au type 6B. Selon cette norme, un vêtement de type 5 B est destiné à la protection contre les poussières, un vêtement 4 B protège contre des pulvérisations de liquide et un vêtement de type 3 B protège contre des jets de liquides. Dans certaines situations de travail, des EPI ne protégeant qu’une partie du corps peuvent être utilisés (tabliers, manchettes…).
En milieu de soins, les casaques chirurgicales protègent contre la contamination croisée entre patient et soignant. Elles sont définies dans la série des normes NF EN 13795, qui les évaluent selon la performance des matériaux et la protection des zones critiques.
Appareils de protection des voies respiratoires
L’utilisation d’un appareil de protection respiratoire (APR) est destinée à prévenir l’inhalation d’agents biologiques. Ce risque peut se présenter dans différents secteurs professionnels (secteur de l’assainissement, secteur de la santé…).
Les APR filtrants anti-aérosols conviennent pour la plupart des situations de travail exposant à un risque biologique par inhalation. Dans cette catégorie d’APR, on trouve :
- les pièces faciales filtrantes à usage unique FFP1, FFP2 et FFP3 (ED 105),
- les appareils réutilisables constitués d’une pièce faciale (demi-masque, masque, cagoule) munie d’une cartouche filtrante P1, P2 ou P3 (ED 6106). Les APR à ventilation assistée assurent une plus grande protection ainsi qu’un plus grand confort, en particulier pour un port prolongé.
Il est indispensable que l’utilisateur ajuste correctement son APR pour être protégé : la présence de fuites au visage rend la protection inopérante.
Le choix de l’APR déterminera le choix des éventuels autres EPI comme les lunettes-masques, les écrans faciaux, afin qu’ils puissent être portés ensemble en assurant une bonne protection. Lorsque les APR sont portés en même temps que d’autres EPI, une séquence de gestes doit être respectée pour éviter de se contaminer lors du retrait de l’ensemble de la tenue de protection.
Dans le milieu de la santé, des APR seront utilisés lors de la prise en charge de patients atteints d’infections transmissibles par air (exemple : tuberculose) ou lors de certains actes médicaux (endoscopies bronchiques, chirurgie au laser…). Les masques chirurgicaux (conformes à la norme EN 14683) ne sont pas des APR ; ils sont utilisés pour protéger contre les gouttelettes émises par un patient.
source : inrs.fr
Facteurs pronostiques du Covid-19, les leçons de Wuhan
Publié le 12/03/2020
La pandémie de Covid-19 est à l’origine d’une croissance exponentielle du nombre de publications qui lui sont consacrées, ce qui ne saurait surprendre face à la tournure des évènements. Parmi celles-ci, il en est une qui retient l’attention même si elle est le fruit d’une étude rétrospective. Pour plusieurs raisons : en premier lieu, elle relate l’évolution clinique de 191 patients tous hospitalisés à Wuhan, l’épicentre de l’épidémie chinoise par laquelle tout a commencé en décembre 2019. Par ailleurs, il y est question de mortalité et de facteurs pronostiques, ce qui ne saurait laisser indifférent à l’heure où l’Italie se débat avec courage dans une situation épidémique préoccupante…qui fait trembler les autres pays. Enfin, même s’il faut intégrer les résultats dans le contexte en tenant compte du lieu géographique et des caractéristiques initiales de l’épidémie, il n’en reste pas moins qu’ils demeurent d’actualité et seront utiles aux cliniciens.
L’étude de cohorte en question qui est transversale et multicentrique a inclus tous les patients adultes (≥18 ans) admis dans les hôpitaux de Jinyintan (n=135) et Wuhan (n=56) avec le diagnostic de Covid-19 confirmé par les tests biologiques (détection obligatoire de l’ARN viral par PCR), sortis de ces hôpitaux ou décédés avant le 31 janvier 2020. Les survivants et les patients décédés ont été comparés dans le but de déterminer les facteurs pronostiques en s’aidant d’analyses univariées et multivariées. Au total, 137 patients ont survécu et ont quitté les services hospitaliers, les 54 autres sont morts pendant l’hospitalisation.
Trois variables pronostiques mais surtout l’âge élevé
Une comorbidité a été identifiée chez 91 patients (48 %) : en tête, hypertension artérielle (30 %) devant diabète (19 %) et maladie coronarienne (15 %).
Une analyse multivariée a révélé que le risque de décès était majoré par les facteurs suivants :
(1) âge avec un odds ratio (OR) de 1,10 (IC95% 1,03–1,17 par année d’âge ; p = 0,0043) ;
(2) score d’atteinte multiviscérale dit SOFA (Sequential Organ Failure Assessment) (OR = 5,65, IC95 % 2,61–12,23 ; p<0,0001) ;
(3) taux plasmatiques de d-Dimères > 1 μg/l lors de l’admission (OR = 18,42 ; IC 95% 2,64–128,55 ; p = 0,0033).
La durée médiane de l’excrétion virale chez les survivants a été estimée à 20 jours, l’écart interquartile étant de 17,0-24,0 et la valeur maximale de 37 jours. Chez les patients décédés, le SARS-Cov2 a pu être détecté jusqu’au décès.
L’efficacité des traitements utilisés, quels qu’ils soient n’a pu être évaluée compte tenu de l’approche rétrospective, mais leur lourdeur a été associée à une surmortalité, à l’instar de la corticothérapie : c’est la sévérité de l’état clinique qui est derrière ces associations dénuées de toute signification autre que statistique…
Une incitation à prolonger l’isolement
Cette étude chinoise qui porte sur près de 200 cas de Covid-19 hospitalisés dans deux hôpitaux de la province du Hubei avant le 31 janvier attire l’attention sur trois variables pronostiques principales qui, dès le stade précoce de l’infection, font craindre une évolution péjorative : un âge élevé, un score SOFA élevé et des D-dimères au diapason (> 1 μg/l). Le grand perdant est celui qui cumule les facteurs de risque, mais l’âge se suffit à lui-même dans cette étude comme dans d’autres.
Par ailleurs, l’excrétion virale prolongée (médiane : 20 jours, maximale : 37 jours) incite à un isolement dont la durée est conditionnée par la négativation des tests biologiques constatée à deux reprises espacées de 24, voire 48 heures.
Dr Peter Stratford
Référence
Fei Zhou et coll. : Clinical course and risk factors for mortality of adult in patients with COVID-19 in Wuhan, China : aretrospectivecohortstudy. Lancet 2020 : publication avancée en ligne le 9 mars. doi.org/10.1016/ S0140-6736(20)30566-3.
Source : jim.fr
Dans quels prélèvements biologiques se cache le SARS-CoV-2 ?
Publié le 16/03/2020
Le diagnostic positif du Covid-19 repose sur la détection de l’ARN du SARS-CoV-2 par RT-PCR dans les prélèvements effectués au niveau des voies aériennes supérieures, en règle la région nasopharyngée ou encore oropharyngée. Cependant, le virus peut être isolé ailleurs et potentiellement transmissible par d’autres voies ou supports que les classiques gouttelettes de Pflügge, produites au cours des éternuements et de la toux et largement incriminées dans l’épidémie de Covid-19. De fait, la biodistribution de tout agent pathogène varie d’une espèce à l’autre ou d’une famille à l’autre dans le cas des coronavirus.
Une étude transversale publiée en ligne dans le JAMA du 11 mars 2020 sous la forme d’une research letter permet de se faire une idée de la présence du SARS-CoV2 dans les différents compartiments ou fluides de l’organisme. Elle a inclus 205 patients (âge moyen 44 ans ; extrêmes, 5-67 ans ; hommes : 68 %) atteints du Covid-19 admis dans trois hôpitaux chinois entre 1er janvier et le 17 février 2020, situés respectivement dans les provinces de Hubei, Shandong et Pékin. Dans la plupart des cas, des prélèvements pharyngés ont été effectués entre le 1er et le 3ème jour après l’admission. D’autres prélèvements ont porté sur le sang, l’expectoration, les fèces et les urines tout au long de l’évolution de la maladie. Une fibroscopie avec lavage broncho-alvéolaire (+/-biopsie) n’a concerné que les patients atteints d’une pneumonie sévère ou encore ceux mis sous ventilation assistée (soit 19 % de la cohorte). En cas de présence de virus dans les selles, quatre échantillons de ces dernières ont été mis en culture en vue d’une étude par microscopie électronique pour déceler des traces du microorganisme vivant.
Excrétion fécale dans 29 % des cas
Au total, 1 070 échantillons biologiques ont été soumis à une recherche de l’ARN viral par RT-PCR. La positivité de cette dernière a varié selon l’origine du prélèvement. Elle s’est avérée maximale dans le liquide de lavage broncho-alvéolaire (14/15 ; 93 %) cependant rarement effectué (environ 7 % des cas), puis, dans l’ordre, dans :
- (1) l’expectoration (72/104 ; 72 %) ;
- (2) les écouvillonnages nasaux (5/8 ; 63 %) ;
- (3) la biopsie bronchique (6/13 ; 46 %) ;
- (4) les prélèvements pharyngés (126/398 ; 32 %) ;
- (5) les fèces (44/153 ; 29 %) ;
- (6) le sang (3/307 ; 1 %).
Aucun échantillon urinaire ne s’est avéré positif.
Cette petite étude transversale chinoise ne porte que sur un peu plus de 200 patients hospitalisés tous atteints d’un Covid-19 confirmé. C’est dans le liquide de lavage broncho-alvéolaire que l’ARN du virus a été le plus souvent retrouvé, plus de neuf fois sur dix, mais cette procédure n’a été utilisée que dans 7 % des cas. Si les échantillons sanguins ne se sont avérés que très rarement positifs (1 %), tel n’a pas été le cas des échantillons fécaux avec une positivité dans 29 % des cas. La transmission du virus par cette voie extrarespiratoire n’est pas pour autant certaine, mais il y a tout lieu de penser qu’elle est possible : cette hypothèse demande à être confirmée. De quoi justifier les mesures actuelles notamment le lavage fréquent et appuyé des mains à chaque fois que cela s’impose.
La confirmation d’une excrétion fécale du virus vivant ne changerait pas drastiquement la donne actuelle qui est celle d’une crise sanitaire mondiale majeure, mais elle éclairerait l’épidémiologie du Covid-19 et la propagation accélérée du SARS-CoV2, en dépit de la rigueur des mesures sanitaires adoptées désormais par la plupart des pays du Monde.
Dr Philippe Tellier
Référence
Wang W et coll. : Research letter. Detection of SARS-CoV-2 in Different Types of Clinical Specimens. JAMA 2020 : publication avancée en ligne le 11 mars. doi:10.1001/jama.2020.3786.
Source : jim.fr
2019-nCoV : un risque de contamination par des sujets asymptomatiques
Publié le 01/02/2020
L’épidémiologie de l’infection à coronavirus 2019-nCoV, décrite pour la première fois fin décembre 2019, se précise à une vitesse inusitée. Et ceci grâce à la coordination du travail des cliniciens, des biologistes, des virologues et des médecins de santé publique en Chine mais aussi dans le monde entier, sans oublier la réactivité de la presse scientifique qui contribue à la diffusion quasi instantanée de l’information.
Comme toujours avec les affections contagieuses, pour bien évaluer le risque et donc adapter les mesures de lutte et de prévention, il nous faut préciser le plus rapidement possible certains paramètres épidémiologiques essentiels et notamment la nature d’un éventuel réservoir animal de virus, les modes de transmission interhumaine, la durée de la période d’incubation, le niveau et la durée de contagiosité et bien sûr la morbimortalité.
Une publication d’une équipe allemande dans le New England Journal of Medicine, le 30 janvier 2020, apporte des réponses pour 2 de ces paramètres fondamentaux.
4 patients Allemands
Camilla Rothe C et coll. de Munich rapportent dans une lettre à l’éditeur les cas très documentés de 5 malades.
Le patient index est une chinoise de Shanghai ayant séjourné à Munich pour affaires jusqu’au 22 janvier 2020, date de son retour en Chine. Durant son séjour en Allemagne, alors qu’elle était totalement asymptomatique, elle a eu plusieurs réunions de travail du 19 au 22 janvier avec des partenaires commerciaux allemands. Lors du vol de retour vers son pays, des symptômes d’infection respiratoire sont apparus qui ont conduit à la pratique d’une PCR. Celle-ci s’est révélée positive au 2019-nCoV le 27 janvier 2020. Les partenaires commerciaux allemands ont été prévenus immédiatement de cette positivité et une enquête épidémiologique a été diligentée à Munich auprès des sujets contacts à Munich (alors qu’elle était totalement asymptomatique).
Quatre d’entre eux ont présenté des symptômes respiratoires à partir du 24 janvier et se sont révélés être contaminés par 2019-nCoV, PCR à l’appui (avec une charge virale élevée chez le premier patient). Ces 4 malades allemands ont été hospitalisés à Munich et isolés pour rompre la chaine de transmission. A la date de publication de cette lettre ils ne présentaient pas de signes de gravité.
Des conséquences pour la lutte contre l’épidémie
Il est à noter que deux de ces 4 patients n’avaient eu aucun contact avec la malade index chinoise ce qui signifie qu’ils ont dû être contaminés par un des cas contacts allemands en début de période d’incubation.
Il est donc démontré, premièrement, que des sujets asymptomatiques peuvent être contagieux durant la phase d’incubation, même à son début, ce qui devrait peut-être conduire à revoir nos modèles de propagation de l’épidémie et les mesures de protection nécessaires.
De plus, deuxièmement, la mise en évidence d’une charge virale élevée chez un de ces malades lors de sa convalescence laisse penser que l’excrétion virale, et donc possiblement la contagiosité, peut se prolonger au-delà de la guérison clinique. Pour confirmer ce phénomène inquiétant on doit toutefois attendre les résultats des cultures virales chez ce malade pour s’assurer que le virus détecté par PCR était viable.
Dr Nicolas Chabert
Références
Rothe C et coll. : Transmission of 2019-nCoV infection from an asymptomatic contact in Germany. N Engl J Med 2020 ; Publication avancée en ligne le 30 janvier 2020.
Source : jim.fr
Le « nouveau coronavirus » (NCoV) est une souche jamais encore détectée chez l’homme avant les premiers cas confirmés par l’OMS en 2012. Bien que le nouveau coronavirus soit génétiquement assez différent du virus à l’origine du SRAS selon l’OMS, celui-ci est particulièrement grave : 16 cas mortels sur 34 cas recensés ont été rapportés au 20 Mai 2013.
- Caractéristiques du coronavirus
Le coronavirus est un virus à ARN ayant un taux de mutation élevé comme celui de la grippe ou du virus HIV. Les coronavirus se retrouvent dans de très nombreuses espèces animales et circulent facilement d’une espèce à l’autre pouvant entrainer la mort.
Les coronavirus peuvent aussi infecter les hommes et provoquer des manifestations banales comme des rhumes.
En 2011, des chercheurs ont émis l’hypothèse que le nouveau coronavirus, nCOV, présent dans la Péninsule arabique n’a pas provoqué de manifestations chez l’homme mais a permis sa contamination auprès d’animaux le rendant l’année suivante très dangereux et potentiellement mortel pour les êtres humains.
- Provenance
La majorité des personnes infectées ont voyagé dans la péninsule arabique ou y résidaient. Le patient qui a été admis en réanimation à Lille le 12 Mai 2013 a séjourné dans la même chambre qu’un patient infecté par le coronavirus et qui avait séjourné à Dubai.
- Quand apparaissent les premiers symptômes ?
10 jours environ séparent la durée d’incubation du virus de l’apparition des premières manifestations.
La personne infectée semble être contagieuse lorsqu’elle présente ses premiers symptômes.
Propagation
Le coronavirus se transmet d’homme à homme, lors de contacts rapprochés et étroits avec une personne présentant les manifestations respiratoires du virus, à moins d’un mètre, et probablement par voie aérienne lors d’épisodes de toux ou de postillons par exemple.
Le contact avec des animaux infectés, situation possible dans les pays de la péninsule arabique, représente un risque de contagion.
Il semble que les hommes soient plus touchés par ce virus.
Les décès constatés semblent survenir davantage chez des personnes immunodéprimées.
Traitement et vaccin
Aucun traitement ni vaccin n’est disponible à la date du 12 mai 2013.
Le transfert dans un service de réanimation s’impose en cas d’aggravation des manifestations.
Protection
Le lavage régulier des mains ainsi que le port de masques peut permettre d’enrayer la propagation du virus.
Dispositif de surveillance
L’Institut de Veille Sanitaire, l’INVS, a mis en place un dispositif de surveillance depuis le 7 décembre 2012 et le Haut Conseil de la Santé publique a émis, le 19 mars 2013, un avis relatif à la prise en charge des patients suspects d’infections provoquées par ce nouveau coronavirus.
L’Organisation Mondiale de la Santé (OMS) et l’European Centre for Divease Prevention and Control (ECDC) ont mis en place une surveillance.
Un numéro vert d’information , 0 800 13 00 00, est disponible du Lundi au Samedi de 9 h à 19 h.
Le Haut Conseil de la santé publique (HCSP) a publié en mars 2013 un avis relatif à la prise en charge des patients suspects d’infections dues au nouveau coronavirus (HcoV-EMC, ou NCoV). Ce document fournit des recommandations aux professionnels de santé sur les conduites à tenir devant des cas possibles ou confirmés de patients infectés par le NcoV, de la démarche diagnostique aux modalités de prise en charge de ces patients à l’hôpital.
Le HCSP précise que les conduites à tenir détaillées dans cet avis sont susceptibles d’évoluer rapidement avec la connaissance de ce nouveau virus.
La menace : agent pathogène et pathologie
Agent pathogène
Le HCSP donne les précisions suivantes concernant la nature et les caractéristiques de l’infection due au nouveau coronavirus :
Maladie due à un virus à ARN de la famille des Coronaviridae, proche du coronavirus du SRAS.
Désignation : HcoV-EMC (Human Coronavirus - Erasmus Medical Center), ou NCoV (Novel Coronavirus).
Il diffère des quatre autres coronavirus respiratoires endémiques connus chez l’homme : il n’est pas détecté par les trousses de PCR multiplex utilisées au laboratoire de virologie.
Transmission interhumaine fortement suspectée (NDLR : suspicion corroborée par l’Institut National de veille Sanitaire), réservoir animal évoqué (ex : chauve-souris).
- Situation épidémiologique
extrait d’un bulletin publié par l’Institut National de Veille Sanitaire.
- Au 13 mai 2013 : majorité des cas identifiés dans la péninsule arabique et 8 cas identifiés en Europe : dont 2 en France.
- 34 cas d’infection au nouveau coronavirus ont été rapportés dans le monde depuis avril 2012, 20 décès.
- La plupart des patients ont voyagé dans la péninsule arabique.
- Transmission
Selon le HCSP :
Contamination interhumaine mise en évidence,
transmission par voie aérienne et par contact envisagée
- Pathologie
Pneumonies graves, parfois associées à une insuffisance rénale aiguë.
- Diagnostic
Cas possible
Le HCSP définit les cas possibles de patients infectés par le nouveau coronavirus selon les critères suivants :
Patient, qui dans une délai de 10 jours consécutif à un séjour dans certains pays (liste des pays concernés plus bas), présente :
– des signes cliniques et/ou radiologiques de détresse respiratoire aiguë, ou d’infection du parenchyme pulmonaire (fièvre ?38°C et toux),
– sans autre étiologie pouvant expliquer la pathologie.
Tout contact (ex. famille, soignants) d’un cas possible ou confirmé, ayant présenté une infection respiratoire aiguë, dans les 10 jours suivant le dernier contact avec le cas possible/confirmé pendant que ce dernier était symptomatique.
Pays concernés : Arabie Saoudite, Bahreïn, Emirats Arabes Unis, Irak, Iran, Israël, Jordanie, Koweït, Liban, Oman, Qatar, Syrie, Territoires palestiniens occupés, Yémen
- Cas confirmés
Les cas possibles sont confirmés après prélèvements respiratoires indiquant la présence du nouveau coronavirus.
- Prise en charge
- Hospitalisation et suivi de tout patient confirmé ou classé possible (en lien avec l’InVS),
- information des contacts de cas confirmés (même asymptomatiques) et de leur médecin traitant,
- se référer à la procédure SRAS, et à la procédure standardisée validée en 2010 par le COREB (voir annexes 6 et 7 du document).
- Organisation de la prise en charge des cas suspects
Précautions complémentaires d’hygiène (mesures d’isolement) dès la suspicion du cas, organiser directement la prise en charge d’un patient contactant le centre 15 ou son médecin traitant (afin d’éviter le contact avec d’autres patients, ne pas l’orienter d’emblée vers les secteurs d’accueil des urgences).
- Mesures d’isolement des cas possibles et confirmés, protection de l’entourage
Elles associent :
- Les précautions complémentaires de type « Air » et
- les précautions complémentaires de type « Contact ».
- Dans le détail :
Hospitalisation en chambre individuelle, avec un renouvellement correct de son air (6 à 12 volumes/h sans recyclage. Si disponible : en chambre à pression d’air négative, et si possible, avec sas (pour l’habillage ou déshabillage du personnel soignant)
Professionnels de santé et visiteurs,
– Port d’une surblouse à usage unique (avec un tablier plastique en cas de soins à risque d’être mouillant ou souillant)
– Port de gants non stériles à usage unique
– Port d’un masque de protection respiratoire de type FFP2
– Port de lunettes de protection (soin exposant)
– Réalisation d’un geste d’hygiène des mains par friction avec un soluté hydroalcoolique (SHA) dès le retrait des gants et avant de quitter la chambre.
Patient (si déplacement hors de la chambre indispensable, ex :dans le cadre de la réalisation d’un examen complémentaire) :
– Port de masque chirurgical
– Désinfection des mains avec une solution hydroalcoolique
Dépôt du matériel potentiellement contaminant dans les récipients prévus à cet effet. Élimination suivant la filière des déchets d’activité de soins à risque infectieux (DASRI).
Pour entrer dans la chambre et réaliser un soin
Démarche détaillée en page 3 du document
En quittant le malade
Démarche détaillée en page 4 du document
Confirmation du diagnostic microbiologique
Selon le HCSP :
Avant la réalisation des prélèvements ou un examen clinique : le soignant doit assurer sa protection en respectant l’association de précautions complémentaires de type « Air » et de type « Contact »
Traitement
D’après les indication du HCSP, il comprend :
- traitement symptomatique de la détresse respiratoire,
- traitement de l’insuffisance rénale éventuellement associée,
Il n’existe pas de traitement antiviral spécifique.
Désinfection des matériels
Le coronavirus est sensible à l’hypochlorite de sodium (eau de Javel) à 0,1 %, aux composés organochlorés à 0,1 %, aux iodophores à 10 %, à l’éthanol à 70 % et au glutaraldéhyde à 2 %, il est résistant aux composés d’ammonium quaternaire à 0,04 % et aux dérivés phénoliques.
Signalement - Déclaration
Le HCSP indique que tout cas suspect doit être déclaré sans délai à :
l’ARS de la région où il a été identifié, via la plateforme régionale de recueil des signalements, et l’InVS par courriel (alerte@invs.sante.fr) ou par téléphone (astreinte 24h/24) : 08 20 42 67 15. Le classement en cas possible sera alors fait par l’InVS en lien avec le clinicien déclarant.
source :
– OMS
– InVs
– HCSP
– sante-medecine.net
En savoir encore plus sur CORONAVIRIDAE - LES CORONAVIRUS
Pour les passionnés, le laboratoire classé P4 Jean Mérieux INSERM
Ci-dessous la liste des villes où sont implantés ces laboratoires P4 dans le monde.
- Afrique du Sud – Johannesburg – National Institute for Communicable Diseases
- Allemagne – Berlin – Institut Robert Koch
- Allemagne – Hambourg – Bernhard Nocht Institute for Tropical Medicine
- Allemagne -Île Riems -Institut Friedrich Loeffler
- Allemagne -Marburg -Hesse Université de Marbourg, Institut de Virologie
- Australie -Geelong -Victoria Australian Animal Health Laboratory
- Australie -Brisbane - Queensland Queensland Health Forensic and Scientific Services
- Australie -Melbourne -Victoria Victoria Infectious Diseases Reference Laboratory (VIDRL)
- Australie -Sydney -New South Wales Centre for Infectious Diseases and Microbiology Laboratory Service (CIDMLS) et The Institute for Clinical Pathology and Medical Research (ICPMR)
- Canada -Winnipeg -Manitoba Laboratory Centre for Disease Control, National Microbiology Laboratory
- États-Unis -Atlanta - Georgia Centres pour le contrôle et la prévention des maladies (CDC)
- États-Unis -Atlanta - Georgia Center for Biotechnology and Drug Design, Georgia State University
- États-Unis -Fort Detrick -Maryland U.S. Army Medical Research Institute of Infectious Diseases (USAMRIID)
- États-Unis - Galveston -Texas Center for Biodefense and Emerging Infectious Diseases, University of Texas Medical Branch
- États-Unis - Hamilton - Montana NIAID Rocky Mountain Laboratories
- États-Unis - San Antonio - Texas Southwest Foundation for Biomedical Research
- France - Gerland - Lyon P4 Jean Mérieux, INSERM
- Gabon - Franceville - Centre International de Recherches Médicales de Franceville (CIRMF)
- Italie – Rome - Lazzaro Spallanzani Hospital, National Institute of Infectious Diseases
- Royaume-Uni – Londres - Angleterre Centre for Infections, Health Protection Agency
- Royaume-Uni – Salisbury – Angleterre Centre for Emergency Preparedness and Response, Health Protection Agency
- Russie – Koltsovo – Novosibirsk Centre de recherches d’état de virologie et de biotechnologie VECTEUR
- Russie – Kirov – Kirov Institute of Microbiology, Russian Ministry of Defense
- Russie – Sergiyev Posad – Moscou Virological Center of the Institute of Microbiology, Russian Ministry of Defense
- Suède – Solna – Stockholm Swedish Institute for Communicable Disease Control
- Suisse – Genève – Hôpitaux Universitaires de Genève
- Suisse – Spiez – Office fédéral de la protection de la population
- Taïwan Kwen-yang Laboratory Center of Disease Control
- Taïwan Preventive Medical Institute of ROC Ministry of National Defense
SARS-CoV-2, le spectre de la mutation
Publié le 09/03/2020
Le coronavirus du Covid-19, désormais dénommé SARS-CoV-2 est l’objet d’une surveillance génétique étroite. La crainte de mutations affectant la souche d’origine, celle qui s’est manifestée en décembre 2019 à Wuhan (Chine), est grande même si ce virus à ARN est doté d’un matériel génétique permettant de réparer les brins d’ARN susceptibles d’être altérés lors de la transmission d’une espèce à l’autre … et d’un humain à l’autre. Cet argument n’est cependant pas suffisant pour garantir la stabilité du génome viral qui est in fine moindre que celle des virus à ADN. Ainsi, une étude chinoise publiée dans la revue National Science Review qui fait autorité en Chine, évoque la possibilité sinon d’une mutation, du moins d’une évolution du génome viral sous l’effet de la pression sélective imposée par les modifications de l’environnement du coronavirus qui a été confronté à quelques obstacles depuis son émergence.
– La chauve-souris, le pangolin et l’homme
Une chose est sûre, c’est que chez les patients infectés, les séquences du génome viral sont quasiment identiques (à 99,9 % près) ce qui plaide en faveur d’une origine commune : le SARS-CoV2 serait ainsi passé d’une espèce à l’autre, en l’occurrence d’un réservoir (sans doute la chauve-souris) à l’homme, en passant probablement par des hôtes intermédiaires, le pangolin étant parmi les principaux suspects. Les similitudes génétiques entre le SARS-CoV-2 et un bêtacoronavirus hébergé par la chauve-souris dit RaTG13, avec un taux de concordance de 96,2 % sont en effet en faveur de cette hypothèse. Par ailleurs, les gènes qui codent pour les protéines en spicules qui permettent au SARS-CoV et au SARS-CoV2 de s’arrimer aux récepteurs cellulaires du type ACE2 (angiotensin converting enzyme II) seraient très voisins de ceux identifiés chez les virus infectant certains pangolins. Enfin, le génome du SARS-CoV-2 est éloigné de celui du SARS-CoV (concordance : environ 79 %) et de celui du MERS-CoV (environ 50 %).
– Mutation(s) ou évolution
L’étude publiée dans National Science Review s’est penchée sur les divergences moléculaires entre le SARS-CoV-2 et d’autres coronavirus. Elle a aussi abordé l’évolution du génome viral au sein d’une population humaine infectée en procédant au séquençage de 103 de ces virus. La variabilité entre les nucléotides du génome de SARS-CoV-2 et du virus RaTG13 de la chauve-souris a été globalement estimée à 4 %. Si l’on s’intéresse aux seuls sites neutres, la valeur correspondante atteint alors 17 %, ce qui est bien supérieur à des estimations antérieures. En d’autres termes, la divergence entre les deux virus aurait été quelque peu sous-estimée.
Les résultats de cette étude plaident par ailleurs en faveur de modifications récentes des sites fonctionnels des récepteurs de liaison des spicules propres au SARS-CoV-2 et aux SARSr-CoVs du pangolin, ce qui fait évoquer deux hypothèses : ou bien des mutations, ou bien une évolution du génome par sélection naturelle au-delà des recombinaisons, voire une association des deux phénomènes. L’analyse des 103 génomes viraux collectés à Wuhan semble indiquer que deux souches principales sont actuellement à l’œuvre dans l’épidémie chinoise et peut-être dans la pandémie mondiale qui prend forme. Il s’agirait des souches désignées par les lettres L et S, définies par deux SNP (single nucleotide polymorphism) qui les distinguent l’une de l’autre.
– L ou S ?
La prévalence du type L (∼70 %) était bien supérieure à celle du type S (∼30 %) au tout début de l’infection, alors que paradoxalement ce dernier type correspondrait à la version ancestrale du virus. Plus agressif et plus contagieux que le type S, le type L pourrait expliquer la gravité et la contagiosité des premiers cas, encore que d’autres hypothèses soient possibles. Si le type L reste prédominant (mais quelle est sa prévalence actuelle ?), force est de reconnaitre qu’il est devenu moins présent dès le début de janvier 2020 d’après les données de l’étude. Les interventions de confinement et de quarantaine pourraient avoir mis la pression sur le type L qui serait plus agressif et plus contagieux que le type S. Pour ce type S qui serait (ou aurait été) le moins méchant, la pression subie aurait été moindre au point de favoriser son retour en plus grand nombre sur la scène épidémique. Mais il n’en serait pas moins dangereux dans la mesure où il avancerait plus souvent … masqué que le type L.
– Une situation confuse quoi qu’il en soit
Ces hypothèses propres à l’épidémie chinoise et notamment à ses débuts ne permettent pas d’affirmer l’existence de mutations génomiques, loin s’en faut.
Une évolution sous pression serait plus plausible (encore que, sur ce point, les avis des experts divergent), mais il est clair que, pour en savoir plus, il faudra combiner sur une grande échelle et dans bien d’autres populations toute une série d’informations à la fois génétiques, épidémiologiques et cliniques avec plus de recul qu’actuellement… ce qui peut sembler paradoxal à l’heure où la pandémie s’étend au point de rappeler le spectre de la grippe espagnole qui est la mère des épidémies modernes à bien des égards. En l’espace d’un siècle, la science et la médecine ont progressé de manière spectaculaire mais la menace que représente le Covid-19 n’en reste pas moins majeure au point de faire trembler la planète entière avec ou sans mutations du SARS-CoV2. Les divergences dans l’expression épidémiologique d’un pays à l’autre (Iran, Italie, Chine, France) pouvant tenir à des facteurs multiples et intriqués (définition des cas, recours plus ou moins précoce aux tests diagnostiques, mesures préventives etc…)
Dr Philippe Tellier
Référence
Xiaolu Tang et coll. : On the origin and continuing evolution of SARS-CoV-2. National Science Review (2020) : publication avancée en ligne le 3 mars. doi.org/10.1093/nsr/nwaa036.
Source : jim.fr
SARS-CoV-2 : a-t-il déjà muté ?
Dr Claude Biéva
10 mars 2020
medscape.com
Le nouveau coronavirus, alias SARS-CoV-2, a-t-il déjà muté ? Tout laisse penser que oui si l’on s’en réfère aux données publiées dans la National Science Revue ce 3 mars, rapportant l’identification de deux souches différentes désignées L et S au terme d’une comparaison des génomes de 103 échantillons du virus [1]. Argument supplémentaire en faveur de sa capacité à muter : les souches humaines diffèrent d’autres souches de coronavirus identifiées chez la chauve-souris ou le pangolin. Dès lors à quoi faut-il s’attendre demain chez l’homme et quel pourrait être l’impact sur la production d’un vaccin ?
Vitesse de propagation
Le SARS-CoV-2 est le coronavirus responsable de l’épidémie de pneumonies virales apparues en décembre 2019 à Wuhan (Chine). Il a d’abord été vu comme un virus saisonnier proche de celui de la grippe (H1N1 et H5N1) dont il partage les symptômes cardinaux. Mais sa vitesse de propagation ont conduit à réviser ce jugement. Le virus s’est aujourd’hui disséminé avec une vitesse comparable à celle du SARS-CoV de 2002. Son taux de contagiosité (R0) serait compris entre deux et trois personnes, supérieur à celui la grippe (1,3) et moindre que la rougeole (> 12). Au 6 mars, on recensait 3 825 décès et 62 000 guérisons pour 110 041 cas confirmés dans 95 pays.
Des différences entre souches humaines et animales
La séquence du SARS-CoV-2 est à 96,2% identique à celle d’un coronavirus identifié chez la chauve-souris (SARSr-CoV ; RaTG13) dans la province du Yunnan. Mais elle ne présente que 79% de ressemblance avec le SARS-CoV et 50% avec le MERS-CoV. On sait aussi que dans la voie de transmission d’un réservoir naturel à l’homme, les pangolins auraient joué un rôle en apportant un gène SPIKE au SARS-CoV-2. Ces différences entre virus laissent penser qu’une ou plusieurs mutations se sont produites au niveau des protéines de surface qui permettent l’infection des cellules cibles. Pour tenter d’identifier ces mutations chez l’homme, l’équipe chinoise a analysé les génomes de 103 échantillons du virus humain qu’elle a comparé au coronavirus retrouvé chez des espèces de chauve-souris ou chez le pangolin. Sans entrer dans les détails, on note que la différence entre les nucléotides du SARS-CoV-2 et d’un coronavirus présent chez la chauve-souris est d’environ 4%.
Les souches L et S
Chez l’homme, des mutations ont été identifiées sur 149 sites des 103 souches séquencées. Sur base d’une étude SNPs, deux souches ont été identifiées : le type L avec une prévalence de 70% et le type S minoritaire (30%). En dépit du fait que la souche L est aujourd’hui majoritaire, les chercheurs estiment que la souche la plus ancestrale serait la souche S apparue à Wuhan au début de l’épidémie et d’origine animale. Aujourd’hui les données suggèrent que la souche L a une vitesse de transmission plus élevée que la souche S, mais une analyse de sa capacité mutationnelle révèle que cette souche L est aussi celle qui accumule un nombre significativement plus élevé de mutations dérivées de la souche S. C’est cette capacité mutationnelle et cette vitesse de transmission élevée de la souche L qui la rend plus agressive que la souche S.
Et pour la production d’un vaccin ?
Les études locales confirment que la souche L est plus prévalente à Wuhan que dans d’autres régions du monde, mais cette prévalence diminue. L’explication serait que les mesures d’hygiène et de confinement prises par les autorités chinoises exercent une pression de sélection sur le type L mais pas sur le type S qui pourrait peu à peu monter en prévalence. Cette hypothèse n’exclut pas pour autant que des patients soient infectés par les 2 souches, à l’instar de cette femme de 63 ans vivant à Chicago et qui après un séjour à Wuhan a peut-être été infectée plusieurs fois.
Les auteurs soulignent toutefois que l’étude manque de robustesse en raison du petit nombre d’échantillons et que des analyses à grande échelle des données génomiques, épidémiologiques et cliniques de tous les patients seront nécessaires pour mieux comprendre l’évolution et l’épidémiologie du SARS-CoV-2. On retiendra que le SARS-CoV-2 peut se comporter comme un virus de la grippe, en mutation permanente en raison d’erreurs génétiques générées lors de sa réplication. Pour la production d’un vaccin, ces données impliquent de faire attention à cibler la bonne souche. Cela signifierait aussi qu’une vaccination contre un SARS-CoV-2 devrait être répétée (à une fréquence à déterminer).
Cet article a été publié initialement sur MediQuality sous l’intitulé : COVID-19 : le SARS-CoV-2 a-t-il déjà muté ?
— -
Le coronavirus qui circule en Europe est plus infectieux in vitro
source : futura-sciences.com avec l’AFP-Relaxnews
Publié le 03/07/2020
La variante du SARS-CoV-2, appelée D614G, qui domine aujourd’hui dans le monde, infecte plus facilement les cellules que celle apparue en Chine. Bien que cela reste à confirmer, une étude publiée dans Cell le 2 juin 2020 suggère que cela la rend probablement plus contagieuse.
« Nous ne savons pas encore si une personne s’en sort moins bien avec elle ou non », a commenté Anthony Fauci, directeur de l’Institut des maladies infectieuses américain, à la revue Jama. « Il semble que le virus se réplique mieux et puisse être plus transmissible, mais nous en sommes toujours au stade d’essayer de le confirmer. Mais il y a de très bons généticiens des virus qui travaillent là-dessus. »
Après sa sortie de Chine et son arrivée en Europe, une variante du nouveau coronavirus, qui mute en permanence comme tout virus, est devenue dominante. C’est cette version européenne qui s’est ensuite installée aux États-Unis. La variante D614G concerne une mutation d’une seule lettre de l’ADN du virus, sur la protéine S (spike) avec laquelle il pénètre les cellules humaines.
Les mutations génétiques du coronavirus sont traquées dans le monde entier par les chercheurs. Ils séquencent le génome de chaque isolat viral et le partagent sur une base de données internationale, GISAID. Un trésor qui compte plus de 30.000 séquences à ce jour.
D614G, une variante du coronavirus plus transmissible ?
Les chercheurs de la nouvelle étude, des universités de Sheffield et Duke et du laboratoire national de Los Alamos, ont établi en avril que D614G dominait désormais. Ils ont alors affirmé, avec une certaine alarme, que la mutation rendait le virus « plus transmissible ». Ils avaient mis leurs résultats en ligne sur le site de prépublications scientifiques BioRxiv.
Mais cette assertion avait été critiquée car les auteurs n’avaient pas prouvé que la mutation elle-même était la cause de la domination. Les scientifiques ont donc réalisé des travaux et des expériences supplémentaires, à la demande des éditeurs de Cell.
Sur cette illustration en 3D, la protéine S (en rouge) du coronavirus reconnaît le récepteur ACE 2 (en bleu) de la cellule. © Juan Gaertner, Shutterstock
Pas de confirmation formelle d’une meilleure transmission du variant
Ils ont d’abord analysé les données de 999 patients britanniques hospitalisés à cause de la Covid-19. Ceux infectés par la variante D614G avaient certes plus de particules virales dans l’organisme, mais sans que cela n’affecte la gravité de leur maladie. Une observation encourageante.
En revanche, des expériences in vitro ont montré que la variante était trois à six fois plus compétent pour infecter des cellules humaines.
« Il semble probable que c’est un virus plus apte », dit Erica Ollmann Saphire, qui a réalisé l’une de ces expériences, au La Jolla Institute for Immunology. Mais tout est dans le « probable » : une expérience in vitro ne peut reproduire la dynamique réelle d’une pandémie.
La conclusion la plus stricte est donc que si le coronavirus qui circule actuellement, la variante D614G, est sans doute plus « infectieux », il n’est pas forcément plus « transmissible » entre humains. Dans tous les cas, écrivent Nathan Grubaugh, de l’université Yale, et des collègues, dans un article distinct également publié dans Cell, « cette variante est désormais la pandémie ».
« D614G ne devrait rien changer à nos mesures de restrictions ni aggraver les infections individuelles », poursuit Nathan Grubaugh. « Nous assistons au travail scientifique en temps réel : c’est une découverte intéressante qui touche potentiellement des millions de gens, mais dont nous ignorons encore l’impact final. Nous avons découvert ce virus il y a six mois, et nous apprendrons encore beaucoup de choses dans les six prochains mois. »
Ce qu’il faut retenir
- Une souche modifiée du virus est devenue largement majoritaire dans le monde en l’espace de quelques semaines.
- Cette souche dominante se répand bien plus vite que l’originale.
- Une autre mutation suggère au contraire un possible affaiblissement du virus qui pourrait s’éteindre de lui-même comme celui du Sars-Cov de 2013.
Pour en savoir plus
Plus dangereux ou moins sévère ? Le coronavirus a subi deux mutations importantes
Article publié le 7 mai 2020 par Céline Deluzarche
Deux nouvelles souches du coronavirus Sars-Cov-2 ont été identifiées. La première, apparue en Europe, est aujourd’hui prédominante dans le monde et expliquerait la propagation accrue du virus par rapport sa version originale chinoise. Une deuxième mutation a entraîné l’effacement complet de certaines séquences, suggérant un affaiblissement du virus.
Voilà de quoi brouiller un peu plus la compréhension du coronavirus à l’origine du Covid-19 : de nouvelles souches ont été identifiées, mais elles produisent des conclusions contradictoires : l’une serait plus dangereuse que l’originale, l’autre montrerait à l’inverse un possible affaiblissement du virus. On sait que le virus subit en permanence de nombreuses mutations : selon le Centre national de Bio-information chinois, plus de 7.551 mutations ont été enregistrées.
La plupart affecte des parties du génome sans intérêt, mais certaines influent sur la fonction même du virus. Des chercheurs chinois ont ainsi montré récemment que certaines souches sont 270 fois plus virulentes que les autres, ce qui expliquerait en partie pourquoi certaines personnes sont plus sévèrement touchées que d’autres.
“
La fréquence à laquelle cette mutation se propage est alarmante
Une nouvelle étude du laboratoire national de Los Alamos, pré-publiée sur le site bioRxiv, a trouvé 14 mutations sur les protéines de pointe à la surface du virus, celles qui servent au virus à pénétrer dans la cellule. En remontant l’arbre phylogénétique des mutations, les chercheurs ont découvert que l’une d’elles a commencé à se répandre en Europe au mois de février 2020 et a rapidement pris le dessus.
C’est cette même souche qui a gagné la côte Est des États-Unis et qui est à l’origine de l’épidémie à New York. Elle serait aujourd’hui majoritaire dans le monde depuis mars. « Lorsque [cette nouvelle souche] est introduite dans une région, elle devient rapidement la forme dominante, atteste Bette Korber, biologiste et auteure principale. La fréquence à laquelle cette mutation se propage est alarmante. »
La mutation G614 (en bleu) s’est répandue à vitesse fulgurante durant le mois de mars, prenant le dessus sur la souche originale de Wuhan (orange). © Bette Korber et al, bioRxiv, 2020
Non seulement cette souche se répand plus rapidement que la version chinoise originale, suggérant un avantage compétitif, mais elle rendrait les personnes plus vulnérables à une seconde infection, avance l’étude. « Nous avons découvert des recombinaisons entre des souches circulant localement, ce qui indique des infections à souches multiples », détaillent les chercheurs qui ont passé en revue plus de 6.000 séquences. Ces mutations à répétition pourraient compromettre la mise au point d’un vaccin, surtout ceux dirigés vers les protéines de surface, concluent-ils.
Des morceaux de génome ont complètement disparu
Encore en préparation, une autre étude est, quant à elle, beaucoup plus optimiste. Menée par l’université d’Arizona et parue dans le Journal of Virology, elle devrait « susciter l’intérêt de la communauté scientifique du monde entier, y compris de l’Organisation mondiale de la Santé », dès lors qu’elle sera publiée sur un site officiel, s’enthousiasme Efrem Lim qui a dirigé l’équipe de recherche. Les scientifiques ont découvert une mutation dans laquelle 81 bases du génome se sont tout simplement évaporées et « supprimées définitivement du génome ».
Or, c’est ce même phénomène qui avait abouti en 2003 à l’affaiblissement du virus Sars-Cov, puis à à sa disparition. « Durant la phase tardive de l’épidémie, le Sars-Cov a accumulé des mutations qui ont atténué le virus. Le virus affaibli provoque une maladie moins grave peut avoir un avantage sélectif s’il est capable de se propager efficacement dans les populations par des personnes infectées à leur insu », indique Efrem Lim.
L’épidémie de Covid-19 pourrait-elle alors disparaitre d’elle-même ? Il est bien trop tôt pour se prononcer, avancent prudemment les auteurs, d’autant plus qu’on ne connaît pas la fréquence de cette souche. À peine 16.000 génomes du virus ont été séquencés à ce jour, « ce qui représente moins de 0,5 % des souches en circulation », signale Efrem Lim.
Stratégies ventilatoires pour le SDRA de la Covid-19 : restons classiques et prudents !
Publié le 09/07/2020
Au cours des deux dernières décennies, l’hétérogénéité du syndrome de détresse respiratoire aiguë (SDRA) a été de plus en plus reconnue, avec la description de sous-groupes de patients présentant des caractéristiques cliniques et biologiques et des réponses au traitement différentes.
La pandémie de Covid-19 a entraîné une augmentation du nombre de patients atteints de SDRA. Dans un premier temps, plusieurs publications avaient suggéré une hétérogénéité phénotypique des patients Covid-19 en SDRA avec des caractéristiques qui les distinguaient du SDRA historique, ce qui impliquait donc une prise en charge ventilatoire différente. Toutefois, de récentes études semblent indiquer qu’en fin de compte les physiopathologies des SDRA des patients avec ou sans Covid-19, sont largement similaires.
Certes, l’hétérogénéité phénotypique est un concept important, mais qui ne doit aucunement être sur-interprété, en s’écartant du paradigme actuel de la prise en charge ventilatoire du SDRA, avec, sinon, le risque de moins bons résultats.
Quoi qu’il en soit, un vieux principe demeure : celui de la ventilation mécanique personnalisée protectrice des poumons dans le SDRA ; le plus important étant de ne pas abimer les poumons avec de trop forts volumes ou de trop fortes pressions lors de la ventilation.
D’où l’objet de cette mise au point sur les stratégies ventilatoires dans le contexte des récents articles qui ont traité de l’hétérogénéité phénotypique chez les patients avec Covid-19 en SDRA.
Gattinoni le retour ? Ou la description des phénotypes de SDRA associés à la Covid-19
Dans une série de 16 patients Covid-19 sous ventilation mécanique, Gattinoni (l’un des papes vivants de la ventilation protectrice) décrit une hypoxémie sévère en dépit d’une compliance pulmonaire relativement normale, soit un constat très inhabituel chez les patients en SDRA grave.
Chez 8 patients, la gazométrie artérielle et les TDM ont révélé un shunt important malgré un volume faible des zones pulmonaires non ventilées, ce qui suggère une hyperperfusion desdites régions. Comme ces poumons semblaient relativement « ouverts », Gattinoni recommande une stratégie de pression expiratoire positive de fin d’inspiration (PEEP) plus faible, ainsi que l’évitement du décubitus ventral, notamment en raison des fortes limitations en ressources humaines pendant la pandémie (nous sommes alors en Italie, au plus fort de la tempête).
Dans un second article, la même équipe soulignant l’hétérogénéité des patients Covid-19 en SDRA, propose 2 phénotypes : le type L (faibles valeurs de l’élastance, du rapport ventilation/perfusion, du poids des poumons et de la recrutabilité) et le type H (valeurs élevées de l’élastance, du shunt droite-gauche, du poids des poumons et de leur recrutabilité), ce dernier type correspondant davantage au SDRA grave typique. Gattinoni pense que la plupart des patients se présentent initialement avec le type L, et que certains migrent vers le type H, en raison de l’aggravation de la pneumonie et des lésions pulmonaires auto-infligés par le patient lui-même qui hyperventile. Par conséquent, il préconise une intubation endotrachéale précoce chez les patients dont les efforts inspiratoires sont excessifs, et qu’une fois "...profondément sédatés, les patients de type L, s’ils sont hypercapniques, peuvent être ventilés avec des volumes supérieurs à 6 ml/kg (jusqu’à 8-9 ml/kg) du poids corporel, car la compliance élevée entraîne une contrainte tolérable sans risque de lésions pulmonaires induites par le respirateur". Nous en étions alors à un stade précoce de la compréhension de l’hétérogénéité des SDRA Covid-19 avec l’idée que l’identification rigoureuse des phénotypes pourrait guider la prise en charge des patients.
Recommandations pour la gestion du SDRA associé à la Covid-19
L’idée que le SDRA est un syndrome hétérogène - perturbations mécaniques et d’échange gazeux variables - est importante, mais aussi ancienne que le concept même de SDRA, qui contribue à la complexité de la prise en charge. Or, la notion d’hétérogénéité n’est cliniquement pertinente que si elle est débouche sur des différences de traitement. Par exemple, les sous-phénotypes hyper-inflammatoires et hypo-inflammatoires pourraient répondre différemment aux niveaux de PEEP et à la gestion des fluides.
Au chevet du patient, la mesure de la capacité de recrutement pulmonaire à l’aide d’une technique simple aide à adapter la gestion ventilatoire du SDRA, y compris lors de la Covid-19. Toutefois, l’application d’une telle approche physiologique personnalisée n’équivaut pas nécessairement à une amélioration du pronostic du patient.
Premièrement, la ventilation protectrice (ventilation limitée en volume et en pression) s’est d’abord révélée efficace dans une population hétérogène de SDRA avec un large éventail de paramètres physiologiques (compliance statique, plateau de pression, rapport PaO2 / FiO2). Tout comme les patients Covid-19 de phénotype L, les patients en SDRA léger ont généralement une meilleure compliance que ceux en SDRA plus grave.
Certaines données suggèrent que la ventilation protectrice peut être bénéfique même chez les patients dont la pression de plateau est relativement faible. En outre, plusieurs études ont montré que la ventilation protectrice chez les patients dont les poumons sont relativement normaux est associée à une diminution des complications pulmonaires, à une moindre progression du SDRA, et à une amélioration clinique.
Les patients dont la réponse inflammatoire est robuste, comme lors de la Covid-19, sont probablement biologiquement plus enclins à développer des lésions pulmonaires induites par la ventilation. Chez ces patients, la mécanique respiratoire pourrait se détériorer, avec risque de lésions pulmonaires en particulier avec la reprise des efforts de ventilation spontanée.
Par conséquent, la « libéralisation » des volumes courants chez ces patients pourrait être associée à de moins bons résultats, même s’ils ne sont pas dans ce que l’on pourrait considérer comme un SDRA typique. Gattinoni recommande des volumes courants supérieurs à 6 ml/kg chez les patients Covid-19 en SDRA de type L qui développent une hypercapnie. Or, en raison du risque de lésions pulmonaires plus importantes induites par le respirateur avec des volumes courants plus élevés, les auteurs de cet article recommandent plutôt de s’attaquer en premier aux causes courantes traitables de l’hypercapnie (fréquence respiratoire inadéquate, espace mort augmenté par le filtre d’échange de chaleur et d’humidité au niveau du raccord en Y, absence de compensation de la compliance du circuit amputant les volumes délivrés) avant de recourir à des volumes courants plus élevés.
Deuxièmement, quel est le niveau d’hypercapnie tolérable ? Une hypercapnie permissive avec des volumes courants plus faibles peut réduire le risque de lésions pulmonaires dues au ventilateur et être bien tolérée. Mais elle peut également être associée à un certain nombre d’effets délétères : croissance bactérienne, moindre cicatrisation des lésions alvéolaires, réabsorption du liquide alvéolaire et prolifération des cellules alvéolaires, aggravation de l’hypertension pulmonaire. Le degré acceptable d’hypercapnie dépendra en partie de l’acidose métabolique ou de l’instabilité hémodynamique qui y est associée.
Troisièmement, l’évolution temporelle proposée pour les phénotypes L et H soulève la question de savoir si ces sous-types ne reflèteraient tout simplement pas l’évolution naturelle du SDRA. Cette question est particulièrement pertinente chez les patients Covid-19 en SDRA qui auraient pu être intubés plus tôt dans l’évolution de la maladie, ce qui n’avait généralement pas été le cas (en Italie). La comparaison des données est difficile car la décision d’intuber peut avoir été prise à des moments très différents de l’évolution de la maladie dans divers centres, selon la disponibilité des ressources. Tout cela soulève la délicate question du moment optimal de l’intubation, avec une fenêtre très étroite et les conséquences d’une intubation trop précoce ou trop tardive.
Quatrièmement, la question des niveaux de PEEP s’avère plus complexe que la précédente discussion sur la gestion du volume courant. Les données précédentes suggèrent déjà que le même niveau de PEEP ne devrait pas être appliqué à tous les patients en SDRA. Une approche personnalisée est nécessaire car la réponse à la PEEP diffère en fonction de la mécanique respiratoire de chacun. Les études fondamentales de Suter et de Dantzker ont montré que la PEEP peut réduire l’hypoxémie tout en réduisant l’apport d’oxygène aux tissus. S’il existe en fait un phénotype dans lequel le dérèglement vasculaire est le principal mécanisme de l’hypoxémie (perte de vasoconstriction pulmonaire, embolie, thrombi pulmonaires), alors l’augmentation de la PEEP pourrait ne pas réduire l’hypoxémie. Par conséquent, la PEEP doit être ciblée pour améliorer la distribution d’oxygène tout en atténuant le risque de lésions pulmonaires induites par le respirateur et de lésion pulmonaire auto-infligée par le patient, selon le contexte clinique. Ce titrage reste compliqué à réaliser chez les patients en SDRA avec ou sans Covid-19.
Quelles preuves de phénotypes dans le SDRA associé à la Covid-19 ?
Gattinoni retrouve un tiers des patients en SDRA grave (type H), ce qui correspond à la proportion déjà connue de patients en SDRA tout venant. Dans deux articles sur des patients ventilés pour un SDRA associé à la Covid-19 à New York, les compliances médianes étaient de 28 mL/cm H2O et 26 mL/cm H2O, ce qui est loin d’être inhabituel chez des patients en SDRA. Des valeurs similaires ont été rapportées dans deux plus petites études à Seattle et à Boston (29 mL/cm H2O et 35 mL/cm H2O, respectivement). Certes ces données n’excluent pas l’existence de phénotypes présentant une compliance élevée, mais elles suggèrent qu’en général, les patients Covid-19 en SDRA ont une mécanique respiratoire similaire à celle des patients souffrant d’un SDRA d’autres causes et que, pour la plupart des patients, le SDRA associé à la Covid-19 est, en fin de compte, un SDRA habituel.
Là où le bât blesse, c’est que le simple fait de considérer le SDRA associé à la Covid-19 comme une entité différente, suggère d’abandonner les principes de traitement actuels en faveur d’une nouvelle approche, laquelle, en l’absence de preuves solides du contraire, peut s’avérer délétère.
Conclusions et orientations futures : déboulonner la statue du Commandeur
Aussi, restons classiques et inoffensifs. Les patients Covid-19 en SDRA modéré à grave doivent être mis en décubitus ventral et les patients en SDRA grave peuvent nécessiter une oxygénation par membrane extracorporelle veineuse (ECMO), comme indiqué dans les recommandations internationales pour le SDRA, et en fonction des ressources disponibles. Ce qui n’exclut nullement des ajustements en fonction des problèmes spécifiques à chaque patient. Par exemple, l’hétérogénéité apparente pourrait être due à un processus pathologique sous-jacent distinct contribuant à l’hypoxémie, qui nécessite un traitement non ventilatoire (prévalence accrue des complications thrombo-emboliques dans la Covid-19). Bien entendu, si un tel patient nécessite une ventilation mécanique, il n’est pas approprié d’utiliser une stratégie ventilatoire qui cible largement des poumons atélectasiques remplis de liquide.
De ta rigueur scientifique, point ne te départira
En particulier en cette ère de dictature des média sociaux, nous devons trouver un équilibre entre les anecdotes, les histoires de chasse et les publications de quelques cas et la rigueur scientifique nécessaire pour étayer tout changement dans le paradigme actuel de la prise en charge des patients. Les auteurs de cette mise au point et disciples du maître de la ventilation protectrice – comme le sont tous les réanimateurs –préconisent de s’en tenir, jusqu’à preuve du contraire, à une approche et une prise en charge fondées sur des données probantes et éclairée par des décennies de recherche sur le SDRA et par la physiologie au chevet du patient.
Messages clés
Lors d’une situation nouvelle et rapidement évolutive telle que la pandémie de Covid-19, il est important de trouver un équilibre entre l’évolution rapide des connaissances et le faible niveau initial des preuves - essentiellement des séries de cas, des rapports de cas et des anecdotes - et la rigueur scientifique nécessaire pour accompagner et défendre tout changement qui s’impose dans le paradigme actuel de la prise en charge des patients.
La notion que le SDRA est un syndrome hétérogène est une constatation omniprésente aussi ancienne que le concept même de SDRA, ce qui contribue considérablement à la complexité de sa gestion. Or la notion d’hétérogénéité est plus pertinente lorsqu’elle est liée à des traitement différenciés dont il a été démontré qu’ils améliorent les résultats.
Les rapports sur l’hétérogénéité phénotypique chez les patients COVID-19 en SDRA, bien qu’intéressants, pourraient facilement être sur-interprétés ou appliqués de manière inappropriée en service de réanimation, ce qui pourrait conduire à des stratégies de gestion ventilatoire préjudiciables chez de tels patients.
De vastes études d’observation suggèrent que les patients Covid-19 en SDRA ont un système respiratoire similaire à celui des patients présentant un SDRA liés à d’autres étiologies, et que chez la plupart d’entre eux, le SDRA associé aux Covid-19 est, en fin de compte, un SDRA comme les autres.
Les auteurs recommandent donc vivement le respect d’une prise en charge de la détresse ventilatoire fondée sur des données probantes, éclairées par l’observation de la physiologie au chevet du patient et étayée par des résultats. Cette approche comprend une ventilation mécanique protectrice des poumons, une PEEP individualisée, une ventilation en décubitus ventral et une oxygénation par membrane extracorporelle veineuse (ECMO) si nécessaire, comme le suggèrent les directives internationales relatives au SDRA et dans la mesure où les ressources le permettent.
Dr Bernard-Alex Gaüzère
RÉFÉRENCE
Fan E, Beitler JR, Brochard L et coll. : COVID-19-associated acute respiratory distress syndrome : is a different approach to management warranted ?Lancet Respir Med., 2020 ; publication avancée en ligne le 6 juillet doi.org/10.1016/ S2213-2600(20)30304-0
source : jim.fr
Ventilation en USI : la PEEP plus basse n’est pas inférieure…
Publié le 03/03/2021
Le recours à la ventilation invasive est très fréquent en unité de soins intensifs (USI) mais ce n’est pas une intervention sans risque. Le rôle protecteur d’un faible volume courant est bien établi. Le niveau idéal de pression positive en fin d’expiration (PEEP) est, en l’absence de syndrome de détresse respiratoire aiguë (SDRA), plus incertain. Ces dernières années, la PEEP a eu tendance à augmenter, passant en moyenne en 1998 de 5 cm d’H20 à 7 cm en 2016, sans informations claires sur le rapport bénéfices/risques de cette tendance.
Il est certes possible que chez les patients sans SDRA ventilés, un plus haut niveau de PEEP contribue à une meilleure aération des poumons, prévienne la survenue d’un SDRA et réduise le risque d’apparition d’une pneumonie liée à la ventilation (VAP). A l’inverse, il pourrait causer ou aggraver des lésions préexistantes et altérer l’hémodynamique. Enfin, il est de coutume d’extuber un patient à basse PEEP et le maintien d’un haut niveau pourrait être cause de retard au sevrage du ventilateur.
Etude RELAx
L’étude RELAx (Restriction vs Liberal Positive end-Expiratory Pressure in Patients without ARDS) a été conçue afin de déterminer si une stratégie ventilatoire avec bas niveau de PEEP n’était pas inférieure à une stratégie avec PEEP plus élevée, lors d’une ventilation mécanique de 28 jours maximum. RELAx est un essai clinique randomisé mené dans les USI de 6 hôpitaux néerlandais. Pour être inclus, les participants devaient avoir été ventilés peu de temps, avant ou après leur admission en soins intensifs et ne devaient pas, en théorie, être extubables dans les 24 heures suivant la randomisation (cette dernière étant effectuée dans l’heure suivant leur passage en USI). La présence d’un SDRA constituait un critère formel d’exclusion, tout comme une durée de ventilation de 12 heures ou plus avant l’entrée en réanimation. La randomisation du degré de PEEP a été centralisée, dans un rapport 1:1, par bloc maximal de 8.
Dans le groupe PEEP la plus basse, entre 0 et 5 cm d’H20, la ventilation mécanique a débuté avec une PEEP de 5 pour une fraction d’oxygène dans l’air inspiré (FiO2) comprise entre 0,21 et 0,6. Ensuite, elle a été abaissée régulièrement de 1 cm toutes les 15 minutes tant que la saturation en oxygène (SaO2) se maintenait à plus de 92 % et que la pression partielle (PaO2) restait supérieure à 60 mm Hg. Par la suite, la ventilation s’est poursuivie avec la PEEP la plus basse possible, selon les critères d’oxygénation définis. Le groupe avec PEEP haute avait une PEEP à 8 cm d’H20, pour une FiO2 comprise entre 0,21 et 0,6. En cas d’instabilité hémodynamique, dans l’un et l’autre groupe, on procédait une adaptation à 5 cm H20, puis, après stabilisation, la PEEP était ramenée à sa valeur initiale, plus basse ou plus haute, l’objectif étant toujours le maintien d’une SaO2 entre 92 et 96 % et une PaO2 entre 60 et 85 mm Hg. Le principal paramètre analysé a été le nombre de jours sans ventilation invasive des patients ayant survécu, à partir de la date de la randomisation. Les paramètres secondaires ont été, principalement, la durée d’hospitalisation en USI et globale, la mortalité au 28e et 90e jour, la durée totale de ventilation des survivants et la survenue de complications pulmonaires (SDRA, VAP, hypoxémie sévère ou pneumothorax). Ont été également notés les traitements de secours en cas d’hypoxémie, le nombre de jours sous vasopresseurs ou sous sédation. L’objectif du travail visait la démonstration d’une non infériorité d’une stratégie à basse PEEP, vs celle utilisant une PEEP plus haute, la marge retenue de non infériorité étant de -10 %, ou encore une différence de ventilation d’au moins 0,5 jours ou 1,6 jours sans ventilation. Plusieurs analyses de sensibilité ont été effectuées, après ajustement en fonction de l’âge, du sexe et du score de gravité APACHE IV.
Entre le 26 Octobre 2017 et le 17 Décembre 2019, sur un total de 2 869 participants potentiels, 980 ont été randomisés, 484 avec une PEEP faible et 456 avec une PEEP plus haute. Le suivi étant incomplet chez quelques malades, l’analyse finale a porté sur 969 patients, dont 476 sous faible niveau de PEEP. L’âge médian était de 66 ans (intervalle interquartile IIQ : 56-74) ; 36 % étaient des femmes. Le motif d’admission en USI le plus fréquent (39,2 %) avait été une détresse respiratoire. Le délai entre début de la ventilation invasive et randomisation avait été très court, en moyenne de 0,6 heures (IIQ : 0,2- 1,1 heures). On a noté , en cours de ventilation, une pression motrice significativement plus haute et une pression plateau plus basse en cas de PEEP moins élevée, durant les 5 premiers jours de ventilation mécanique, sans différence significative entre les 2 bras concernant les paramètres d’ oxygénation (FiO2, SaO2 et rapport PaO2/ FiO2). On n’a observé aucune différence, entre les 2 bras, dans le niveau de sédation requis, la fréquence cardiaque, la pression artérielle moyenne, l’administration de fluides, de transfusions ou de drogues vaso actives.
17 jours sans ventilation contre 18
Au 28e jour, les 476 patients du groupe PEEP basse avaient eu une médiane de 18 jours sans ventilation (IIQ : 0- 27) vs 17 jours pour ceux du groupe PEEP haute (IIQ : 0- 27), soit un rapport moyen de non infériorité s’établissant à 1,04 jours (Intervalle de confiance à 95 % IC : 0,95-∞, p= 0,007). La limite inférieure de l’intervalle de confiance se situe donc dans la marge de non infériorité. Une hypoxémie sévère est survenue dans, respectivement, 20,6 % et 17,6 % des observations (rate ratio RR : 1,17 ; IC : 1,02- 1,79). La mortalité, au 28e jour, a été de 38,4 vs 42 % (Hazard Ratio HR à 0,81 ; IC : 0,73- 1,09 ; p= 0,99). On ne note aucune différence dans les durées d’hospitalisation en USI ou globale.
Ce travail démontre donc que chez des patients admis en USI, nécessitant une ventilation artificielle mais sans SDRA, une stratégie de ventilation à basse PEEP n’est pas inférieure à une stratégie utilisant une PEEP plus haute si l’on retient comme critère principal le nombre de jours non ventilés lors d’un suivi de 28 jours. Il n’y a pas, non plus, de différences significatives, concernant la durée d’hospitalisation, le taux de mortalité ou encore de celui des complications observées dans les 2 groupes. Ces résultats prennent toute leur importance eu égard à la tendance observée, ces dernières années, à augmenter le niveau de PEEP, en l’absence de données précises sur le rapport bénéfices/ risques de cette élévation.
Nombre de points forts sont à relever dans cet essai. Les biais possibles ont été réduits grâce à un protocole précis. Par opposition à un essai espagnol, le taux de VAP a été faible, de l’ordre de 1,3 %, sans différence statistique entre les 2 bras, possiblement en rapport avec la décontamination digestive sélective mise en œuvre dans RELAx. Toutefois, à l’évidence, cet essai n’a pas été mené en aveugle, des patients ont été exclus de par le cours intervalle requis entre début de la ventilation et randomisation. Enfin, il importe de signaler que le score APACHE IV était plus élevé dans le groupe PEEP forte.
En conclusion, chez des patients sans SDRA ventilés en USI, appliquer une PEEP basse n’est pas inférieur à une stratégie de PEEP plus élevée si l’on prend en compte le nombre de jours sans ventilation, après un suivi total de 28 jours. Ces données plaident donc en faveur de l’utilisation d’une PEEP faible en cas de ventilation mécanique quand il n’y a pas de SDRA.
Dr Pierre Margent
Référence
RELAx collaborative group. : Effect of a lower vs higher positive end-expiratory pressure strategy on ventilation-free days in ICU patients without ARDS. JAMA. 2020 ; 324(24) : 2509-2520. doi : 10.1001/jama.2020.23517
Source : jim.fr
Opter pour le décubitus ventral éveillé dans les Covid-19 graves
Publié le 25/08/2021
Chez les patients intubés en SDRA modéré à sévère, le positionnement en décubitus ventral (DV) améliore l’oxygénation et réduit la mortalité. Au cours d’études rétrospectives et observationnelles menées chez des patients non intubés présentant un SDRA et, plus récemment, chez des patients atteints d’une forme grave de Covid-19, le DV sans sédation ou DV éveillé a été associé à une meilleure oxygénation et a été identifié comme une priorité de recherche par le Surviving Sepsis Research Committee. Il ne restait plus qu’à procéder à des essais prospectifs et randomisés à grande échelle afin de savoir si cette technique qui requiert la pleine coopération du patient pouvait prévenir l’intubation ou le décès chez les patients atteints de Covid-19 grave.
Moins d’échec de traitement en DV éveillé
Dans ce méta-essai collaboratif prospectif, défini et établi a priori, portant sur six essais de supériorité randomisés, contrôlés et ouverts, ont été inclus des adultes nécessitant une assistance respiratoire avec canules nasales à haut débit pour une insuffisance respiratoire hypoxémique aiguë due à la Covid-19, provenant de différents pays : Canada, France, Irlande, Mexique, États-Unis, Espagne. Le principal résultat composite était l’échec du traitement, défini comme la proportion de patients intubés ou décédés dans les 28 jours suivant l’inclusion. Entre le 2 avril 2020 et le 26 janvier 2021, 1 126 patients ont été assignés de manière aléatoire, soit au positionnement en DV éveillé (n = 567) soit à une prise en charge dite standard (n = 559) ; 1 121 patients (à l’exclusion de cinq qui se sont retirés de l’étude) ont été inclus dans l’analyse en intention de traiter.
L’échec du traitement a été constaté chez 223 (40 %) des 564 patients en DV éveillé et chez 257 (46 %) des 557 patients recevant des soins standard (risque relatif 0-86 [intervalle de confiance à 95 % IC 95 % 0,75 – 0,98]). Le hazard ratio (HR) pour l’intubation a été de 0,75 (0,62 – 0,91), et le HR pour la mortalité était de 0,87 (0,68 – 1,11) dans de bras DV éveillé par rapport au bras des soins standards, dans les 28 jours suivant l’inclusion. L’incidence des événements indésirables pré-spécifiés a été faible et similaire dans les deux groupes.
Le DV éveillé, comment ça marche ?
Au-delà des avantages individuels, le moindre recours à l’intubation pourrait soulager la pression sur les besoins en ventilateur, tandis que la durée de séjour à l’hôpital n’a pas été affectée par le positionnement en DV éveillé. Plusieurs mécanismes physiologiques pourraient sous-tendre ces résultats cliniques favorables. Le DV assure une distribution plus homogène de la pression dans les régions pulmonaires, ce qui réduit le stress et la tension pulmonaires régionaux. Il améliore l’oxygénation, probablement en homogénéisant le rapport ventilation / perfusion et en diminuant le shunt alvéolaire. En outre, la baisse de la fréquence respiratoire observée pendant le DV éveillé pourrait refléter une réduction de la pulsion respiratoire et entraîner une diminution des oscillations de la pression trans-pulmonaire, ce qui minimiserait les lésions pulmonaires auto-infligées par le patient. Mais, contrairement au positionnement en DV des patients intubés et sous sédation, voire curarisés, la mise en œuvre efficace du positionnement en DV éveillé nécessite la coopération des patients.
Quelle durée optimale pour le DV éveillé ?
D’importantes variations dans la durée du DV éveillé reflétant des caractéristiques individuelles telles que l’âge, la stature, la tolérance, le soutien de l’équipe soignante et la disponibilité d’options d’escalade existaient entre les patients et les études. Bien que des durées de DV plus longues ont été associées à un plus grand taux de réussite, cette étude n’avait pas été conçue pour évaluer l’effet de la durée du positionnement en position allongée éveillée, et la gravité initiale de l’état des patients et la réponse au positionnement pourraient influencer l’engagement dans la procédure de positionnement en DV éveillée. De futures études sont nécessaires pour explorer l’effet dose-réponse. Mais, étant donné que des durées plus longues de positionnement en décubitus ventral éveillé ont été associées à un risque plus faible d’échec du traitement, les patients doivent être encouragés à rester en décubitus ventral aussi longtemps qu’ils peuvent le tolérer.
Le présent travail présente plusieurs limites
Tout d’abord, la nature même de l’intervention n’a pas permis de procéder en aveugle, avec le risque que la médiatisation de la technique ait influencé la prise de décision des réanimateurs. De plus, malgré l’existence de critères d’intubation clairement définis, les réanimateurs auraient pu s’abstenir d’intuber sur la base d’améliorations transitoires des paramètres respiratoires pendant le DV éveillé ou, inversement, avoir un seuil d’intubation plus bas pour les patients du groupe de soins standard.
Toutefois, ces limites sont largement contrebalancées par l’avantage de la mise en place très rapide d’une étude internationale randomisée générant des preuves de haut niveau dans un court laps de temps. Ces résultats soutiennent le positionnement en décubitus ventral éveillé systématique des patients atteints de Covid-19 qui nécessitent une assistance avec des canules nasales à haut débit.
À consommer sans modération…
Dr Bernard-Alex Gaüzère
Référence
Ehrmann S et coll. : Awake prone positioning for COVID-19 acute hypoxaemic respiratory failure : a randomised, controlled, multinational, open-label meta-trial. Lancet Respir Med., 2021. publication avancée en ligne le 20 août. doi.org/10.1016/S2213-2600(21)00356-8
Source : jim.fr
Production d’aérosols au cours de l’anesthésie générale, c’est comme quand on tousse !
Publié le 17/04/2022
L’intubation, la laryngoscopie et l’extubation sont considérées comme des procédures fortement génératrices d’aérosols, et ceci a conduit à mettre en place des protocoles de sécurité supplémentaires pendant cette pandémie de Covid-19. Cependant, les études qui ont inspiré ces nouvelles démarches sont principalement expérimentales et n’ont ni analysé l’exposition du personnel à la génération d’aérosols dans l’environnement réel de la salle d’opération, ni comparé l’exposition aux concentrations d’aérosols générées pendant les soins habituels aux patients. Il n’existe pas de consensus sur les procédures qui sont significativement génératrices d’aérosols et actuellement les CDC rappellent « qu’il n’existe ni consensus d’experts, ni données justificatives suffisantes pour créer une liste définitive et complète des procédures générant des aérosols pour les établissements de santé. »
Les concentrations de particules générées lors de l’AG et de la toux sont comparables
Afin d’évaluer l’exposition du personnel des blocs à la génération de particules potentiellement infectieuses pendant l’anesthésie générale, cette étude observationnelle multidisciplinaire monocentrique menée à l’hôpital universitaire d’Helsinki auprès de 39 patients adultes (56 % d’hommes, 44 % de femmes, âge médian 55 ans (intervalle 19-85), IMC moyen de 26,7 (intervalle 15,6 - 44,9), a mesuré la concentration et la distribution de la taille des particules à l’aide d’un calibreur optique de particules, chez les patients lors d’une intervention chirurgicale avec intubation trachéale. Les concentrations moyennes de particules pendant les différentes procédures d’anesthésie ont été comparées statistiquement aux données de contrôle de la toux recueillies auprès de 37 volontaires pour évaluer les différences dans la génération de particules.
Les mesures ont concerné 25 pré-oxygénations, 30 ventilations au masque, 28 intubations et 24 extubations. La concentration totale d’aérosols la plus élevée, de 1 153 particules (p)/cm³, a été observée pendant la ventilation au masque. Les pré-oxygénations, les ventilations au masque et les extubations ainsi que les intubations non compliquées ont généré des concentrations moyennes d’aérosol statistiquement comparables à la toux. Il convient de noter que, curieusement, l’intubation difficile a généré significativement moins d’aérosols que l’intubation simple (p = 0,007) ou la toux (p = 0,006).
Ne pas baisser la garde pour autant
Toutes les procédures effectuées au cours d’une anesthésie générale génèrent principalement des particules aérosols de petite taille (< 1 µm) qui peuvent rester en suspension dans l’air pendant de longues périodes et peuvent être inhalés jusqu’au niveau alvéolaire. D’après ces résultats, l’inscription de la pré-oxygénation, de la ventilation au masque, de l’intubation et de l’extubation sur la liste des procédures générant des aérosols à haut risque devrait être reconsidérée. En outre, en raison des grandes différences interindividuelles, des quantités élevées d’aérosol ont été observées pour certains patients. Ces résultats peuvent être appliqués à l’évaluation du risque d’infection par voie aérienne dans les salles d’opération.
Dr Bernard-Alex Gaüzère
RÉFÉRENCE
Oksanen L-M, Sanmark E, Sofieva S, et coll. : Aerosol generation during general anesthesia is comparable to coughing : An observational clinical study. Acta Anaesthesiol Scand., 2022 ; 66 : 463– 472. doi:10.1111/aas.14022
Source : jim.fr
La Covid va avec la pollution, évidemment !
Publié le 29/04/2022
De longue date, la pollution de l’air a été identifiée comme pouvant contribuer à des infections respiratoires telles que la grippe, la dengue ou le syndrome de détresse respiratoire aigu. De façon similaire, elle pourrait majorer le risque d’infections à SARS-CoV-2 ou leur gravité en modifiant la susceptibilité de l’hôte et/ou en augmentant les co morbidités. En complément à des preuves expérimentales, de récentes études écologiques ont suggéré le rôle de cette pollution mais ces dernières comportaient un risque notable de surestimation, car menées à un niveau de groupe et non à un niveau individuel. En outre, peu de travaux ont ciblé la population d’adultes jeunes.
Z Yu et coll. ont donc conduit une étude pour mieux préciser l’association éventuelle entre exposition à court terme à une pollution atmosphérique au niveau de la résidence individuelle et risque d’infection à SARS-CoV-2 chez de jeunes adultes suédois. Ils ont analysé l’impact de différents facteurs dont le sexe, l’existence d’un surpoids, d’un asthme ou d’un tabagisme, la saisonnalité et la symptomatologie infectieuse auto rapportée. Les données de cette étude, ont été tirées de la cohorte BAMSE (Children, Allergy, Milieu, Stockholm, Epidemiology) dans laquelle ont été identifiés en PCR tous les cas positifs au SARS-CoV-2 entre le 5 Mai 2020 et le 31 Mars 2021. Le jour retenu était celui de la réalisation du test PCR, des contrôles étant effectués à des dates identiques pour le jour, la semaine et le mois. L’analyse des données recueillies a été menée entre le 1er Septembre et le 31 Mars 2021. Les polluants de l’air analysés journellement étaient les particules de diamètre ≤ 2,5 µM (PM 2,5), celles ≤ 10 µM (PM 10), les émissions de noir de carbone (black carbone BC) et les oxydes d’azote (NOx). Les mesures de ces divers polluants étaient réalisées sur le lieu même de la résidence des participants. Les émissions provenaient du trafic routier, de la combustion de bois de chauffage, de la production d’énergie, de l’industrie et d’autres sources de pollution situées dans les régions de Stockholm et d’Uppsala. Dans le même temps étaient enregistrées les données météorologiques, dont la force du vent. Le principal paramètre analysé a été le taux d’infections à SARS-CoV-2 et sa relation avec les différents polluants atmosphériques, avec utilisation de modèles de régression logistique et prise en compte de différentes covariables (âge, sexe, niveau d’éducation, profession, tabagisme, indice de masse corporelle). L’étude a été menée polluant par polluant et également de façon cumulative.
6 à 7 % de tests positifs en plus quand le taux de particules et de black carbone augmente dans l’air
Au total, 425 participants de la cohorte BAMSE ayant présenté un test PCR positif au SARS-CoV-2 ont été identifiés entre le 5 Mai 2020 et le 31 Mars 2021. Leur âge moyen était de 25,6 (écart interquartile EIQ 24,9- 26,3) ans ; 229 (53,9 %) sont des femmes. Le taux médian d’exposition au PM2,5 a été de 4,4 (2,6- 6,8) µg/m3 les jours retenus. Il a été de 7,7 (4,6- 11,3) µg/m3 pour les PM10, de 0,3 (0,2- 0,5) pour les BC et de 8,2 (5,6- 14,1) µg/m3pour les NOx. A titre de comparaison, les moyennes d’exposition les jours contrôle se situaient respectivement à 3,8 (2,4- 5,9) pour les PM2,5, à 6,6 (4,5- 10,4) pour les PM10, à 0,2 (0,2- 0,4) pour les BC et à 7,7 (5,3 -12,8) µg/m3 pour les NOx. Chaque hausse (d’un EIQ) dans le degré d’exposition aux PM 2,5 était associée, avec un décalage de 2 jours, à une augmentation relative du taux de positivité des tests PCR au SARS-CoV-2 d’environ 6,8 % (intervalle de confiance à 95 % IC : 2,1- 11,8 %). Pour l’exposition accrue aux PM10, elle était de 6,9 % (IC : 2,0- 12,1) et, avec un retard de un jour, de 5,8 % (IC : 0,3- 11,6) pour les BC. A contrario, aucune variation n’a été constatée en fonction de l’exposition aux NOx. Les résultats globaux ne sont pas non plus affectés par le sexe, la présence d’un tabagisme, un asthme éventuel, un surpoids ou en fonction de signes auto respiratoires auto rapportés de Covid-19. L’allongement de la période d’étude jusqu’ à 14 jours après exposition aux divers polluants atmosphériques n’a pas modifié les premiers résultats.
Ce travail est, à priori, le premier à avoir analysé l’association entre pollution de l’air et Covid chez des adultes jeunes. Il est apparu que chaque augmentation d’un IQR des concentrations journalières de PM2,5, PM10 et BC était associée à une hausse des taux de Covid-19 comprise entre 6 et 7 %. Ces constations sont en accord avec les résultats de plusieurs études écologiques antérieures, menées dans des régions et pays variés, qui avaient démontré qu’une qualité de l’air médiocre était associée à davantage d’infections respiratoires. Une méta analyse récente, ayant inclus 35 études observationnelles avait confirmé cette association, le rapport de risque RR se situant à 1,003 (IC : 1,002-1,004) pour une augmentation des PM2,5 et à 1,005 (CI : 1,003- 1,006) pour une augmentation de 1 µg/m3 des PM10. Dans ce travail, le délai entre exposition aux polluants de l’air et survenue de l’infection a été très court, de l’ordre de 2 jours pour les PM2,5 et 10, voire de 1 jour pour les BC. Il est plausible que l’exposition aux divers polluants provoque une inflammation des voies aériennes, entraîne un stress oxydatif, des modifications de l’immuno- modulation de l’hôte face à l’agent infectieux, voire agit en aggravant une infection pré existante. Point à souligner, ni le sexe, ni un éventuel tabagisme ou un surpoids ne semblent interférer dans cette association.
Les points forts de ce travail tiennent au modèle utilisé, stratifié en fonction du temps et à la prise en compte d’autres facteurs comme la densité de population ou le mode de vie. Ils sont aussi liés à la fiabilité des données recueillies, à partir de registres nationaux, à l’analyse effectuée à un niveau individuel et non collectif et au ciblage de différents sous-groupes de population. A l’inverse, on ne peut exclure la possibilité d’erreurs de classification ou l’intervention d’autres facteurs confondants méconnus. Des études ultérieures restent à mener, sur des populations plus nombreuses et dans d’autres régions géographiques, pour confirmer l’association entre pollution de l’air à court terme et infection à SARS-CoV-2.
En conclusion, cette étude des relations entre pollution atmosphérique et Covid-19, suggère qu’une exposition à court terme à divers polluants, sur le lieu de résidence, est associée à une augmentation du risque d’avoir un test PCR positif à SARS-CoV-2 dans les uns à deux jours suivants. Ces résultats renforcent l’intérêt, en matière de santé publique, de tenter de réduire les taux de pollution dans l’air ambiant.
Dr Pierre Margent
Référence
Yu Z et coll. : Association of Short Term Air Pollution Exposure with SARS-CoV-2 Infections Among Young Adults in Sweden. JAMA Netw Open. 2022, 5 (4). e : 228 109. doi : 10.1001/jamanetworkopen.2022.8109.
Le décubitus ventral pour éviter l’intubation
Publié le 20/12/2022
Il existe des données prouvant l’efficacité de la position en décubitus ventral pour les patients ventilés pour détresse respiratoire liée à la Covid-19. L’intérêt de cette position pour les patients respirant spontanément est toutefois incertain.
Le British Medical Journal publie les résultats d’une méta-analyse de 17 essais randomisés, comparant le décubitus ventral aux soins habituels chez des patients présentant une insuffisance respiratoire hypoxémique liée à la Covid-19, non intubés. Le critère de jugement principal était la nécessité d’une intubation. Les critères secondaires étaient la mortalité, le nombre de jours sans ventilation, la durée d’hospitalisation, l’évolution des doses d’oxygène nécessaires, et les effets indésirables.
Les données confirment que la position en décubitus ventral peut réduire le risque d’intubation, en comparaison avec les soins habituels (24,2 % vs 29,8 % ; risque relatif RR 0,83 ; intervalle de confiance à 95 % 0,73 à 0 ,94). Les résultats ont un degré élevé de certitude et persistent après les nombreuses analyses de sensibilité. En moyenne, la position en décubitus ventral permet d’éviter 55 intubations tous les 1 000 patients. En revanche, elle a un effet très limité, voire nul, sur la mortalité, sur les jours sans ventilation, les durées de séjour ou les autres critères secondaires.
Le décubitus ventral est sans danger, avec des effets indésirables rares, parmi lesquels des déplacements non intentionnels de cathéter, un inconfort, des nausées ou des lésions cutanées. Les essais futurs devraient permettre de définir des stratégies pour améliorer la tolérance de la position, déterminer sa durée optimale et son intérêt pour d’autres causes d’insuffisance respiratoire hypoxémique.
Dr Roseline Péluchon
Références
Weatherald J. et coll. : Efficacy of awake prone positioning in patients with covid-19 related hypoxemic respiratory failure : systematic review and meta-analysis of randomized trials
BMJ 2022 ;379:e071966. doi.org/10.1136/bmj-2022-071966
jim.fr
Origine du SARS-CoV-2 : la vérité nous-a-t-elle été cachée ?
Publié le 27/12/2022
Des échanges entre responsables américains rendus publics révèlent comment la thèse de l’origine humaine du SARS-CoV-2 a été écartée au début de la pandémie.
En décembre 2019, les premiers cas de ce que l’on n’appelait pas encore la Covid-19 étaient détectés dans la ville de Wuhan en Chine, amorçant les prémices d’une pandémie qui allait bouleverser l’humanité. Trois ans plus tard la question de l’origine du SARS-CoV-2 reste ouverte et de nombreux scientifiques à travers la planète planchent sur la question. Deux théories s’opposent : celle de l’origine naturelle, selon laquelle le virus serait passé de la chauve-souris à l’humain probablement via un animal-hôte intermédiaire, et celle de l’accident de laboratoire, puisque l’on sait que l’institut de virologie de Wuhan, laboratoire classé P4 (ce qui signifie qu’il abrite des microorganismes hautement pathogènes), travaillait sur le RaTG13, un virus de chauve-souris proche du SARS-CoV-2.
Mais ces deux théories n’ont pas toujours été appréciées de la même manière. Le 17 mars 2020, alors que des centaines de millions de personnes sont déjà confinées dans le monde, la revue Nature publie « The Proximal Origin of SARS-CoV-2 », l’un des articles les plus diffusés de l’histoire puisqu’il a été téléchargé 5,7 millions de fois et cité dans 2 650 publications. Ecrit par cinq scientifiques anglo-saxons dont Kristian Andersen, l’un des grands experts américains de l’immunologie, l’article conclut de façon quasi-certaine que « le SARS-CoV-2 n’est pas une construction de laboratoire ou un virus manipulé à dessein ».
Dès lors, l’hypothèse que la pandémie soit due à une fuite de laboratoire est reléguée au rang de théorie du complot, à tel point que son évocation est censurée sur les réseaux sociaux. Il faudra attendre plus d’un an pour que la possibilité que la pandémie soit d’origine humaine soit de nouveau sérieusement envisagée par les scientifiques.
70 % de probabilité que le virus provienne d’un laboratoire, selon un expert du coronavirus
De là, la naissance d’une autre théorie du complot, très prisée dans les rangs du parti républicain aux Etats-Unis, celle selon laquelle l’origine humaine de l’épidémie aurait été sciemment cachée au public par les autorités scientifiques afin d’éviter une crise diplomatique (voire pire) avec la Chine. Des échanges de mails récemment rendus publics dans les médias états-uniens grâce à la loi américaine sur la liberté d’accès aux informations donnent du grain à moudre aux tenants de cette théorie. Si certains de ces courriers avaient déjà été publiés ces derniers mois, ils étaient en grande partie caviardés.
On découvre dans ces messages que l’article « The Proximal Origin of SARS-CoV-2 » a donné lieu à de nombreux échanges en février 2020, préalables à sa publication, entre ses auteurs et divers éminents scientifiques américains dont le Pr Anthony Fauci, principal conseiller scientifique de la Maison Blanche, et Ron Fouchier célèbre pour avoir mené des expériences dites de « gain de fonction » rendant des virus plus pathogènes artificiellement. Une intervention extérieure qui n’a jamais été évoquée par les auteurs de l’article, ce qui pose évidemment la question du conflit d’intérêts, notamment quand on sait que Fouchier a collaboré avec le laboratoire de virologie de Wuhan.
Surtout, ces nouveaux documents rendus publics témoignent que la thèse de la fuite de laboratoire est initialement loin d’être considérée comme loufoque, bien au contraire. Tous les scientifiques qui participent à ces discussions au sommet s’étonnent de la proximité du SARS-CoV-2 avec le RaTG13 conservé au laboratoire de Wuhan mais également de la présence dans la structure du virus d’un site de clivage de furine, qui favorise l’infection et n’est pas présent dans cette famille de coronavirus. Mike Farzan, découvreur du récepteur du SARS, estime alors à 70 % les risques que le virus provienne d’un laboratoire. Plus prudent, Kristian Andersen constate que « les preuves scientifiques ne sont pas suffisamment concluantes » pour trancher entre l’origine naturelle et l’accident de laboratoire.
Qui veut la peau d’Anthony Fauci ?
Pourtant, Andersen et ses collègues finissent par se ranger à l’avis de Ron Fouchier, qui considère comme impossible que le virus qui commence alors à se propager dans le monde soit sorti d’un laboratoire et livrent donc un article à l’avis très tranché. Interrogé sur l’hypothèse de la fuite de laboratoire lors d’une conférence de presse en avril 2020, Anthony Fauci renvoie à l’article de Nature, écrit selon lui par « un groupe de virologues évolutionnistes hautement qualifiés », sans jamais évoquer sa participation à son élaboration.
Qu’est ce qui a poussé les plus éminents scientifiques anglo-saxons à discréditer la thèse de la fuite de laboratoire après l’avoir sérieusement envisagée ? Difficile de le dire, tous les échanges de mails n’ayant pas encore été rendus publics. Bien sûr, tout ceci ne prouve ni que le SARS-CoV-2 se soit échappé d’un laboratoire, ni que cette hypothèse ait été délibérément dissimulée. Pour Andersen, il ne faut y voir qu’un « exemple classique de la méthode scientifique où une hypothèse préliminaire est rejetée en faveur d’une hypothèse concurrente après que davantage de données soient disponibles ».
Mais pour certains membres du parti républicain, qui viennent de prendre le contrôle de la chambre des représentants, il n’y a pas de doute : les autorités sanitaires américaines et en premier lieu le Pr Anthony Fauci, qui s’apprête à quitter ses fonctions de directeur de l’institut national des maladies infectieuses (NIAD), ont caché aux Américains le fait que le virus se soit échappé d’un laboratoire. Leur motivation : éviter une guerre avec la Chine mais également cacher leur implication dans l’affaire, puisque l’institut national de la santé (NIH) aurait financé en 2021 des expériences de gain de fonction menées à Wuhan. « La carrière fédérale du Dr Fauci touche à sa fin, mais l’enquête du Congrès sur ses efforts pour dissimuler les origines du Covid-19 ne fait que commencer » a récemment lancé un ténor du parti républicain.
Nicolas Barbet
jim.fr
Covid : un rapport accablant de l’IGAS sur la gestion de la première vague de Covid
Publié le 04/01/2023
Le journal le Parisien révèle les grandes lignes d’un rapport resté secret de l’IGAS, qui décrit la désorganisation qui régnait au ministère de la Santé lors de la première vague de la pandémie de Covid.
Beaucoup de choses ont été dites et écrites et beaucoup le seront encore sur ces quelques mois de 2020 où la France a été prise par surprise par la Covid-19 et où l’ensemble de la population a été confinée, tandis que plus de 25 000 personnes perdaient la vie. Déjà fin juin 2020, Olivier Véran, ministre de la Santé d’alors, s’interrogeait sur la manière dont la crise avait été gérée et avait donc commandé à l’inspection générale des affaires sociales (IGAS) un rapport sur la question.
Ce document, remis au gouvernement en novembre 2020 et intitulé “retour d’expérience du pilotage de la réponse de l’épidémie de Covid-19" est longtemps resté secret. Selon les journalistes du Parisien qui en révèlent ce mercredi les grandes lignes, il leur a fallu plus de deux ans pour mettre la main sur ce rapport. Toutes les voies officielles avaient jusque-là échoué, les journalistes (qui n’indiquent pas comment ils ont finalement obtenu le rapport) ayant essuyé le refus de l’IGAS, de la commission d’accès aux documents administratifs (CADA) et de la justice administrative.
25 organigrammes en 3 mois
Ce document particulièrement accablant décrit la désorganisation qui régnait au sein du ministère de la Santé au début de la pandémie et son manque de réactivité. Le 27 janvier, alors que des premiers cas sont signalés en France et que le confinement a déjà démarré en Chine, la gestion de la crise est confiée au centre opérationnel de régulation et de réponse aux urgences sanitaires et sociales (Coruss). Comptant 11 agents seulement, ce comité qui n’a jamais eu à affronter de crise majeure se retrouve rapidement sous-dimensionné.
Il faudra attendre le 10 mars, soit une semaine seulement avant le confinement, pour que l’on commence à venir chercher à droite à gauche des “agents de tout profil” sans compétence adéquate pour compléter les effectifs. Autre écueil : jusqu’à la mi-mars, la direction des opérations est confiée à Jérôme Salomon, directeur général de la Santé (DGS). Mais l’infectiologue, qui cumule des fonctions de directeur stratégique, scientifique et opérationnel, est rapidement débordé. “Une seule personne ne peut pas assurer des fonctions aussi lourdes” résument les agents de l’IGAS.
La cellule interministérielle de crise n’est finalement déclenchée que le 17 mars, jour du confinement. Au manque de réactivité va se substituer un trop plein de mobilisation stérile. Des cellules dédiées apparaissent à côté du centre de crise (cellule communication, tests, masques, publics précaires...) et l’IGAS parle “d’absence d’organisation structurée et durable” : entre début mars et fin juin, 25 organigrammes différents sur la direction de la crise se succèdent. “L’organisation de la crise a connu un éclatement tel qu’au cours de la mission, aucun acteur rencontré n’a semblé en avoir une vision claire et exhaustive” résument les auteurs du rapport.
Les Ehpad abandonnés
Une désorganisation illustrée par le fameux fiasco des masques. En principe, la mission est du ressort de Santé Publique France (SPF), mais “étant donné la nécessité d’acheter massivement à l’international, SPF se révèle rapidement sous-dimensionnée” constate l’IGAS. Une cellule logistique interministérielle, qui s’appuie essentiellement sur des agents extérieurs au ministère, est donc créé pour épauler SPF, mais les relations entre cette cellule et SPF s’avèrent rapidement exécrables, rendant l’organisation des opérations encore plus difficile. SPF est notamment accusée de pinailler sur des détails légaux, notamment en demandant des “lettres de saisine” pour assurer “la contractualisation des marchés”.
Fiasco également sur la gestion du début de l’épidémie dans les Ehpad, pourtant particulièrement vulnérables face au virus. Le rapport indique notamment que lorsque le 30 janvier, Jérôme Salomon émet une note sur le fonctionnement du centre de crise sanitaire, elle n’est pas envoyée à la direction générale de la cohésion sociale (DGCS), en charge des établissements pour personnes âgées. Les Ehpad sont de nouveaux oubliés lors de la publication du premier “guide méthodologique Covid-19" le 20 février.
Deux cellules de crise, celle du ministère et celle de la DGCS, gèrent la situation en parallèle, ce qui ne fait que rajouter à la confusion. Il faudra ainsi attendre le 6 avril, alors que l’épidémie est au plus haut, pour une consigne nationale de dépistage dans les Ehpad soit diffusée. Tous les acteurs de terrain notent que les directives étaient “trop nombreuses, difficiles à lire et dans certains cas inapplicables”. La remontée des informations est également rendue difficile par “des modes de comptage différents et des sources différentes” et ce n’est que le 2 avril qu’un premier bilan de l’épidémie dans les maisons de retraite est connu. Au total, 22 000 résidents d’Ehpad décèderont durant les 9 premiers mois d’épidémie.
Zéro pointé pour la recherche
La recherche française en prend également pour son grade dans ce rapport de l’IGAS. Là encore, la plus grande confusion règne, SPF n’ayant “pas joué le rôle de coordination de l’expertise attendu au regard de ses missions légales” écrivent les agents de l’IGAS. Des projets de recherches “redondants et trop segmentés” se multiplient, la plupart n’arrivant pas à leur terme en raison de difficultés à recruter des patients : à la fin du mois d’août, seulement 2,5 % des patients hospitalisés en France ont participé à un essai clinique. A contrario, l’IGAS cite l’exemple de l’étude britannique Recovery, qui a recruté 15 000 patients et a obtenu des “résultats particulièrement intéressants”.
Au final, ce rapport accablant pourrait peut-être un jour devenir une pièce à conviction : il a été versé au dossier de l’enquête de la Cour de Justice de la République, qui instruit depuis plus de 2 ans sur la gestion du début de la pandémie. Pour le moment, seul l’ancienne ministre de la Santé Agnès Buzyn a été mise en examen.
Nicolas Barbet
jim.fr
— -
L’avis de la CADA
Avis 20211463 Séance du 15/04/2021
Communication du rapport concernant le retour d’expérience portant sur les modalités de pilotage et de gestion de l’épidémie de Covid-19.
Madame X, pour le quotidien « X », a saisi la commission d’accès aux documents administratifs, par courrier enregistré à son secrétariat le 24 février 2021, à la suite du refus opposé par la Cheffe de l’IGAS à sa demande de communication du rapport concernant le retour d’expérience portant sur les modalités de pilotage et de gestion de l’épidémie de Covid-19.
La commission rappelle que les rapports d’audit et autres diagnostics demandés par une personne publique ou une personne privée chargée d’une mission de service public, dans le cadre de l’exercice de cette mission, revêtent le caractère de documents administratifs, communicables à toute personne qui en fait la demande, en application de l’article L311-1 du code des relations entre le public et l’administration, sous réserve, d’une part, qu’ils soient achevés, c’est-à-dire en l’espèce qu’ils aient été remis à leur commanditaire et, d’autre part, qu’ils soient dépourvus de caractère préparatoire.
Elle précise que de tels rapports ne peuvent revêtir un caractère préparatoire, au sens des dispositions du livre III du code précité, que lorsqu’ils sont destinés à éclairer l’autorité administrative en vue de prendre une décision administrative déterminée et que cette décision n’est pas encore intervenue, ou que l’autorité administrative n’a pas manifestement renoncé à la prendre, à l’expiration d’un délai raisonnable. Dans un tel cas, le caractère préparatoire d’un rapport s’oppose en principe à la communication immédiate de l’ensemble de son contenu, à moins, toutefois, que les éléments de ce rapport préparant une décision ultérieure ne soient divisibles de ses autres développements.
En l’espèce, en réponse à la demande qui lui a été adressée, la Cheffe de l’IGAS a informé la commission que le rapport sollicité, remis à son commanditaire le 26 novembre 2020, revêt un caractère préparatoire à tout le moins pour l’ensemble de la période de crise lié à la pandémie de Covid-19, dès lors qu’il explore des pistes d’organisation ou de réorganisation internes au ministère des solidarités et de la santé, qui constituent des références utiles dans le cadre de l’adaptation continue du dispositif de gestion de cette crise.
Au regard de ces éléments, la commission estime que ce rapport conserve, en l’état, un caractère préparatoire, et émet donc un avis défavorable à sa communication.
Où le Covid long fait long feu…
Publié le 03/01/2023
La persistance ou l’apparition de symptômes de longue durée après l’infection par le SARS-CoV-2 sont dénommées « affection post-Covid-19 » ou plus communément « Covid long ». Selon la définition consensuelle de l’Organisation Mondiale de la Santé (OMS), « le Covid long se manifeste généralement dans les 3 mois suivant l’infection initiale au SARS-CoV-2, et se caractérise par des symptômes persistants au moins 2 mois, lesquels, d’une part ne peuvent pas être expliqués par d’autres diagnostics, et, d’autre part, ont un impact sur la vie quotidienne ». Asthénie, essoufflement et dysfonctionnement cognitif sont des symptômes fréquemment retrouvés, mais la liste de l’OMS en comprend 22 autres dont, le malaise après l’effort, une fièvre intermittente, la perte du goût ou de l’odorat, la dépression [1, 2, 3].
Selon la Haute Autorité de Santé, « 4 % des répondants d’un panel de volontaires adultes résidant en France métropolitaine présentent les critères d’une affection post-Covid-19 selon la définition consensuelle de l’OMS, soit 30 % des personnes ayant eu une infection par le SARS-CoV-2 plus de trois mois auparavant. Cela correspondrait à 2,06 millions de personnes de plus de 18 ansconcernées dans la population française début avril 2022 » (Résultats de l’enquête Affection post-Covid, 22 mars - 8 avril 2022) [4].
Essentiellement trois types de symptôme
De nombreuses études ont été conduites sur la symptomatologie des Covid longs. Un groupe de travail international a analysé chez 1,2 millions de patients, à partir de 54 études complétées par 2 bases de données médicales, 3 symptômes parmi les plus fréquents de Covid long, après la pandémie de 2020-2021, : la fatigue durable avec douleurs physiques et modifications de l’humeur, les troubles cognitifs et les symptômes respiratoires persistants. Il ressort de cette étude, publiée en octobre 2022, que 6,2 % des patients ayant présenté une infection symptomatique à SARS-CoV-2 et ayant survécu à la phase aiguë durant la période 2020-2021, ont souffert d’au moins un des trois symptômes analysés, toujours présent au 3e mois. La grande majorité des Covid longs ont disparu avec le temps [5, 6].
Mais ces symptômes non pathognomoniques peuvent aussi être attribués à d’autres causes et donc ne pas être liés à l’infection par le SARS-CoV-2, comme par exemple dans des infections virales (grippe, Ebola, EBV) et non virales (fièvre Q, Lyme, giardase) [5].
Une question se pose ainsi : croire que l’on a été infecté par le SARS-CoV2 peut-il être associé aussi, comme chez des sujets réellement infectés, à des symptômes persistants évoquant ainsi un Covid long ?
Pour tenter de répondre à cette question, une équipe française a étudié l’association de la Covid-19 autodéclarée à des résultats des tests sérologiques, chez des sujets décrivant des symptômes physiques persistants (Covid long). Nous en présentons les résultats publiés dans le JAMA International Medicine en novembre 2022 [7].
Il s’agit d’une étude transversale conduite pendant la pandémie de Covid-19, et portant sur 26 823 adultes volontaires de la cohorte française CONSTANCES* basée sur la population, inclus entre 2012 et 2019 qui ont pris part aux enquêtes emboîtées SAPRIS et SAPRIS-SERO**. Entre mai et novembre 2020, un test immuno-enzymatique a été utilisé pour détecter les anticorps anti-SARS-CoV-2. Entre décembre 2020 et janvier 2021, les participants devaient déclarer le cas échéant, s’ils pensaient avoir été infectés par le virus de la Covid-19 et s’ils avaient eu des symptômes physiques au cours des 4 semaines précédentes, ayant persisté pendant au moins 8 semaines. Les participants qui ont dit avoir eu une Covid-19 seulement après avoir effectué le test sérologique ont été exclus. Des régressions logistiques pour chaque symptôme persistant en tant que résultat ont été calculées dans des modèles incluant à la fois la maladie Covid-19 autodéclarée et les résultats du test sérologique ; il y a eu ajustement sur l’âge, le sexe, le revenu et le niveau d’éducation.
Association avec la conviction d’avoir été infecté plus qu’avec la sérologie
Les 26 823 adultes inclus (74,8 % des sujets volontaires) avaient tous des données complètes pour les tests sérologiques et l’infection autodéclarée. L’âge moyen était de 49,4 ans ; 51,2 % étaient des femmes.
L’infection autodéclarée était positivement associée aux symptômes physiques persistants, avec des rapports de cotes allant de 1,44 (intervalle de confiance à 95 % IC 95 %, 1,08-1,90) à 16,61 (IC 95 %, 10,30-26,77), à l’exception des troubles auditifs (rapport de cotes, 1,38 ; IC 95 %, 0,76-2,51), des douleurs articulaires (rapport de cotes, 1,32 ; IC 95 %, 0,98-1,80) et des troubles du sommeil (rapport de cotes, 1,12 ; IC 95 %, 0,87-1,44).
Un résultat de test sérologique positif pour le SARS-CoV-2 n’était positivement associé qu’à une anosmie persistante (odds ratio, 2,59 ; IC à 95 %, 1,57-4,28), même en restreignant les analyses aux participants qui attribuaient leurs symptômes à une infection au Covid-19. Des ajustements supplémentaires pour l’auto-évaluation de la santé ou les symptômes dépressifs ont donné des résultats similaires. Il n’y avait pas d’interaction significative entre les croyances et les résultats des tests sérologiques.
Les auteurs concluent que les symptômes physiques persistants après une infection au Covid-19 peuvent être davantage associés à la croyance d’avoir été infecté par le SARS-CoV-2 qu’à une Covid-19 confirmée en laboratoire.
Ils concluent aussi que la Covid-19 autodéclarée était associée à la plupart des symptômes physiques persistants, tandis que l’infection par le SARS-CoV-2 confirmée en laboratoire était associée uniquement à l’anosmie. Ainsi pour eux, les symptômes physiques persistants après une infection au Covid-19 ne doivent pas être automatiquement attribués au SARS-CoV-2 ; une évaluation médicale complète peut être nécessaire pour éviter d’attribuer à tort les symptômes au virus et ainsi de porter par erreur un diagnostic de « Covid long ».
*Constances est une cohorte épidémiologique « généraliste » constituée d’un échantillon représentatif de 200 000 adultes âgés de 18 à 69 ans à l’inclusion, consultants des Centres d’examens de santé (CES) de la Sécurité sociale. https://www.constances.fr/
** SAPRIS-SERO est le volet biologique du projet SAPRIS, une grande enquête pilotée par l’Inserm sur le COVID-19 qui s’appuie sur les grandes cohortes épidémiologiques Constances, E3-E4N, NutriNet-Santé et Elfe-Epipage2.
Pr Dominique BAUDON
RÉFÉRENCES
- [1] Organisation mondiale de la Santé. 2021. Une définition de cas clinique pour l’affection post-COVID-19 établie par un consensus Delphi, 6 octobre 2021. https://apps.who.int/iris/handle/10665/347764
- [2] Nehme M et coll. COVICARE TEAM. : COVID-19 symptoms : longitudinal evolution and persistence in outpatient settings. Ann Intern Med. 2021 ;174(5):723-725. doi:10.7326/M20-5926
- [3] Mahase E : Covid-19:what do we know about “long covid” ? BMJ. 2020 ;370:m2815. doi:10.1136/ bmj.m2815
- [4] L’affection post-COVID-19 (aussi appelée COVID long) en France. Résultats de l’enquête Affection post- COVID, 22 mars - 8 avril 2022. Saint-Maurice : Santé publique France, 5 p. Directrice de publication : Pr Geneviève Chêne. Dépôt légal : 21 juillet 2022
- [5] Global Burden of Disease Long COVID Collaborators, et coll. : Estimated Global Proportions of Individuals With Persistent Fatigue, Cognitive, and Respiratory Symptom Clusters Following Symptomatic COVID-19 in 2020 and 2021. JAMA. 2022 Oct 25 ;328(16):1604-1615. doi : 10.1001/jama.2022.18931. PMID : 36215063.
- [6] https://www.jim.fr/medecin/pratique/recherche/e-docs/combien_de_fatigue_de_troubles_respiratoires_ou_cognitifs_persistants_apres_covid_19_symptomatique__194779/document_actu_med.phtml. Publié le 08/11/2022
- [7] Joane Matta, et coll. : Association of Self-reported COVID-19 Infection and SARS-CoV-2 Serology Test Results With Persistent Physical Symptoms Among French Adults During the COVID-19 Pandemic. JAMA Intern Med. 2022 ;182(1):19-25. doi:10.1001/jamainternmed.2021.6454 Published online November 8, 2021.
Source : jim.fr
Covid-19 : Retour sur la bataille des lits de réanimation
Quentin Haroche | 15 Mars 2024
Jim.r
Dans une étude approfondie, la Drees revient sur l’évolution du nombre de lits de réanimations entre 2020 et 2022 pour faire face à l’afflux de patients atteints de la Covid-19.
Il y a quatre ans presque jour pour jour, le 16 mars 2020, Emmanuel Macron mettait en place le tout premier confinement pour tenter de freiner la pandémie de Covid-19. L’objectif de cette mesure de restriction de liberté sans précédent était notamment d’éviter la submersion des services de réanimation et de leur permettre de faire face à l’afflux de patients atteints par la maladie. Tout au long de ces deux ans de crise, le gouvernement et les Français ont suivi avec attention le taux d’occupation des services de réanimation, dont dépendait bien souvent la dureté des mesures sanitaires mises en place par les autorités. Dans une étude publiée ce jeudi, la Drees, le service des statistiques du ministère de la Santé, revient sur l’évolution du nombre de lits de réanimation tout au long de la pandémie.
Pour rappel, les lits de soins critiques comprennent les lits de réanimation, les lits de soins intensifs et les lits de surveillance continue, ces différentes unités étant définies selon la gravité de l’état de santé des patients qu’ils prennent en charge. Pour faire face à l’afflux de patients atteints de la Covid-19, le nombre de lits de soins critiques a augmenté de 3,6 % en 2020 par rapport à 2019, alors qu’il n’augmentait que de 1,1 % par an en moyenne lors de la décennie précédente. Le nombre de lits de réanimation est celui qui a connu l’augmentation la plus importante : après avoir stagné depuis 2013 (+ 0,1 % par an en moyenne), il a grimpé de 14,5 % en 2020, passant de 5 420 lits au 31 décembre 2019 à 6 210 un an plus tard.
Près de 9 200 patients en réanimation en avril 2020
Le nombre de lits de réanimation a ensuite diminué en 2021 (- 3,8 %) et en 2022 (- 4,6 %) mais est tout de même resté supérieur au niveau d’avant pandémie : au 31 décembre 2022, on comptait 5 700 lits de réanimation, soit 5,2 % de plus qu’avant la pandémie. Certains de ces lits de réanimation correspondent à de nouvelles unités ouvertes pour donner suite à des autorisations temporaires, tandis que d’autres sont des lits de soins critiques qui ont été reconvertis en lits de réanimation. Ainsi, le nombre de lits de soins intensifs n’a augmenté que de 0,6 % en 2020 et 2021 (contre + 1,6 % par an en moyenne les années précédentes) tandis que le nombre de lits de surveillance continue a diminué de 1,4 % en 2020.
Cette fluctuation du nombre de lits de réanimation, au gré des vagues épidémiques, était bien sûr rendue nécessaire par le nombre très important de patients à prendre en charge. Lors de la première vague épidémique au printemps 2020, ce sont près de 9 200 patients qui ont dû être pris en charge en réanimation, soit deux fois plus que le nombre maximal constaté en temps normal depuis 2013. Au cours de la période 2020-2022, les patients Covid-19 ont ainsi représenté 11,3 % des personnes pris en charge en réanimation et 21,1 % des journées d’hospitalisation en réanimation, en raison de séjours en réanimation en moyenne deux fois plus longs pour les patients atteints de la Covid-19.
Les transferts de patients ont permis d’éviter la saturation
Mais des focus sur les pics épidémiques qu’a connus la France permettent de mieux comprendre les difficultés qu’ont pu rencontrer les services de réanimation lors de certaines périodes. Les patients atteints de la Covid-19 ont ainsi représenté 61 % des patients en réanimation en avril 2020 et 50 % en avril 2021. L’augmentation du nombre de lits de réanimation a cependant permis d’empêcher la saturation des services : le taux d’occupation des lits sur l’année a atteint 89 % en 2020 et 95 % en 2021, contre 88-89 % en temps normal. En 2022, ce taux est redescendu à 86 %, soit moins que lors des années précédant la pandémie.
L’étude de la Drees montre également que certaines régions ont connu plus de difficultés que d’autres durant ces deux années de crise sanitaire à l’hôpital. Durant la première vague, ce sont l’Ile-de-France et le Grand Est qui ont été le plus touchés. Fin mars 2020, alors que le nombre de lits nécessaires au niveau national correspondait à 140 % des capacités normale en réanimation, ce taux atteignait 226 % dans le Grand Est et 250 % en Ile de France. Les transferts de patients vers des régions moins touchées ont alors permis d’éviter une saturation des services rappelle la Drees. Lors des vagues suivantes, ce sont les départements d’outre-mer qui ont été les plus durement touchés : en août 2021, les hôpitaux martiniquais ont dû prendre en charge plus de 120 patients en réanimation, malgré une capacité initiale de seulement 30 lits.
Rappelons qu’en mars 2022, au sortir de la crise sanitaire, le gouvernement avait promis de maintenir le nombre de lits de réanimation au-dessus des 6 000, afin notamment de répondre au vieillissement de la population. Un objectif qui n’aura donc pas été atteint, la faute sans doute à la difficulté d’attirer des soignants et notamment des infirmières vers la réanimation.
— -
Arnaud BASSEZ
IADE/Formateur AFGSU-NRBC
Administrateur