HYPOTHERMIE
Cheval de bataille, objet de discorde entre l’équipe d’anesthésie et l’équipe chirurgicale dont les buts sont opposés en la matière, le chirurgien a besoin d’opérer en ayant un champ opératoire le plus dégagé possible, l’équipe d’anesthésie ayant à cœur de réchauffer dès l’entrée dans la chambre froi...la salle d’opération, le patient.
Mettons-nous l’espace d’un instant dans la peau d’un futur opéré, nu à peine recouvert d’une chemise légère ou d’un pyjama en papier, qui s’allonge sur une table souvent humide et seulement recouverte d’un drap plié et qui une fois endormi perd son réflexe de frisson et est donc incapable de se réchauffer par lui-même, surtout après avoir été largement badigeonné de bétadine à température ambiante qui participe à la perte calorique. Si en plus le patient a une laparotomie ou une xypho-pubienne, voire une incision selon les rites initiatiques chirurgicaux qui veut que "grand chirurgien, grande incision", on entrevoit d’ici les effets de l’hypothermie sur les patients.
DÉFINITION
Un organisme homéotherme présente une hypothermie lorsque la température profonde est inférieure de plus d’une déviation standard à la température moyenne soit en pratique une température centrale inférieure à 35°C pour l’ espèce.
PHYSIOPATHOLOGIE
Rappels de physiologie :
• La température est un « paramètre d’ état » qui correspond à l’ agitation des atomes. L’ unité en est le degré Celsius (°C) , l’unité de chaleur est la calorie qui est par définition la quantité de chaleur nécessaire pour porter 1 gramme d’ eau de 14,5° à 15,5° C. L’ unité d’ énergie internationale est le Joule ; 1 calorie = 4,187 Joules = 0,0012 Watt h
• Les transferts de chaleur se produisent dès qu’ existe une différence de température entre deux milieux. Ils sont de 3 types :
a) la conduction : par contact direct,
exemple : patient sur la table d’opération
b) la convection : met en jeu un fluide servant d’ échangeur thermique
exemple. : circulation sanguine, flux laminaire ventilation pulmonaire
c) la radiation : échange de chaleur par émission de photons donc de lumière (Infra-rouge)
• Thermogenèse, Thermolyse
Thermogenèse : Production de chaleur par l’organisme
– Métabolisme de base : 80 Watts
– x 2 ou 3 lors de la marche
– x 10 ou 20 effort violent ( sports )
Thermolyse : Perte de chaleur par :
- radiation = 60%
- évaporation 22%
- convection = 15%
- conduction = 3%
EFFET ÉOLIEN
Il est souvent légendé comme température ressentie, bien qu’il soit en réalité un nombre sans unité. Ceci signifiant seulement que la valeur équivaut à la sensation ressentie sur la peau par une journée calme à cette température. La formule de calcul du refroidissement éolien est la suivante pour avoir un nombre similaire à des degrés Celsius :
– R = 13,~!12 + 0,~!6215 \,T + (0,~!3965 \, T - 11,~!37) \times V^0,~!16
où T est température ambiante exprimée en °C et V est la vitesse du vent exprimée en km/h. Le refroidissement éolien n’est pas défini pour des vitesses de vent inférieures à 5 km/h.
Voir le tableau de l’effet éolien
Exposition au froid = stimulus douloureux ▬► Récepteurs périphériques captent ce stimulus douloureux ▬► stimulation de l’ hypothalamus
Conséquences (3 localisations différentes) :
– ▬► stimulation du Cortex ▬► réponse = Adaptation comportementale
– ▬► stimulation des centres bulbaires ▬► réponse = Adaptation physiologique
(augmentation de la fréquence respiratoire et cardiaque)
– ▬► stimulation récepteurs cutanés ▬► réponse = Adaptation mécanique = Frissons
• Régulation thermique
– Thermo récepteurs = périphériques, centraux
– Centres régulateurs : hypothalamiques, Médullaires
(= réponse neuro-végétative)
Mécanismes :
- réaction centrale « contrôlée »
exemple : sujet se couvre, sensation de chaud et de froid :
commande directe des mécanismes thermogenèse
- exemple : frissons
– isolement thermique au niveau de l’ écorce : vasoconstriction
– stimulation des glandes sudoripares.
• Distribution de la température :
La température corporelle n’est pas uniforme
– L’ écorce :
L’écorce est sacrifié au profit du noyau central.
Depuis la peau jusqu’ à 2,5 cm de profondeur.
Zone tampon équivalente à une couverture.
Température inhomogène
– Le noyau central :
Température uniforme à 37°C ne variant que de plus ou moins 0,5 °C pendant les différentes phases.
La seule température à connaître est la température centrale :
- mesure idéale noyau central
- sonde œsophagienne
- thermomètre rectal
- thermomètre tympanique
- thermomètre collé sur la peau
• Physiopathologie
2 types d’ hypothermie :
1. Défense maxima ou hypothermie compensée :
sujet sain, régulation thermique de l’organisme dépassée par l’ intensité du froid.
Évolution en 3 temps :
• ler temps : vasoconstriction ▬► chute de la température cutanée
• 2ème temps : organisme va essayer de produire de la chaleur
frissons : (activité musculaire involontaire) permet de produire 5 à 6 fois le métabolisme de base = hypothermie légère = le corps est encore capable de lutter.
• 3ème temps : production chaleur métabolique
température centrale, altération de la thermorégulation
– arrêt du frisson à 32° puis rigidité musculaire, 30° production de chaleur proche du métabolisme de base. = hypothermie grave = l’organisme est dépassé
– 27 ° : disparition de la rigidité musculaire
2. Défense minima ou « non compensée » :
(Le système thermorégulateur est déjà altéré au départ)
malnutrition : couche adipeuse cutanée faible
– âge :
- nouveau né ; rapport surface corporelle, poids défavorable
- vieillard ; diminution réaction vasoconstriction, frissons
dépression du système thermorégulateur : drogues, alcool, barbituriques
causes endocriniennes : hypothyroïdie, hypopituitarisme
atteinte centrale du centre thermorégulateur : tumeur cérébrale, hématome sous dural...
EPIDEMIOLOGIE
2 types
-accidentelles pathologie sportive : ski, alpinisme, plongée
organique : hypothyroïdie, AVC,
-toxicologique : alcool, médicamenteuse,
hypothermie provoquée :
- chirurgie cardiaque
- bloc opératoire, anesthésie
< conditions météorologiques ;
< conditions socio économiques
chômage, SDF = 69
isolement, exclusion = 39,4
mauvaise condition de chauffage.
< limite inférieure de la température compatible avec la vie
indéterminée
- littérature = 15,2°C et 9°C
- chute dans l’ eau à 6 °▬► survie 15 minutes
- 15° ▬► survie 4 h
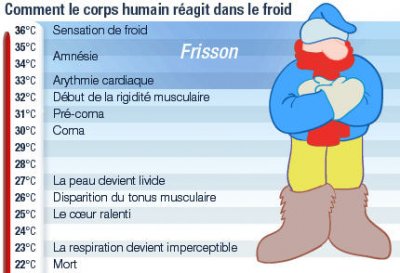
SYMPTOMATOLOGIE
4 stades :
- 1. Hypothermie légère > 34 ° (mortalité 7 %)
- 2. Hypothermie modéré : 34° - 32 ° (mortalité 40 %)
- 3. Hypothermie grave : 32° - 27° (mortalité 62 %)
- 4. Hypothermie profonde : < 27°
A- SIGNES NEUROLOGIQUES
Quand la température corporelle diminue, il y a rapidement adaptation neurologique : le cerveau va s’auto protéger en diminuant ses besoins en oxygène + protection du noyau (cerveau et appareil cardio-respiratoire).
– Hypothermie légère :
Conscient, frissons ++, peau froide
Les besoins du cerveau sont diminués en oxygène, d’où augmentation de la résistance du cerveau à l’ischémie.
– A 32° : disparition du phénomène de frissons, le corps ne peut plus produire de chaleur = seuil de gravité des hypothermes
– En dessous de 32° : agitation importante, dysarthrie. L’amnésie est de règle.
– En dessous de 30° : hypertonie musculaire, hyper réflexie ostéotendineuse, myosis. le coma s’installe progressivement
– En dessous de 28° : l’hyper reflexie fait place à une hyporeflexie , la rigidité musculaire persiste, une mydriase fait place au myosis.
– En dessous de 22° : la mydriase devient aréactive, un état de mort apparente s’installe
B SIGNES CARDIO VASCULAIRES
C’est l’appareil qui souffre le plus du froid.
L’hypothermie tue par troubles cardiaques
La pression artérielle : peu modifiée jusqu’à 30°
Puis se pince ( TA systolique, TA diastolique)
Puis elle chute progressivement
La variation de pression artérielle est essentiellement due à une baisse du débit cardiaque. Cette baisse du débit cardiaque est due à :
- Hypovolémie
- Baisse fonction contractile du myocarde
- Bradycardie progressive
Les troubles du rythme cardiaque : Elles sont fréquentes.
Tout peut se voir
Bradycardie progressive avec la baisse de la température
– < 28° apparition d’une fibrillation auriculaire
– <20° disparition du pouls périphérique et des bruits du cœur
Lors du réchauffement, il peut se produire une fibrillation auriculaire mortelle ou une bradycardie aiguë avec insuffisance cardiaque gauche irréversible .
Les signes ECG :
– troubles de la repolarisation
– Élargissement du QRS
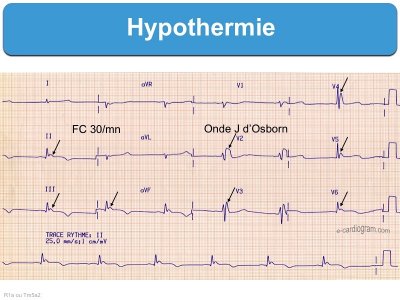
– Onde J d’Osborn : Il s’agit d’une déflexion positive visible (au moins 1 mm, jusqu’à 10 mm), fine ou légèrement arrondie au sommet, qui débute à la fin du complexe QRS, avant la fin de l’onde R, diffuse dans presque toutes les dérivations.
Elle peut apparaître à partir de 35°5 C et son amplitude augmente avec la profondeur de l’hypothermie. Elle correspond à un courant de lésion. Elle ne constitue pas un signe de mauvais pronostic dans le cadre d’une hypothermie.
(en savoir plus sur les ondes de l’ECG)
C SIGNES RESPIRATOIRES
Le rythme respiratoire est accéléré jusqu’à 32° puis apparaît une bradypnée franche et importante, pouvant conduire à des pauses respiratoires.
Les lésions anatomiques sont caractérisées par un œdème pulmonaire
D SIGNES RÉNAUX
à 30° le débit rénal est diminué de moitié (car diminution du débit cardiaque => diminution de la tension artérielle).
La diurèse diminue progressivement mais est réversible avec le réchauffement.
E – SIGNES BIOLOGIQUES
- Acidose progressive métabolique puis métabolique + respiratoire des l’apparition de la bradypnée
- Les gaz du sang restent difficilement interprétables, ils doivent être corrigés en fonction de la température réelle du patient .
- Hyperglycémie jusqu’à 32° ( lutte active). puis hypoglycémie progressive
- Insuffisance rénale progressive
ACCIDENT DU RÉCHAUFFEMENT
A – L’ AFTER DROP
CPK la plus fréquente => 1 ère cause de décès
Manipulation = mobilisation sang froid péri vers le noyau ( le cœur) _ refroidissement brutal du noyau = trouble du rythme = DC
Donc les hypothermes sont à mobiliser avec énormément de précaution surtout si la température < 32°C + isoler du froid le plus vite possible.
B – RÉCHAUFFEMENT INTEMPESTIF
2ème cause de décès
Un réchauffement de la périphérie va ouvrir le lit vasculaire, périphérique par une vasodilatation = augmentation du débit sanguin péri alors que le cœur reste à température initiale et ne modifie pas son débit = collapsus
C COMPLICATION BRONCHOPULMONAIRE
Baisse du réflexe du carrefour et inhalation au cour du réchauffement
D COMPLICATION RÉNALE
Libération de K, CPK, H. (résultat d’une lyse cellulaire) majorant l’acidose métabolique et crée ainsi une insuffisance rénal organique par Rhabdomyolyse.
E TROUBLES DU RYTHME
En dessous de 30° les hypothermes sont des patients susceptibles de faire un trouble du rythme cardiaque mortel. La moindre stimulation notamment les stimulations nociceptives peuvent crée des fibrillation surtout au alentour de 28.° de température corporelle. Ceci induit de grande précaution lors des prises en charge préhospitalières.
TRAITEMENT
BUT :
- Ne pas majorer l’hypothermie
- Soustraire au terrain
- Isoler le patient
- Attention aux manipulations
- Être le moins agressif possible
- Définir le degré d’hypothermie

MOYENS
Le réchauffement lent passif externe : ( hypotherme léger)
- Patient dans une pièce à 22 24 °C sous monitorage
- Couvertures, séchage
- La température remonte lentement en 3 4h à 37°C
- Gain : 0.5 à 1° /h
Le réchauffement rapide :
Réchauffement du noyau avant l’écorce
A Actif externe
- Couverture chauffante
- Matelas chauffant
Risques+++ after drop, collapsus de réchauffement
Gain : l à 2°/h
B Actif interne
- Perfusions chaudes ( 38°C)
Risque : collapsus de réchauffement
- Réchauffement de l’air inhalé (42°C) ( parachute thermique)
- Lavages gastriques (40°C)
- Dialyse péritonéale +++ très pratiquée pour hypotherme grave et profond
Gain : 1 à 4° C/h
- Thoracotomie
- Hémodialyse
- CEC ; rapide pour les hypothermes profond en ACR
Rare cas de survivant
Dr Laurent Chardin de l’hôpital de Moutiers (73)
l’article en PDF
§§§
La température en anesthésie. Que faire chez l’enfant ?
Dr Serge Dalmas,
Clinique d’Anesthésie
Hôpital Jeanne de Flandre
CHRU de Lille
L’article sur le site JLAR
L’enfant est d’autant plus susceptible de modifier sa température centrale que sa surface corporelle est proportionnellement plus élevée par rapport à celle de l’adulte. En effet les particularités morphologiques jouent un grand rôle dans la sensibilité à l’hypothermie (1) et au réchauffement (2).
I . Physiologie de la thermorégulation chez les nourrissons et les enfants
La température ambiante de neutralité thermique est de 28°C chez l’adulte et de 32°C chez le nouveau-né ; la température critique (température ambiante au-dessous de laquelle l’individu ne parvient plus à maintenir sa température centrale) est de 1°C chez l’adulte, mais de 23°C chez le nouveau-né. Un nouveau-né placé nu dans une pièce chauffée à 23°C se trouve donc dans la même situation qu’un adulte à qui l’on demanderait de sa déshabiller dans une chambre froide à 1°C. Les nouveau-nés, nourrissons et les jeunes enfants sont plus sensibles à l’hypothermie car les mécanismes de protection ou de production de chaleur sont moins performants. Ils ont un rapport surface cutanée sur volume plus élevé et une conductance cutanée thermique plus élevée (la peau est fine) entraînant une perte plus importante de chaleur. La zone de neutralité thermique, pour laquelle l’activité métabolique est la plus faible est étroite chez les nourrissons ; en dehors de cette zone le maintien d’une température centrale normale est associé à une augmentation de la consommation d’oxygène et une acidose métabolique.
Chez l’enfant à terme la consommation d’oxygène n’est pas corrélée à la température centrale mais au gradient entre température cutanée et température extérieure. Enfin pendant l’anesthésie une vasoconstriction cutanée peut permettre de limiter la chute de la température centrale.
Le processus de thermorégulation comprend trois étapes : les afférences thermo-sensorielles, la régulation centrale et la réponse efférente.
1. Les afférences thermiques sensitives
La sensibilité au froid serait transmise préférentiellement par les fibres A-Delta et la sensibilité au chaud par les fibres C. La plupart des informations thermiques sont ensuite transmises aux centres par le faisceau spino-thalamique situé au niveau de la corne antérieure de la moelle.
2. La régulation centrale
Au niveau de l’hypothalamus les informations en provenance de la peau, du névraxe et des tissus profonds sont comparées avec les seuils thermiques inférieur et supérieur et initient une réponse lorsque ces seuils sont dépassés.
L’intervalle de température ne déclenchant pas de réponse effectrice est étroit à l’état éveillé (0,2 °C) mais s’élargit notablement pendant l’anesthésie (environ 3,5°C).
Les mécanismes permettant à l’organisme de fixer un niveau de référence absolu de température ne sont pas connus. Ce niveau dépend de divers facteurs (rythme circadien, exercice, prise alimentaire, facteurs hormonaux, l’adaptation au froid ou à la chaleur, les agents anesthésiques). La régulation centrale est parfaitement fonctionnelle chez l’enfant. Les réponses sont déclenchées par les afférences en provenance de l’ensemble des tissus (température moyenne de l’organisme) et ne dépendent pas que du niveau de la température centrale. La température cutanée est à l’origine des réponses comportementales.
3. Les réponses efférentes
L’homéostasie thermique est maintenue lorsque la température dépasse les valeurs inférieure et supérieure grâce à des réponses actives : augmentation de la production de chaleur avec ou sans frisson, baisse de la dissipation de chaleur par vasoconstriction active ou application d’une couverture, augmentation de la perte de chaleur par vasodilatation, sudation, déshabillage.
3.1. La vasoconstriction cutanée est une réponse constante et précoce face à une hypothermie ; elle résulte d’un relarguage local de noradrénaline qui survient pour des températures inférieures à 35°C. L’augmentation de noradrénaline circulante peut entraîner une vasoconstriction pulmonaire avec un risque de retour en circulation fœtale chez le nouveau-né.
3.2. La production de chaleur résulte d’une augmentation du métabolisme par plusieurs mécanismes : augmentation de l’activité musculaire volontaire, involontaire (frisson) et la thermogénèse sans frisson.
3.2.1. Le frisson, retrouvé chez l’enfant de plus de six ans, peut multiplier la production de chaleur par quatre de manière transitoire et par deux de manière soutenue. Il est aboli pendant l’anesthésie, et peut se manifester au réveil.
3.2.2. La thermogénèse sans frisson est le mécanisme le plus important chez le nouveau-né, alors que le frisson prédomine chez l’enfant et l’adulte. Comparé à l’adulte, le nourrisson compense moins facilement une hypothermie en raison de l’absence de frissons et d’une réaction vasoconstrictrice moins intense. La perte de chaleur facilitée par les caractéristiques anatomiques, les capacités diminuées à produire de la chaleur et la réponse diminuée à l’hypothermie les rendent particulièrement vulnérables. La thermogénèse sans frisson est une augmentation de la production de chaleur par augmentation du métabolisme sans augmentation de l’activité musculaire. Elle résulte principalement d’une oxydation de la graisse brune mais peut aussi survenir dans le muscle, le foie, le cerveau et la graisse blanche. La graisse brune constitue 2 à 6% du poids du nourrisson et se trouve principalement entre les omoplates, autour des vaisseaux du cou, au niveau du creux axillaire, dans le médiastin et au niveau des reins et des surrénales.
C’est un tissu abondamment vascularisé et innervé par des terminaisons sympathiques, constitué de cellules multinuclées contenant de nombreuses mitochondries. Le froid entraîne à son niveau une libération locale de noradrénaline puis une augmentation du métabolisme. Outre un probable rôle du tissu adipeux brun dans le contrôle de la température corporelle et la combustion des graisses, la thermogenèse du tissu adipeux brun pourrait induire la satiété au niveau cérébral, la fin des prises de repas chez le bébé, et contrôler le rythme des repas. La diminution de la température centrale pourrait induire la demande de nourriture et la prise d’aliment. La prise d’aliments activerait le tissu adipeux brun qui produit de la chaleur. L’augmentation de la température centrale déclencherait la fin de la tétée. Les corticoïdes et la thyroxine sont aussi impliqués dans l’augmentation du métabolisme. Cette réaction peut être inhibée par un blocage sympathique ou par les agents halogénés.
II. Hypothermie per-opératoire : modifications physiologiques
L’anesthésie générale diminue le niveau de température en deçà duquel l’organisme met en jeu les mécanismes de compensation de l’hypothermie. Une hypothermie légère de 1 à 3°C en dessous de la normale est donc fréquente et résulte de plusieurs phénomènes : une réduction de l’activité métabolique (environ 15%), une augmentation de l’exposition à l’environnement, une inhibition des mécanismes de régulation, et une redistribution de la chaleur au sein de l’organisme. L’hypothermie évolue ainsi typiquement en trois phases : une redistribution interne de la chaleur, une perte vers l’environnement et une phase d’équilibre (3).
1. La première phase consiste en un refroidissement du compartiment central pendant les 30 à 45 premières minutes. Après l’induction anesthésique la taille du compartiment central augmente, la température des compartiments périphérique et cutané augmente, la température centrale diminue.
2. La seconde phase consiste en une dissipation de la chaleur vers l’environnement ; cette phase dure environ 2 à 3 heures, et la perte de chaleur est linéaire, de 0,5 à 1°C par heure. Cette perte de chaleur est progressivement limitée à mesure que la température du patient se rapproche de la température extérieure. Les pertes de chaleur se font par conduction, convection, radiation et évaporation. Les pertes par conduction dépendent de la différence de température entre l’enfant et la table d’opération. Le matériel et l’interface modifient les transferts par conductance. Les contacts avec les solutions d’irrigation ou les liquides de perfusion permettent également un transfert thermique. Ainsi l’énergie perdue pour réchauffer des liquides peut être une source importante de refroidissement. L’évaporation comprend plusieurs composantes : la sudation, les pertes insensibles transcutanées d’eau, l’évaporation de liquides appliqués au niveau cutané comme les solutions antiseptiques. De l’énergie est consommée lors du passage de la forme aqueuse à la forme gazeuse : la chaleur latente de vaporisation de la sueur à une valeur de 2260 KJ/kg. Lorsque la température extérieure est identique ou supérieure à la température cutanée, la sudation est le seul mécanisme permettant une dissipation de la chaleur. Tout ce qui limite l’évaporation peut alors entraîner une augmentation de la température centrale. Ainsi l’enveloppement peropératoire par des tissus plastiques permet un maintien de la température. Inversement un enfant humide ou au contact de draps humides va se refroidir rapidement. L’humidification de gaz secs inspirés par l’enfant est une source de perte de chaleur ; en raison d’une ventilation minute importante un tiers des pertes totales de chaleur est d’origine respiratoire chez le nouveau-né, impliquant la nécessité de réchauffer et d’humidifier les gaz inspirés, ou d’utiliser un filtre adapté si le poids le permet : cela n’est réellement efficace qu’au-delà de 3 kg. Lorsqu’il existe un courant gazeux les transferts de chaleur par convection dépendent de la différence de température entre le gaz et la peau. Les échanges de chaleur par radiation dépendent de la différence de température à la puissance 4 entre les deux surfaces opposées. A 22°C, 70% de la chaleur est perdue par radiation. Les transferts de chaleur par radiation et convection sont réduits par un simple linge recouvrant l’enfant.
3. La troisième phase est le plateau, au moment duquel la production de chaleur est égale aux pertes et la température centrale reste constante. Chez l’enfant la température centrale peut remonter secondairement par mise en route de mécanismes de production de chaleur sans frisson, bien que ceci puisse être inhibé par les agents halogénés.
III. Effets des agents anesthésiques
Les agents anesthésiques inhibent les mécanismes de régulation de la température de 2,5°C environ pour l’hypothermie et de 1,3°C environ pour l’hyperthermie. Dans ces limites le patient devient poïkilotherme, la température de l’organisme variant passivement en fonction de la production de chaleur et de l’environnement. La vasoconstriction et la thermogénèse sans frisson sont les seuls mécanismes permettant de limiter la baisse de la température centrale. Pour l’isoflurane chaque pourcentage inhalé peut entraîner une réduction de température de 3°C, chez l’enfant comme chez l’adulte. L’inhibition de la vasoconstriction est indépendante du poids et de l’âge chez l’enfant mais est plus marquée que chez l’adulte si la concentration d’agent halogéné est corrigée en fonction de l’âge. Les mécanismes centraux de la thermorégulation ne sont pas affectés par l’anesthésie loco-régionale, mais l’inhibition régionale de la vasoconstriction peut favoriser une hypothermie, en fonction de la taille du territoire concerné.
Dans certaines conditions il pourra survenir à l’inverse une hyperthermie peropératoire : pendant l’anesthésie, le seuil de réponse à l’hyperthermie est déplacé vers la droite. Les mécanismes régulateurs mis en jeu par l’hypothalamus sont déclenchés au-delà d’une augmentation de 0.3°C à l’état éveillé, alors que sous anesthésie ils le sont au-delà de 1 à 1,4°C. Les réponses physiologiques efférentes sont la vasodilatation active et la sudation. La sudation est la mécanisme le plus efficace, pouvant multiplier par cinq les pertes de chaleur. Le nouveau-né va suer si la température de son environnement dépasse 35°C et la température rectale 37°C. Le prématuré a une fonction de sudation immature. Chez l’enfant de moins de 15 kg, ce mécanisme est moins efficace que chez l’enfant plus grand et l’adulte, et d’autant plus si de l’atropine a été administrée, alors que la vasodilatation est intacte quelque soit l’âge. Un réchauffement inadéquat peut aboutir à une hyperthermie per-opératoire, rendant indispensable le monitorage de la température. En cas de mise en place de garrots le risque de survenue d’une hyperthermie est augmenté chez l’enfant, en raison de la diminution de la perte de chaleur en périphérie (4). Les problèmes liés à l’hyperthermie maligne ne seront pas abordés.
IV. Le monitorage de la température
Chez l’enfant une surveillance per-opératoire est indispensable pour détecter l’hypothermie mais aussi l’hyperthermie. Les thermomètres les plus utilisés sont des thermocouples reliés à un moniteur de surveillance ; ils existent sous forme de dispositifs à usage unique, et ont un coût modéré. La température peut être mesurée au niveau central ou périphérique.
La température axillaire est fiable si le thermomètre est placé au niveau de l’artère axillaire et le bras en adduction et peut suffire pour des interventions de courte durée. La température naso-pharyngée peut être influencée par des fuites autour de la sonde d’intubation. La température oesophagienne est fiable lorsque la sonde est placée au niveau de la partie distale de l’œsophage, cependant une influence de la température des gaz trachéaux est possible, en raison de la faible épaisseur séparant l’oesophage de la trachée ; c’est à ce niveau que le monitorage est le plus fréquemment réalisé. La température rectale est particulièrement fiable mais peut être perturbée par la présence de matières ou l’ouverture de la cavité péritonéale. La température intravésicale est très fiable si le débit urinaire est suffisant. La température tympanique donne une bonne approximation de la température de l’hypothalamus. La température cutanée n’est pas bien corrélée à la température centrale chez l’enfant anesthésié et ne peut lui être substituée, alors que c’est une des méthodes de régulation des tables radiantes chez le nouveau-né éveillé.
V. Prévention et correction de l’hypothermie
Une hypothermie légère (34 à 36°C) est fréquente et tolérable, bien que des effets sur la coagulation et la réponse immune aient été décrits chez l’enfant comme chez l’adulte.
L’hypothermie initiale liée à la redistribution peranesthésique est constante et ne peut être réduite que si les dispositifs de réchauffement cutanés sont mis en place avant l’induction afin de réduire le gradient entre le compartiment central et la peau. Les recommandations pour l’équipement des blocs opératoires prenant en charge des enfants listent ainsi de manière détaillée les matériels nécessaires pour lutter contre les hypothermies péri-opératoires, en salle d’intervention ou en salle de surveillance post-interventionnelle (5). La température de la salle d’intervention pédiatrique doit être supérieure à 24°C et même portée à 26°C pour limiter les hypothermies chez les nouveau-nés. Le confort de l’équipe chirurgicale est l’une des principales limites de ces températures élevées ; les chirurgiens pédiatres sont cependant habitués à des températures ambiantes élevées et la plupart des gestes sont de courte durée chez le jeune enfant.
Le recouvrement de l’enfant est une mesure simple de prévention passive de l’hypothermie. Il faut éviter de déshabiller les enfants lorsque c’est inutile. Il faut recouvrir immédiatement les territoires désinfectés avec des champs stériles. La couverture de la tête par un bonnet est indispensable chez le nouveau-né car sa surface représente près de 20% de la surface corporelle. L’emballage des membres permet également de réduire la surface exposée au froid. La réduction de la perte de chaleur dépend de la surface cutanée couverte, quelque soit la zone couverte ou le matériau utilisé. L’utilisation de champs chirurgicaux en matériau non tissé et imperméable empêche toute application de liquide sur la peau, source d’une perte importante de chaleur par évaporation.
Les dispositifs actifs réalisent un réchauffement cutané qui permet de prévenir ou limiter la redistribution initiale, par radiation au moyen de tables chauffantes infrarouges, par conduction au moyen de matelas chauffants à eau ou électriques et par convection au moyen de couvertures soufflantes. La température des matelas chauffant doit être contrôlée régulièrement, les modèles les plus utilisés sont les matelas électriques ; on doit interposer un matelas de gel entre le matériel chauffant et l’enfant. Un système d’enveloppement chauffant actif des membres et du tronc a été développé, délivrant la chaleur au moyen d’une circulation d’eau chaude (6). Les couvertures électriques ne doivent pas être utilisées dans le bloc opératoire car les infiltrations d’humidité peuvent être à l’origine de brûlures graves. La table radiante n’est utile qu’à la phase d’induction si l’enfant est dévêtu pour permettre des réaliser les gestes techniques nécessaires mais elle devient peu efficace après la mise en place des champs chirurgicaux. Le système actif le plus efficace et le plus utilisé est la couverture soufflante, appliquée sur une zone libre ou en positionnant l’enfant directement au dessus de la couverture. Le système ne doit jamais être utilisé directement, dirigeant le flux d’air chaud vers une surface limitée et induisant un risque de brûlures, mais toujours par l’intermédiaire d’une couverture de taille adaptée.
L’humidification des gaz inspirés prévient les lésions trachéales, et réduit la perte de chaleur respiratoire. Elle peut être active eu moyen de systèmes humidificateurs et réchauffeurs, ou passive au moyen de filtres (nez artificiels). Une humidification d’environ 50% peut être obtenue au moyen de ces filtres. Un réchauffement actif n’est nécessaire qu’en cas de ventilation en circuit ouvert. En effet le réchauffement passif est efficace chez l’enfant en raison du niveau élevé de la ventilation alvéolaire. Les risques d’un réchauffement actif (brûlures des voies aériennes, hyperhydratation) ne sont pas négligeables et les contraintes d’utilisation de ces dispositifs sont importantes (manipulations, renouvellement de l’eau, condensation dans les circuits).
Le réchauffement des solutés de perfusion est nécessaire si les volumes perfusés sont importants ou si la température du liquide est basse (sang, albumine concentrée, plasma). Pour être efficace à des débits de perfusion faibles, le système doit être adapté, notamment avec des systèmes de réchauffement coaxiaux afin que le réchauffement du liquide soit effectif jusqu’à l’entrée de la veine (7).
Conclusion
L’hypothermie est un problème habituellement rencontré chez l’enfant en phase péri-opératoire et a des causes multiples. La prévention est possible quelque soit l’âge avec des équipements adaptés. Il est conseillé d’utiliser un dispositif actif de réchauffement systématiquement chez l’enfant de moins de 1 an, lorsque l’intervention dure plus de 30 minutes de l’âge de 1 an à la période scolaire, et pour les interventions longues chez l’enfant de plus de 8 ans. Le réchauffement péri-opératoire doit être ainsi une des préoccupations principales de l’anesthésiste-réanimateur, sous contrôle du monitorage de la température.
1. Kurz A, Sessler D, Narzt E et al. Morphometric influences on intraoperative core temperature changes. Anesth Analg 1995 ; 80 : 562-567.
2. Szmuk P, Rabb M, Baumgartner J et al. Body morphology and the speed of cutaneous rewarming. Anesthesiology 2001 ; 95 : 18-21.
3. Bissonnette B. Physiologie du système nerveux central et régulation de la température, in Anesthésiologie Pédiatrique, Claude Ecoffey, Ed Flammarion, 1997.
4. Bloch E, Ginsberg B, Binner R et al. Limb tourniquets and central temperature in anesthetized children. Anesth Analg 1992 ; 74 : 486-489.
5. Recommandations pour les structures et le matériel en anesthésie pédiatrique. SFAR et ADARPEF, septembre 2000.
6. Nesher N, Wolf T, Urtzky G et al. A novel thermoregulatory system maintains peroperative normothermia in children undergoing elective surgery. Paed Anaesth 2001 ; 11 : 555-560.
7. JA Schultz, C Sims, B Bissonnette. Methods for warming intravenous fluid in small volumes. Can J Anaesthesia 1998 ; 45 : 1110-1115.
– Conséquences de l’hypothermie peropératoire ( Pr J Fusciardi, dr F Lebrun
Département d’anesthésie-réanimation chirurgicale, hôpital Jean Bernard, CHU, 86000 Poitiers)
– Dysrégulation thermique per opératoire (Dr Pascal Alfonsi. Département d’anesthésie-réanimation chirurgicale, hôpital St Joseph, Paris 14)
Résumé / Conclusion :
L’hypothermie accidentelle péri-opératoire est une complication classique de l’anesthésie qui favorise la survenue des infections, des saignements et des accidents cardiovasculaires péri-opératoires, et est responsable d’une surmortalité péri-opératoire. Bien que des moyens de prévention soient largement utilisés, elle reste très fréquente en France. Ce constat a amené un groupe d’experts à rédiger, sous l’égide de la Société Française d’Anesthésie et de Réanimation, plusieurs recommandations visant à améliorer la prévention de l’hypothermie accidentelle péri-opératoire. Les principales propositions des experts sont de maintenir une température corporelle centrale la plus proche possible de 36,5°C en utilisant les dispositifs de réchauffement de manière adaptée. Les techniques de réchauffement cutané actif sont recommandées avant et pendant l’anesthésie ainsi qu’en salle de surveillance post-interventionnelle. Il est également recommandé de réchauffer les fluides i.v., les produits sanguins labiles et les fluides chirurgicaux en complément ou en cas d’impossibilité de réchauffement cutané. Les experts suggèrent d’améliorer le dépistage de l’hypothermie péri-opératoire en généralisant le monitorage de la température centrale.
L’hypothermie peropératoire : son incidence et ses conséquences sur la transfusion sanguine et la durée d’hospitalisation
article original :
- Méthode : Etude rétrospective sur 45 866 patients opérés d’une chirurgie non cardiaque >/=60min sans pré-réchauffement. Analyse des relevés de température pris par sonde œsophagienne au cours de la chirurgie et formulation de l’hypothèse que le temps en degré-heure passé sous le seuil de 37°C est un facteur de risque de transfusion sanguine et de prolongation de la durée d’hospitalisation.
- Résultats : La température centrale moyenne au bout d’1 heure après induction était de 35,7 +/- 0,6°C. A 45 min après l’induction, 64,4% des patients avaient une température centrale < 36°C. La moitié des patients avaient une température centrale < 36°C de manière prolongée pendant au moins 1h et 20% des patients avaient une température centrale < 35,5°C de manière prolongée pendant plus d’1h. Le temps passé en situation d’hypothermie < 37°C était significativement associé à une augmentation du risque de transfusion sanguine et de durée d’hospitalisation (même si pour ce dernier critère l’association était faible et cliniquement peu importante). Une température en fin d’intervention aux alentours de 35,5°C était associée à un risque relatif de transfusion sanguine de 22%
On voit bien que le pic d’incidence d’hypothermie opératoire se situe à 1h après l’induction
- Commentaire : Comme on peut le voir sur les courbes et sur les résultats, l’hypothermie est beaucoup plus fréquente dans la première heure après l’induction. Ensuite avec le réchauffement actif et la réapparition des seuils de thermorégulation (qui sont abaissés sous AG), la température centrale remonte, même si dans cette étude, même après 6h d’anesthésie, 20% des patients avaient une température centrale < 36°C. Ces résultats sont importants à considérer pour notre pratique quotidienne : la prévention de l’hypothermie post-induction est donc particulièrement importante pour les chirurgies courtes !!! En effet pour les chirurgies longues, le réchauffement actif peut suffire pour faire remonter la température centrale. Par contre pour les chirurgies courtes, on n’a pas le temps de réchauffer les patients, qui restent donc hypothermes tout le long de l’intervention. Il faut donc les « pré-réchauffer » pour éviter l’hypothermie de « redistribution ». On voit aussi que même la perte d’1°C augmente le risque de transfusion sanguine. Il est donc primordial de réchauffer ces patients et de monitorer correctement.
source legazier.com
(pas de conflit d’intérêt avec les documents commerciaux diffusés.)
Le thermomètre frontal sans contact est-il fiable ?
Publié le 31/03/2016
Un thermomètre idéal doit refléter avec précision la température du corps, à tous les âges, être pratique, confortable à utiliser, donner un résultat rapide, ne pas être à l’origine de la transmission d’infection, ne pas être influencé par la température ambiante, enfin être sans danger et économique.
Pour les enfants de moins de 4 ans, la plupart des guidelines préconisent actuellement la prise de la température dans le creux axillaire avec un thermomètre digital. Les voies orale et rectale ne sont plus recommandées, quant au thermomètre tympanique, plusieurs paramètres semblent interférer sur ses résultats, dont la présence de cerumen.
Comparaison aves les thermomètres digital et tympanique
Reste le thermomètre frontal sans contact, qu’a testé une équipe italienne, sur 119 nouveau-nés en bonne santé, nés à terme et 70 prématurés en incubateurs. La prise de température était réalisée sur chaque participant dans les deux creux axillaires avec un thermomètre digital, dans les deux conduits auditifs avec un thermomètre tympanique et au niveau du front, avec un thermomètre frontal sans contact.
Les mesures par le thermomètre frontal font preuve d’une bonne reproductibilité dans les deux groupes de nouveau-nés. Aucune mesure aberrante n’est relevée. Les données semblent tout à fait correctes, y compris chez les nouveau-nés en incubateurs. Les auteurs précisent toutefois que les conclusions doivent être prudentes, l’étude ayant été réalisée sur des nouveau-nés en bonne santé, sans infection fébrile. S’il semblerait intéressant de préciser l’influence éventuelle de facteurs extérieurs sur la fiabilité des mesures, le thermomètre frontal sans contact apparaît toutefois ici comme une méthode simple, rapide, non invasive et sure de prise de la température, y compris chez les prématurés en incubateurs.
Dr Roseline Péluchon
RÉFÉRENCES
Sollai S. et coll. : Performance of a non-contact infrared thermometer in healthy newborns
BMJ Open 2016 ; 6 : e008695
Publié le 29/04/2016
Et si on « montait le chauffage » en salle de césarienne ?
Selon l’OMS, la température idéale en salle de naissance doit se situer entre 25° et 28°C afin de prévenir l’hypothermie néonatale qui favorise la morbidité (allant de l’hypoglycémie à la détresse respiratoire).
En cas de naissance par césarienne, la température au bloc opératoire est bien inférieure à ces recommandations, aussi une équipe américaine a cherché à savoir si l’augmentation de la température au bloc pouvait permettre de diminuer l’hypothermie néonatale. Pour cela, les chercheurs ont effectué une étude dans laquelle un groupe de patientes était césarisées dans un bloc chauffé à 20°C, tandis qu’un autre groupe bénéficiait d’une température à 23°C, le maximum autorisé au-delà duquel l’humidité augmente.
Toutes les patientes recevaient les mêmes soins : blouses et couvertures chaudes, perfusions réchauffées et couverture chauffante en cas d’anesthésie générale.
Moins d’hypothermies pour les nouveau-nés mais plus d’inconfort pour l’obstétricien !
Les nouveau-nés (NN) de plus de 32 SA étaient soigneusement essuyés, la tête couverte d’un bonnet et recouverts d’un drap chaud. Les NN de moins de 32 SA étaient séchés puis placés en sac de couchage, les matelas avec gel chauffant étant réservés aux moins de 28 SA. Les enfants étaient ensuite mis en peau à peau tant que les conditions néonatales et maternelles le permettaient, puis placés en incubateur à 38°C, la température étant prise à environs 5 min de vie et à l’arrivée dans la nurserie.
Dans le groupe interventions (406 NN dont 81 de moins de 37 SA), l’hypothermie (36,5°C) est moins fréquente que dans le groupe contrôle (419 NN dont 65 de moins de 37 SA) : 35 % vs 50 %, p < 0,001, idem pour l’hypothermie modérée à sévère (< 36°C) 5 % vs 19 % p < 0,001, néanmoins la morbidité est similaire dans les deux groupes. Paradoxalement, dans le sous-groupe des prématurés, c’est chez les grands prématurés qu’il a été retrouvé le moins d’hypothermies, sans doute parce qu’ils font l’objet de plus d’attention à cet égard ; aucun NN ayant bénéficié du matelas chauffant n’a été en hypothermie.
Du coté des obstétriciens, l’augmentation de la température a été pratiquement systématiquement ressentie et un peu plus de la moitié a trouvé cette augmentation inconfortable, 21 % ont même considéré que cela avait pu affecter leurs performances même si objectivement ce ne fut pas le cas.
Au final l’augmentation de la température en salle d’opération ne serait acceptable pour les chirurgiens qu’en cas d’effet positif prouvés sur les NN, ce qui nécessiterait des études de cohortes bien plus importantes.
Marie Gélébart
RÉFÉRENCES
Duryea EL, Nelson DB, Wyckoff MH, et coll. : The impact of ambient operating room temperature on neonatal and maternal hypothermia and associated morbidities : a randomized controlled trial. Am J Obstet Gynecol 2016 ; 214 : 505.e1-7.
Chute de température en cas de traumatisme grave, ça jette un froid !
Publié le 12/03/2018
L’hypothermie des patients victimes de graves traumatismes est un facteur prédictif indépendant de leur mortalité. Le but de cette étude de cohorte observationnelle prospective était de mesurer les variations de la température corporelle centrale des traumatisés graves (capteur épitympanique placé dans le conduit auditif sur les lieux de l’accident et pendant 3 heures) au cours de différentes phases de leur prise en charge pré-hospitalière et hospitalière.
Vingt-deux victimes ont été incluses avec un score médian de gravité des blessures (ISS) de 21 (IQR 14-29). La plupart des patients (N = 16 ; 73 %) étaient déjà hypothermiques (< 36° C) sur les lieux de l’accident lors de la première mesure. Vingt victimes (91 %) se sont encore refroidies sur les lieux de l’accident. En moyenne, la diminution de la température a été de -1,7 ° C / h. L’enveloppement des blessés à réduit la perte à -1,1° C / h. Puis, leur température est restée stable pendant les phases de transport ambulancier et de prise en charge aux Urgences.
Des mesures de prévention à instaurer immédiatement
Norvégienne et non pas tropicale, cette étude jette un froid en démontrant sans ambages que la prévalence de l’hypothermie chez les traumatisés est très élevée et que les victimes de traumatismes graves sont déjà en état de déperdition calorique sur les lieux de l’accident, avec des variations individuelles considérables. Même dans le feu de l’action, l’hypothermie doit être activement recherchée avec une mesure immédiate de la température centrale sur les lieux de la prise en charge, afin d’instaurer des mesures immédiates de prévention de la perte de chaleur par les témoins de l’accident et les secouristes, mesures qui doivent être maintenues pendant le transport ambulancier et au service des Urgences.
Dr Bernard-Alex Gaüzère
Référence
Eidstuen SC, Uleberg O, Vangberg G, Skogvoll E. : When do trauma patients lose temperature ? - a prospective observational study. Acta Anaesthesiol Scand., 2018 ; 62 : 384-393. doi : 10.1111/aas.13055.
source jim.fr
NDLR Cet article traite plus du préhospitalier, pour autant, il y a fort à parier qu’un polytraumatisé passera au bloc très rapidement. Raison de plus pour prêter attention à la température corporelle du patient. En plus de celle du bloc... (AB
Comparaison de 3 réchauffeurs de perfusion au bloc
Publié le 13/08/2018
La perfusion d’une solution saline froide ou d’érythrocytes entraîne une baisse significative de la température à cœur. Et, pour augmenter la température corporelle de 1 kg d’eau de 1 °C, il faut 1 kcal d’énergie. Ainsi, le patient doit fournir 16 kcal d’énergie pour augmenter la température de 1 litre de cristalloïdes de la température ambiante (21 °C) à la température corporelle de 37 °C.
La gestion péri-opératoire de la température est fondamentale afin de maintenir les patients en normothermie. Les réchauffeurs de fluide, dont la taille a diminué au cours des dernières années, peuvent y contribuer. Mais leur miniaturisation peut-elle influencer la performance du chauffage ? Question à laquelle une équipe – qui ne déclare aucun conflit d’intérêt même en période hivernale - s’est proposée de répondre en testant l’efficacité de trois réchauffeurs de fluide : enFlow®, Fluido compact® et Thermosens®, en mesurant la température d’entrée et de sortie du sérum physiologique tempéré et refroidi par la glace à des débits de 25, 50, 75 et 100 mL/min.
A tous les débits étudiés, les appareils de chauffage testés ont réchauffé efficacement le sérum physiologique qui était à la température de la pièce. L’enFlow® a fourni la température de sortie la plus élevée de manière significative (p < 0,05) dans tous les débits testés par rapport aux deux autres réchauffeurs. Lors de l’utilisation d’une solution saline refroidie par de la glace, l’enFlow® a maintenu une température de sortie stable > 38 °C à tous les débits testés. Le Fluido compact® n’a maintenu une température de sortie stable > 38 °C que pour des débits de 25 et 50 mL/min, alors que le Thermosens® a maintenu une température de sortie stable > 38 °C à des débits de 25, 50 et 75 ml/min.
Pas de différence à faible débit
Les trois réchauffeurs testés procurent un réchauffement adéquat à faible débit. Par contre, pour des débits plus élevés et, en particulier, avec des liquides de perfusion refroidis, seul l’enFlow® maintient des modalités de chauffage stables. Par conséquent, enFlow® s’avère supérieur lorsque la perfusion rapide de liquides de perfusion refroidis est nécessaire. En dehors de la nécessité d’une perfusion rapide, comme par exemple dans les interventions de routine, les capacités de chauffage d’enFlow®, Fluido compact® et Thermosens® s’avèrent comparables.
Dr Bernard-Alex Gaüzère
Référence
Zoremba N et coll. : Heating capabilities of small fluid warming systems. BMC Anesthesiol. 2018 Jul 28 ; 18 (1) : 98.
Source : jim.fr
Tous les moyens ne se valent pas pour maintenir la normothermie des prématurés à la naissance
Publié le 07/11/2023
L’hypothermie immédiatement après la naissance n’est pas rare chez les nouveaux-nés prématurés. Le Collège royal britannique de pédiatrie et de santé infantile de 2021 a rapporté que seulement 73,2 % des nourrissons très prématurés admis dans les unités de soins intensifs néonataux (USIN) en 2021 étaient normothermes et que 12,2 % étaient hyperthermiques.
Bien qu’une revue Cochrane ait conclu que la prévention de l’hypothermie pourrait ne pas se traduire par de meilleurs résultats cliniques, une méta-analyse en réseau a indiqué que l’utilisation d’un sac ou d’un emballage en plastique afin de limiter la déperdition thermique chez les nourrissons prématurés améliorer la survie. Le Comité international de liaison sur la réanimation néonatale a suggéré d’utiliser des interventions combinées pour prévenir l’hypothermie lors de l’admission en USIN chez les nourrissons très prématurés (recommandation faible basée sur des preuves de certitude très faibles).
74 études aux méthodologies variées
Cette revue systématique (Medline, Embase, CINAHL et CENTRAL) a voulu évaluer de manière exhaustive diverses interventions en salle d’accouchement afin de prévenir l’hypothermie immédiatement après la naissance des prématurés. Le seuil de moins de 34 semaines de gestation (SG) a été choisi pour cette revue parce qu’une revue complémentaire a déjà portée sur les nourrissons de plus de 34 SG.
Des essais contrôlés randomisés (n=29), des études observationnelles (n=16) et des études d’amélioration de la qualité (n=29) ont été pris en compte. Les principaux critères de jugement étaient la survie jusqu’à la sortie et le taux de normothermie (température axillaire, cutanée ou rectale comprise entre 36,5 °C et 37,5 °C) à l’admission dans une unité néonatale. Une méta-analyse à effets aléatoires a été réalisée et la certitude des preuves a été réalisée à l’aide des lignes directrices GRADE.
température ambiante, incubateur, couvre-chef, emballage…
Par rapport aux soins standards, une température de la salle d’accouchement supérieure ou égale à 23°C a amélioré les résultats de température du nouveau-né, sans risque d’accumulation d’hyperthermie (faible certitude), tandis qu’un chauffage radiant en mode « servo » par rapport au mode manuel a diminué la température corporelle moyenne (certitude modérée). L’utilisation d’un sac ou d’un emballage en plastique a amélioré la normothermie (faible certitude), mais avec un risque d’hyperthermie (certitude modérée).
Le capuchon en plastique a amélioré la normothermie (certitude modérée) et, lorsqu’il est associé à l’emballage en plastique, a amélioré la température corporelle moyenne (faible certitude). L’utilisation d’un bonnet en tissu a diminué l’hypothermie modérée (faible certitude). Bien que le matelas thermique ait amélioré la température corporelle moyenne, il a augmenté le risque d’hyperthermie (faible certitude). Les gaz chauffés-humidifiés pour la réanimation ont diminué le risque d’hypothermie modérée et d’hémorragie intraventriculaire grave (certitude très faible à faible). Enfin, aucune des interventions n’a amélioré la survie, mais la taille des spécimens était insuffisante.
Ainsi, une température de la salle d’accouchement supérieure ou égale à 23 °C, un incubateur radiant en mode manuel, l’utilisation d’un emballage en plastique et d’un couvre-chef sont suggérés pour les nouveaux-nés prématurés de moins de 34 SG. Les gaz chauffés-humidifiés et le matelas thermique pourraient être envisagés en plus de l’emballage en plastique, à condition que les ressources le permettent, dans les contextes où l’incidence de l’hypothermie est élevée. Afin d’éviter l’hyperthermie, une surveillance renforcée s’avère indispensable.
Les limites de cette étude comprennent les difficultés de synthèse des preuves des essais qui ont utilisé des comparaisons et des mesures de résultats variés, et dans certains cas, ont exclu les nourrissons admis en service de réanimation. L’absence de méthode standardisée de recueil de la température a également limité la méta-analyse. Enfin, le manque de données pour des interventions telles que la surveillance précoce de la température, ou les sacs chauds de liquide qui pourraient avoir un intérêt particulier dans des situations à ressources faibles, entraînant la nécessité d’études futures.
Dr Bernard-Alex Gauzère
jim.fr
RÉFÉRENCE
VV Ramaswamy, JA Dawson, MF de Almeida et al. Maintien de la normothermie immédiatement après la naissance chez les nourrissons prématurés de moins de 34 semaines de gestation : revue systématique et méta-analyse, Resuscitation, octobre 2023 ; 191 : 109934. est ce que je : 10.1016/j.resuscitation.2023.109934.
— -
Ce ne sont pas les réchauffeurs qui manquent. Sur ce site par exemple, mais il y en a d’autres.
Arnaud BASSEZ
IADE/ Administrateur