
L’anesthésie pédiatrique est une spécificité dans la spécialité.
Les enfants selon leur âge, ne présentant pas les mêmes caractéristiques que les adultes, voire les grands adolescents.
Voici quelques documents.
Il ne tient qu’à vous d’enrichir cet article en proposant des documents réalisés par vos soins ou par des équipes pédiatriques.
Le petit Armand pratique, outre le document PDF à télécharger, se présente aussi sous la forme d’un site web pratique. (à quand une application smartphone ?).
C’est une référence actuellement, pour sa simplicité, sa facilité d’apprentissage et sa grande rigueur. A fortement recommander par conséquent.
Les risques de l’anesthésie pédiatrique (SFAR)
Indispensables en Anesthésie Pédiatrique - CHU - Montpellier
La prise en charge du patient pédiatrique présentant une exacerbation aiguë de l’asthme
l’article sur la réanimation cardio-pulmonaire chez l’enfant
Pratique de l’anesthésie locorégionale en pédiatrie - CHU de Rouen
Hypnose et anesthésie en pédiatrie
La douleur de l’enfant : stratégies soignantes de prévention et de prise en charge
Hôpital d’enfants Armand Trousseau, Paris) Copyright © Len medical, Pediatrie pratique, décembre 2010
– Le score de Silverman permet de diagnostiquer et évaluer la détresse respiratoire d’un nouveau-né.
Il se compose de cinq items quotés de zéro à deux. La détresse respiratoire est importante si le score est supérieur à quatre et nécessite une intubation.
Un score à zéro ne veut pour autant pas dire que l’enfant va bien.
Moyen mnémotechnique : « BéBé(balancement/battement) Tire(tirage) En(entonnoir) Geignant(geignement) »
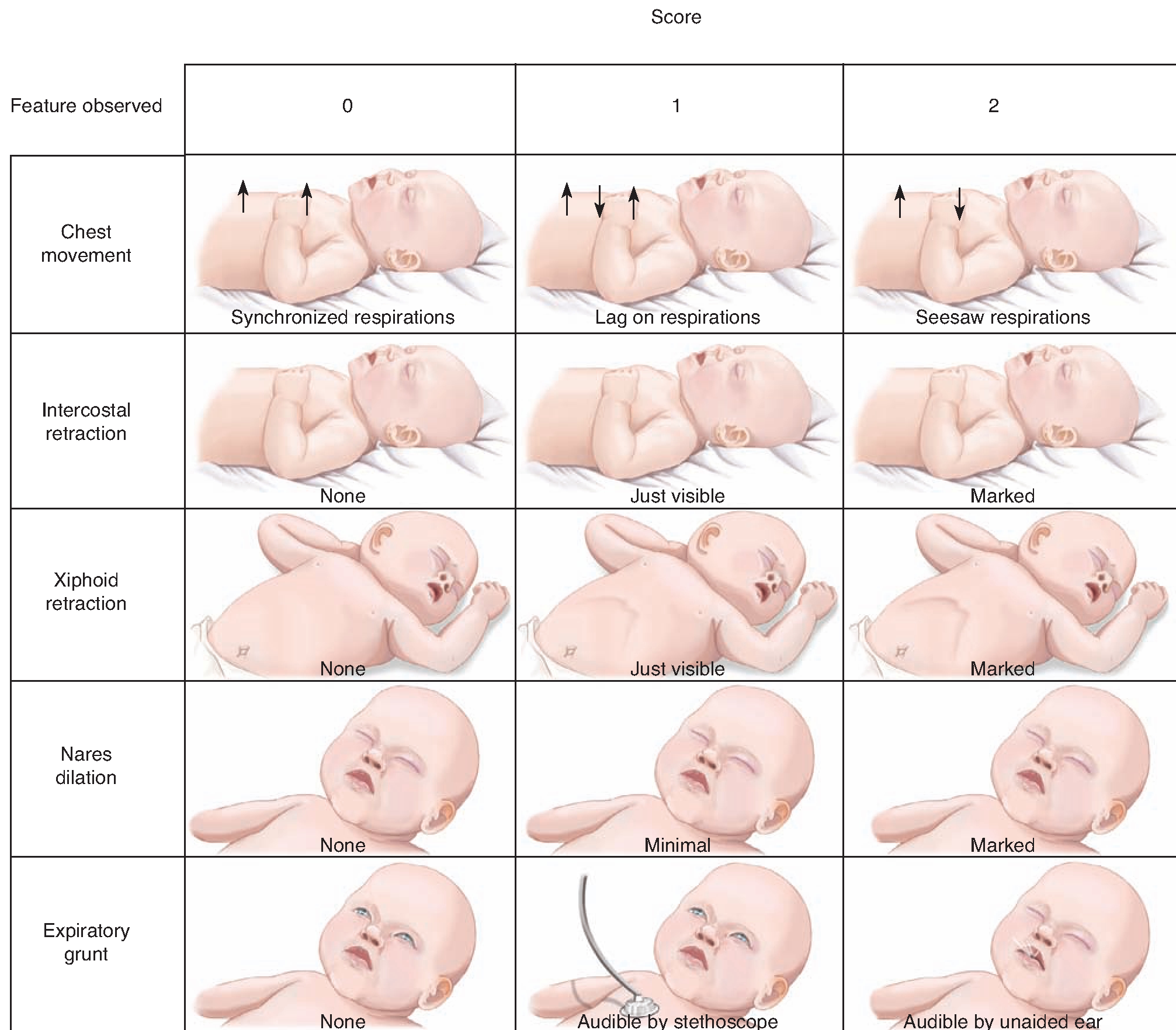
Les signes apparaissent quasiment toujours dans le même ordre : battement des ailes du nez, puis tirage, geignement expiratoire, entonnoir xiphoïdien, puis balancement. Quand on observe une balance thoraco-abdominale, c’est que le score est déjà de 9 ou 10 : l’enfant est tellement épuisé qu’il n’arrive plus à exprimer les autres signes.
– Détresses respiratoires et cardiaques du nouveau- né Cours infirmier Le 26/03/2013 Dr Audrey Dupont Service de réanimation pédiatrique CHU-Lenval 1.
Anesthésie : avec papa ou maman, ça change tout
Autoriser le père ou la mère à accompagner son enfant en salle d’opération pour assister à l’anesthésie diminue considérablement le degré d’anxiété des petits et des grands.
La pratique classique consiste à séparer le jeune patient et ses parents au moment d’entrer au bloc opératoire. S’agit-il de la manière la plus efficace de procéder ? Pas sûr du tout, si l’on en croit les résultats de ces tests réalisés par une équipe de l’hôpital de Sagunto (Valence).
Des enfants qui devaient subir une ablation des amygdales (amygdalectomie) ont été répartis en deux groupes (au hasard) : dans l’un, au moins un parent a été autorisé à rester avec son enfant jusqu’au moment de l’induction de l’anesthésie générale, alors que dans l’autre la famille a été séparée à l’entrée du quartier opératoire. A plusieurs reprises pendant cette séquence, puis au réveil de l’enfant, tous les participants (petits et grands) ont répondu à un questionnaire destiné à évaluer leur degré d’anxiété.
Le résultat est formel : la présence de la mère et/ou du père jusqu’en salle d’op réduit « considérablement » le stress tant de l’enfant que de ses parents. Et ce bénéfice est d’ailleurs souligné et apprécié par l’équipe médicale. Tous les parents qui avaient assisté à l’induction de l’anesthésie ont indiqué qu’ils souhaitaient le refaire si nécessaire, alors que 87% de ceux qui n’ont pas pu accompagner leur enfant l’ont regretté. Enfin, la qualité globale de la prise en charge a obtenu un 9/10 dans le premier groupe contre un 7/10 dans le second.
Lorsque les circonstances le permettent, poursuivent les auteurs de cette étude, autant donc organiser cet accompagnement parental.
publié le : 21-08-2014
Source : European Society of Anaesthesiology (www.esahq.org)
Anesthésie générale chez les nourrissons : c’est sans danger cognitif
Publié le 05/11/2015
La question de la toxicité de l’anesthésie générale (AG) sur le cerveau en développement a dépassé le stade de l’expérimentation sur l’animal et des études observationnelles. Trois essais contrôlés et randomisés, répondant aux acronymes PANDA, GAS et MASK, sont en cours. L’essai GAS (General Anesthesia compared to Spinal anaesthesia) s’est donné pour objectif principal d’évaluer le développement cognitif à 5 ans après une AG au cours des premiers mois de vie (1).
Sa population, recrutée dans sept pays de 2007 à 2013, est formée de 722 enfants d’âge gestationnel supérieur à 26 semaines, ayant bénéficié d’une cure de hernie inguinale avant l’âge corrigé de 60 semaines. Elle comprend 55 % d’anciens prématurés (sans lésions cérébrales sévères) et plus de 80 % de garçons. D’une façon aléatoire, une moitié des enfants (359) a été opérée sous AG au sévoflurane, et l’autre moitié (363) a été opérée sous anesthésie régionale (AR), rachidienne ou caudale, en général à la bupivacaïne, en état d’éveil. Aucun nourrisson n’avait été exposé au sévoflurane antérieurement.
Dans le groupe AG, l’administration du sévoflurane a duré moins de 60 min, en valeur médiane. Dans le groupe AR, il y a eu 20 % de violations de protocole (le plus souvent abandon de l’AR pour une AG).
En attendant l’âge de 5 ans, le niveau de développement des enfants toujours suivis a été déterminé à 2 ans ± 2 mois en utilisant les échelles de Bayley révisées (Bayley-III), complétées par l’inventaire de MacArthur-Bates pour le langage.
Pas de différence entre AG et anesthésie régionale
A 2 ans, le score composite moyen de l’échelle cognitive des enfants opérés sous AG est équivalent à celui des enfants opérés sous AR. L’intervalle de confiance 95 % [IC 95] de la différence AR – AG des scores s’inscrit dans un intervalle de plus ou moins 5 points dans l’analyse per protocole comme dans l’analyse en intention de traiter, ce qui exclut un biais dû aux violations de protocole du groupe AR.
Les fréquences des retards mentaux (scores cognitifs inférieurs à 70) sont similaires dans les deux groupes.
Pour trois des 4 autres échelles du Bayley-III, l’échelle de la motricité, l’échelle du langage et l’échelle de l’adaptativité, les deux groupes d’enfants ont aussi des scores équivalents.
Au total, ces résultats intermédiaires accréditent l’idée qu’une anesthésie générale au sévoflurane durant moins d’une heure n’est pas nocive pour le développement neurologiques des jeunes enfants, mais bien sûr ils doivent être confirmés par les tests cognitifs prévus à l’âge de 5 ans.
Tout en soulignant l’exemplarité de l’essai, les éditorialistes relèvent plusieurs choix de méthode qui empêchent de généraliser les résultats obtenus à l’âge de 2 ans : des AG avec un produit unique, des interventions d’un seul type, un outil d’évaluation global…(2).
Dr Jean-Marc Retbi
- Références
- 1. Davidson AJ et al. Neurodevelopmental outcome at 2 years of age after general anaesthesia and awake-regional anaesthesia in infancy (GAS) : an international multicentre, randomised controlled trial. Lancet 2015 ; Publicatioon avancée en ligne en ligne le 25 octobre
- 2. Warner DO, Flick RP. Anaesthesics, infants and neurodevelopment : case closed ? Lancet 2015 ; Publicatioon avancée en ligne en ligne le 25 octobre
Copyright © http://www.jim.fr
Réglette pédiatrique
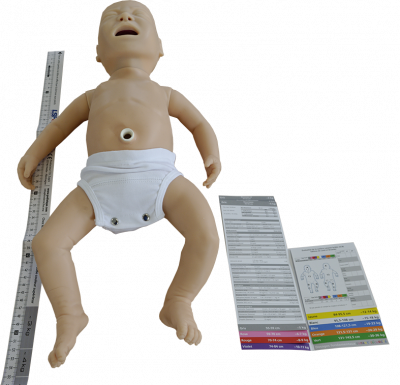
La réglette pédiatrique est un formidable outil pour vous faciliter la prise en charge des patients pédiatriques. Inspirée par la célèbre réglette de Broselow, elle a été traduite et adaptée en français par l’équipe de Life Support France.
Le dispositif se compose d’un mètre ruban indéchirable qui vous permettra d’estimer le poids de l’enfant en fonction de sa taille, ainsi q’une zone de couleur. Il suffira de vous référer à la zone de couleur correspondante dans le livret fourni pour connaître les posologies des différentes drogues de réanimation ou d’anesthésie, la taille à utiliser de sondes, etc.
Livrée dans une pochette plastique avec la notice d’utilisation, la réglette pédiatrique est disponible au prix de 30€ (Frais de port en sus en fonction de la quantité souhaitée).
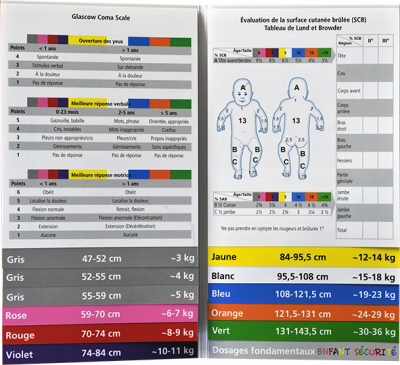
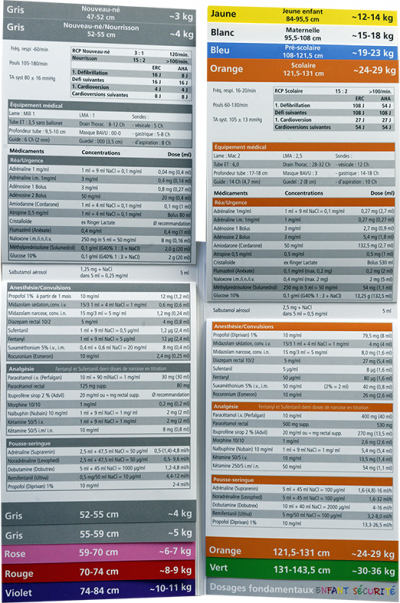
Utilisation
Placer le ruban pédiatrique le long de l’enfant à environ 20cm de distance. Placer ou maintenir l’extrémité avec la marquage "placer cette partie à la tête" à hauteur du sommet de la tête et effectuer la lecture aux pieds de l’enfant afin de sélectionner le code couleur correspondant. Pour les enfants obèses, sélectionner la prochaine zone de couleur en direction des pieds. Le couleur est basé sur les données de l’enquête américaine NHANNES (National Health and Nutrition Examination Survey) et a été adapté en 2011.
Recherchez ensuite dans le livret fourni la couleur de la page dûment caractérisée pour identifier les équipements et les dosages de médicaments appropriés en fonction de la zone de couleur Broselow.
Vous y trouverez également
- - Les valeurs normales pour la fréquence respiratoire, le pouls et la pression artérielle
- - Les recommandations pour la réanimation, en particulier le choix de l’énergie pour la défibrillation et la cardioversion
- - Les recommandations de tailles pour l’équipement médical (Lame, profondeur pour le tube ET, guide)
- - Les recommandations des médicaments ainsi que leur concentration et la dose recommandée
Douleur chez l’enfant : quelles alternatives à la codéine ?
Par David PAITRAUD (vidal.fr)- Date de publication : 03 Mars 2016
La codéine est contre-indiquée chez l’enfant de moins de 12 ans et ne peut être utilisée chez l’enfant de plus de 12 ans qu’après échec du paracétamol et/ou d’un anti-inflammatoire non stéroïdien.
Paracétamol, ibuprofène, tramadol, morphine sont autant d’alternatives parmi lesquelles le prescripteur devra choisir en fonction des autorisations de mise sur le marché, des formes galéniques disponibles, du profil de l’enfant, des caractéristiques et de l’intensité de la douleur.
Pour accompagner les professionnels de santé dans la prise en charge de la douleur aiguë et prolongée en pédiatrie, la Haute Autorité de santé (HAS) a établi des recommandation de bonne pratique où elle propose des alternatives médicamenteuses à la codéine, dans les situations cliniques problématiques les plus fréquentes.
Le diagnostic de douleur est parfois difficile chez l’enfant. Son expression peut être particulière du fait des relations avec les soignants ou les parents.
Quel est en 2016 le périmètre d’utilisation de la codéine en pédiatrie ?
La codéine entre dans la composition de spécialités antalgiques ou antitussives.
Suite à une réévaluation européenne, le périmètre d’utilisation de la codéine en pédiatrie a été restreint, comme suit :
- contre-indication chez les enfants de moins 12 ans,
- utilisation comme antalgique de seconde intention chez les enfants à partir de 12 ans, après échec du paracétamol et/ou d’un anti-inflammatoire non stéroïdien (AINS),
- contre-indication après amygdalectomie ou adénoïdectomie,
- contre-indication chez la femme qui allaite.
Concernant les médicaments contenant de la codéine utilisés en pédiatrie
Suite à la réévaluation, initiée en novembre 2012, des médicaments à base de codéine utilisés comme antalgiques chez l’enfant (CODENFAN en France), le PRAC a émis les recommandations suivantes :
- Indication restreintes aux douleurs aiguës d’intensité modérée pour les adolescents à partir de 12 ans après échec du paracétamol et/ou des AINS.
Prescription à la dose efficace la plus faible et pour la durée la plus courte possible.
Contre-indication chez l’enfant, quel que soit l’âge, après amygdalectomie ou adénoïdectomie du fait du risque additionnel que représente le syndrome d’apnée obstructive du sommeil.
En effet, un très faible nombre de cas graves, voire mortels, de dépression respiratoire ont été rapportés chez des enfants métaboliseurs rapides.
Contre-indication au cours de l’allaitement.Le passage de la codéine dans le lait représente une voie d’exposition chez le nouveau-né.
Rappel aux prescripteurs de la voie de métabolisation de la codéine (transformation hépatique en morphine par le cytochrome P450 CYP2D6) et contre-indication, quel que soit l’âge, pour les patients connus pour être des métaboliseurs rapides.
En effet, certains patients présentent un profil de métaboliseurs rapides CYP2D6, qui se traduit par une transformation plus rapide de la codéine en morphine. Chez ces patients, les taux sanguins de morphine sont plus élevés, ce qui fait courir un risque toxique et, notamment, un risque d’insuffisance respiratoire. Cette voie de métabolisation est par ailleurs immature chez l’enfant.
Le PRAC prévoit d’évaluer ultérieurement l’intérêt de l’utilisation de la codéine dans le traitement de la toux.
Les recommandations du PRAC (Comité pour l’évaluation des risques en matière de pharmacovigilance), doivent être présentées au groupe de coordination européen (CMDh) lors de sa réunion du 24 au 26 juin prochain, afin qu’une décision finale soit prise et éventuellement mise en place au niveau national.
Codéine chez les enfants dans le traitement de la toux : les restrictions d’utilisation sont applicables au niveau européen
Les restrictions suivantes concernant l’utilisation de la codéine chez l’enfant dans le traitement de la toux ont été approuvées au niveau européen.
La codéine, lorsqu’elle est utilisée comme antitussif :
- est contre-indiquée chez les enfants de moins de 12 ans ;
- n’est pas recommandée chez les enfants et les adolescents entre 12 et 18 ans présentant une fonction respiratoires altérée ;
- est contre-indiquée chez les patients connus comme étant des métaboliseurs ultrarapides des substrats du CYP2D6.
Ces nouvelles modalités d’utilisation sont applicables dans tous les Etats membres européens, et doivent être prises en compte sans attendre l’actualisation des autorisations de mise sur le marché (AMM) des spécialités concernées.
En outre, il est recommandé d’étendre la contre-indication au cours de l’allaitement à toutes les spécialités contenant de la codéine indiquées chez l’adulte, quelle que soit l’indication.
Une recommandation visant à sécuriser les flacons de solutions buvables de codéine a également été émise.
Les médicaments contenant de la codéine sont désormais contre-indiqués dans le traitement de la toux chez les enfants de moins de 12 ans.
Lors de sa dernière séance (20 au 22 avril 2015), le CMDh (Groupe de coordination des procédures de reconnaissance mutuelle et décentralisées) a approuvé à l’unanimité les recommandations proposées par le PRAC (Pharmacovigilance Risk Assessment Committee) en mars dernier, concernant les spécialités de codéine indiquées dans le traitement de la toux sèche (voir notre article du 20 mars 2015).
Désormais, les modalités d’utilisation de la codéine comme antitussif applicables dans tous les Etats membres sont les suivantes :
- contre-indication dans le traitement de la toux chez les enfants de moins de 12 ans ;
- non recommandation chez les enfants et les adolescents entre 12 et 18 ans présentant une fonction respiratoires altérée ;
- contre-indication chez les patients connus comme étant des métaboliseurs ultra-rapides des substrats du CYP2D6.
Les autorisations de mise sur le marché (AMM) des spécialités concernées devraient être modifiées prochainement (par la biais des procédures nationales) afin d’intégrer ces nouvelles dispositions.
Autres recommandations
Le CMDh recommande par ailleurs :
d’étendre la contre-indication au cours de l’allaitement à toutes les spécialités contenant de la codéine indiquées chez l’adulte, quelle que soit l’indication.
de renforcer la sécurité des flacons pour toutes les solutions orales contenant de la codéine et destinées à l’enfant, afin de minimiser le risque de surdosage accidentel.
Ces restrictions ont été décidées suite aux décès et événements indésirables graves rapportés après son administration, principalement en post-amygdalectomie.
La plupart des décès, liés à une dépression respiratoire, sont survenus chez des enfants métaboliseurs rapides ou ultra-rapides via le cytochrome P2D6, enzyme impliquée dans le métabolisme de la codéine.
Chez ces patients, le taux du principal métabolite de la codéine, la morphine, augmente de manière trop importante dans la circulation sanguine, avec un risque accru d’effets indésirables morphiniques potentiellement fatals, notamment une dépression respiratoire.
A ce titre, la codéine est contre-indiquée, quel que soit l’âge, chez tous les patients connus comme métaboliseurs ultra-rapides CYP2D6.
En 1re intention : paracétamol et ibuprofène, seuls ou associés
Selon les recommandation de bon usage de la HAS (janvier 2016), le paracétamol et l’ibuprofène constituent les traitements de première intention en pédiatrie, en fonction de l’intensité de la douleur :
- douleur faible à modérée : paracétamol ;
- douleur aiguë modérée à intense : ibuprofène.
- En cas d’efficacité insuffisante en monothérapie, ces principes actifs peuvent être associés : la HAS recommande l’association, et non l’alternance.
Focus sur l’ibuprofène : un antalgique efficace et sûr, selon la HAS
L’ibuprofène peut être utilisé chez l’enfant dès l’âge de 3 mois, dans le traitement de la douleur et de la fièvre.
Se référant au rapport de l’Organisation mondiale de la santé (OMS) de 2012, la HAS indique que l’ibuprofène est l’anti-inflammatoire non stéroïdien (AINS) le mieux étudié en pédiatrie, en termes :
- d’efficacité : sa supériorité a été démontrée par rapport au paracétamol dans la douleur aiguë, ainsi que par rapport aux antalgiques de palier 2 voire 3 en traumatologie ou en traitement des douleurs post-opératoires, "contrairement à l’idée implicite induite par la classification de l’OMS en paliers" ;
- de sécurité : le profil de sécurité est comparable à celui du paracétamol, d’après des études de cohortes portant sur plusieurs dizaines de milliers d’enfants.
La HAS précise que, "prescrit aux posologies recommandées (20 à 30 mg/kg/j) par voie orale et pour une durée courte (48 à 72 heures), les effets indésirables des AINS sont rares".
Des précautions d’utilisation toutefois nécessaires
La HAS rappelle également les situations pour lesquelles certaines précautions d’utilisation de l’ibuprofène sont nécessaires :
- en cas de varicelle : l’ibuprofène (et les AINS) ne doit pas être utilisé, "même si aucun lien de causalité n’a pu être prouvé" avec les rares cas de graves complications infectieuses cutanées et des tissus mous notifiés chez des enfants atteints de varicelle traités par AINS pour fièvre et/ou douleur (Cf. Information de sécurité de l’Afssaps du 15 juillet 2004) ;
- en cas d’infection pulmonaire ou ORL sévère, d’infection bactérienne sévère, d’infection cutanée ou des tissus mous : "malgré l’absence d’études cliniques montrant un lien entre l’utilisation des AINS et des risques majorés d’infection" ;
- en cas de risque hémorragique ou trouble de la coagulation : une évaluation de la balance bénéfice/risque doit préalablement être réalisée par le prescripteur ;
- en cas de risque de déshydratation (pouvant favoriser une insuffisance rénale) : "une déshydratation doit être prévenue ou corrigée avant l’utilisation d’AINS".
Des contre-indications spécifiées dans le résumé des caractéristiques du produit des AINS
Les AINS, dont l’ibuprofène, sont contre-indiqués dans les situations suivantes :
- insuffisance rénale, hépatique ou cardiaque sévère ;
- antécédents d’hémorragie ou de perforation digestive au cours d’un précédent traitement par AINS ;
- hémorragie gastro-intestinale, hémorragie cérébro-vasculaire ou autre hémorragie en évolution ;
- ulcération gastro-duodénale.
Tramadol et morphine : réservés aux douleurs intenses ou aux échecs des antalgiques de palier 1
Deux autres alternatives antalgiques sont citées par la HAS :
- le tramadol, antalgique de palier 2, chez l’enfant de plus de 3 ans, pour la prise en charge d’une douleur intense d’emblée ou en cas d’échec du paracétamol ou de l’ibuprofène. La HAS met en garde sur les risques d’événements indésirables graves pouvant survenir avec ce principe actif, étant donné que son métabolisme fait intervenir le CYP2D6 comme la codéine ;
- la morphine orale, antalgique de palier 3, en cas de douleurs intenses ou d’échec des autres antalgiques. Ce traitement nécessite une surveillance médicale (1 heure), en particulier après la première administration.
- La HAS souligne cependant les contraintes galéniques actuelles des spécialités de morphine orale (Cf. Tableau I) et préconise la mise à disposition de formes pharmaceutiques adaptées à l’usage pédiatrique.
Tableau I - Données pharmacologiques concernant les molécules alternatives à la codéine (extrait des Recommandations de bonne pratique de la HAS, janvier 2016)
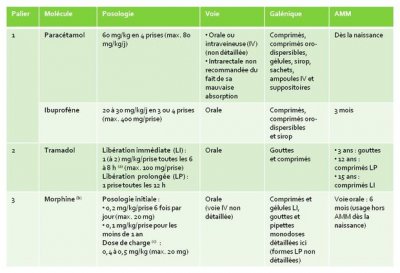
- (a) : en LI posologie prescrite et augmentée en fonction de la douleur, en principe au maximum 400 mg/j ;
- (b) : doses initiales chez un enfant naïf de morphine, l’adaptation des posologies se fait ensuite selon la douleur avec des augmentations de 50 %/24 h (et jusqu’à 100 %/24 h pour des prescripteurs expérimentés), sans dosage maximal, la posologie à atteindre étant celle qui soulage la douleur sans entraîner d’effets indésirables gênants ;
- (c) : en cas de douleur très intense et en fonction de la situation clinique.
Douleurs aiguës ou prolongées : quelle prise en charge choisir ?
Dans ses Recommandations de bonne pratique, la HAS propose 2 tableaux d’aide à la décision thérapeutique en fonction de l’intensité de la douleur et de la situation clinique de l’enfant :
- l’un concerne les douleurs aiguës (page 4 du document) : douleur post-opératoire, douleur aux urgences, infections ORL, stomatites ;
- l’autre, les douleurs prolongées et/ou chroniques, à l’exception des douleurs neuropathiques (page 5 du document) : douleur d’origine cancéreuse, douleur chronique non cancéreuse non expliquée, crises vaso-occlusives et douleurs aiguës récentes, migraines, céphalées de tension et céphalées chroniques.
Nalbuphine et oxycodone : des alternatives à étudier en pédiatrie
La HAS conclut son travail en évoquant deux autres substances antalgiques de palier 3, la nalbuphine et l’oxycodone, qui pourrait être proposées en cas d’échec, de contre-indications ou d’événements indésirables graves avec les autres molécules antalgiques : "Toutefois, leur utilisation en pédiatrie nécessite des études".
Actuellement, la nalbuphine est uniquement disponible à l’hôpital, sous forme injectable.
Selon l’autorisation de mise sur le marché de ces spécialités, la nalbuphine peut être utilisée par voie intraveineuse à partir de 18 mois en cas de douleurs intenses et/rebelles aux antalgiques de niveau plus faible. Elle est d’usage plus rare et hors AMM par voie intrarectale.
Quant à l’oxycodone (OXYCONTIN, OXYNORM, OXYNORMORO), cet antalgique ne dispose pas d’AMM en pédiatrie.
AG avant 3 ans : un danger pour le cerveau ?
Publié le 10/02/2017
Depuis plus de 15 ans, les potentiels effets délétères à long terme des anesthésiques généraux (AG) chez le jeune enfant ou chez le fœtus via la femme enceinte sont un sujet d’inquiétude et de recherche. A tel point qu’aux Etats-Unis, la Food and Drug Administration (FDA) s’est fendue sur ce sujet de 3 débats publics destinés à informer le public et les médecins et à promouvoir le dialogue et la discussion bénéfices-risques entre parents et médecins.
Du cerveau du lombric à celui du jeune enfant
Les données des expérimentations in vitro et animales montrent, du lombric au primate non humain, que tous les AG, y compris les antagonistes de N-methyl-d-aspartate (NMDA) et les agonistes de l’acide gamma-aminobutyrique, ont des effets neuro-anatomiques immédiats et à long terme (1).
Mais en clinique humaine, les preuves peinent à se montrer avec des données rassurantes sur les expositions courtes et uniques aux AG. D’autre part, les effets délétères neuro-dévelopementaux à long terme observés lors des anesthésies générales longues (> 3 heures) ou itératives chez les enfants de moins de 3 ans, sont d’appréciation difficile en raison de nombreux facteurs confondants, tels l’inflammation du cerveau du prématuré ou l’hypoxémie chronique du cerveau de l’enfant porteur d’une cardiopathie congénitale cyanogène.
Du parapluie au parasol, en attendant Marisol
En décembre 2016, sans attendre les résultats de 2 études en cours dont les résultats seront connus pour l’une en 2017 (Mayo Anesthesia Safety in Kids) (2) et pour l’autre dans plusieurs années (Recognition Memory Study), la FDA a pris médecins et chercheurs de court, en émettant un avis de tempête sur le développement cérébral de l’enfant de moins de 3 ans, en cas d’anesthésies longues (> 3 heures) ou répétées, ainsi que chez la femme enceinte lors du 3ème trimestre (3).
Cet avertissement va entraîner une modification d’indication de 11 AG agissant sur les récepteurs GABA ou NMDA, y compris les gaz anesthésiques (sévoflurane) et les AG intraveineux (propofol, kétamine, barbituriques, benzodiazépines). En ouvrant ainsi, non pas un parapluie mais un vaste parasol, cette décision sème une belle panique parmi le corps médical et les parents des 1,5 million à 2 millions de jeunes enfants anesthésiés chaque année dans le monde hyper-judiciarisé américain ! Maigre consolation, seuls les morphiniques et la dexmédétomidine ne seraient pas susceptibles d’altérer le cerveau de l’animal, mais ils ne sauraient à eux seuls suffire pour un acte de longue durée.
Entre peste et choléra, mon cerveau balance
C’est ainsi que les médecins et les gestionnaires de risques du Texas Children’s Hospital (43 000 anesthésies annuelles, 13 000 chez des moins de 3 ans, 1 300 durant plus de 3 heures, deux tiers pour des cardiopathies congénitales menaçant l’existence à court terme, 1 400 anesthésies itératives, 2 000 pour des IRM) ont dû rapidement modifier leurs pratiques (4). Désormais chez les enfants de moins de 3 ans avec des anesthésies prévues d’une durée supérieure à 3 heures, ou des anesthésies itératives, les parents sont informés des conséquences réelles ou supposées sur le cerveau de leur futur petit Donald, ainsi que de la possibilité ou non de reporter l’acte après l’âge de 3 ans.
Or, à l’exception des rares actes pouvant être pratiqués sous anesthésie locorégionale (chirurgie abdominale basse ou des membres inférieurs), les chirurgies lourdes, urgentes et indispensables requièrent les AG incriminés par la FDA. D’où la crainte que la prise de position récente de la FDA ne se traduise par des pertes de chances parmi les femmes enceintes et les enfants de moins de 3 ans, bien plus préjudiciables que les hypothétiques effets sur le développement cérébral de l’enfant.
Qu’en sera t-il chez nous ? Chats échaudés craignant encore l’eau froide, quelle sera la difficile position des autorités de santé si promptes à déployer le sacro-saint principe de précaution ? Quoi qu’il en soit, voici une raison de plus pour promouvoir le dialogue entre soignants et soignés, autour de la balance des bénéfices et des risques, et surtout d’en garder trace écrite.
Dr Bernard-Alex Gaüzère
RÉFÉRENCES
1) Sanders RD, Hassell J, Davidson AJ, Robertson NJ, Ma D. : Impact of anaesthetics and surgery on neurodevelopment : an update. Br J Anaesth 2013 ; 110 : Suppl 1 : i53-i72.
2) Pinyavat T, Warner DO, Flick RP, et coll. : Summary of the update session on clinical neurotoxicity studies. J Neurosurg Anesthesiol., 2016 ; 28 : 356-60.
3) Drug Safety Communication”(www.fda.gov/Drugs/DrugSafety/ucm532356.htm)
4) Andropoulos DB, Greene MF. : Anesthesia and Developing Brains - Implications of the FDA Warning. N Engl J Med. 2017 ; publication avancée en ligne le 8 février. doi : 10.1056/NEJMp1700196.
Copyright © http://www.jim.fr
Trop d’anesthésies générales avant l’âge de 3 ans, c’est peut-être trop !
Publié le 26/04/2019
Avant l’âge de 3 ans, l’exposition à des anesthésies générales (AG) multiples (mais non uniques), est-elle associée à des déficits de la vitesse de traitement des informations et de la motricité fine ? Pour répondre à cette interrogation, une analyse secondaire des données de l’étude Mayo Anesthesia Safety in Kids a été effectuée, au cours de laquelle des enfants non exposés à une AG, exposés à une seule AG et exposés à plusieurs AG, nés entre 1994 et 2007, ont passé des tests neuropsychologiques entre 8-12 ou 15-20 ans.
Des conséquences à long terme
Dans l’analyse factorielle, les données se sont avérées bien adaptées à un modèle à cinq facteurs. Chez les enfants exposés à de multiples AG (mais pas à une seule), un facteur reflétant les habiletés motrices, l’intégration visuelle-motrice et la vitesse de traitement des informations était significativement plus faible [différence standardisée de -0,35 (intervalle de confiance à 95 % IC 95 % -0,57 à -0,13)] comparativement aux sujets non exposés. Aucun autre facteur n’a été associé à l’exposition à de mutiples AG.
Trois groupes ont été identifiés dans l’analyse en grappes, soit 106 sujets (10,6 %) dans la grappe A (rendement le plus faible dans la plupart des tests), 557 (55,9 %) dans la grappe B et 334 (33,5 %) dans la grappe C (rendement plus élevé dans la plupart des tests). Les probabilités d’appartenir à la grappe A pour les enfants aux multiples expositions étaient de 2,83 (IC 95 % : 1,49-5,35 ; p = 0,001) comparativement à ceux appartenant au groupe B.
Des expositions multiples, mais non uniques, à des interventions nécessitant une anesthésie générale avant l’âge de 3 ans sont associées à un schéma spécifique de déficits révélés par les tests neuropsychologiques, même avec plusieurs années de recul. Toutefois, les facteurs prédictifs des déficits les plus prononcés demeurent inconnus.
Mais, comme toujours, association n’est pas causalité…
Les limites de cette étude ont fait l’objet de discussions approfondies dans des travaux antérieurs, principalement sur la possibilité que des facteurs de confusion non mesurés influent sur les résultats, tels un facteur de confusion lié aux indications chirurgicales. En effet, fondamentalement, les enfants qui ont besoin de procédures chirurgicales diffèrent de ceux qui n’en ont pas besoin. Il n’empêche !
Dr Bernard-Alex Gaüzère
RÉFÉRENCE
Zaccariello MJ, Frank RD, Lee M et coll. : Patterns of neuropsychological changes after general anaesthesia in young children : secondary analysis of the Mayo Anesthesia Safety in Kids study. Br J Anaesth., 2019 ; 122 : 671-681. doi : 10.1016/j.bja.2019.01.022.
Copyright im.fr
Anesthésie générale chez le tout-petit : des conséquences cérébrales ?
Publié le 16/11/2022
Un enfant sur sept aura besoin d’une anesthésie générale (AG) avant l’âge de 3 ans. Cet âge de trois ans correspond au seuil fixé en 2017 par la Food and Drug Administration) en dessous duquel l’AG pourrait avoir un impact sur le développement cérébral, faisant écho à plusieurs publications parues de la fin des années 1990.
La toxicité cérébrale potentielle des anesthésiques a fait l’objet de plusieurs études et reste sujette à controverse dans la communauté scientifique et à vive émotion auprès des familles de patients et du grand public. Trois études cliniques récentes, à haut niveau de preuve, ont montré qu’une exposition unique et courte à l’AG pour une chirurgie dans la petite enfance n’altère pas les mesures de l’intelligence globale (quotient intellectuel). Néanmoins, aucune de ces études n’a évalué l’effet de cette exposition sur la structure même du cerveau.
L’objectif d’une étude menée par l’Inserm et l’Université de Caen Normandie, était d’étudier si l’exposition d’un cerveau en développement à une AG pouvait entraîner des modifications comportementales et structurelles cérébrales.
– Deux sujets d’étude : la souris et le petit enfant
Une première étude a été réalisée chez la souris. Les comportements (conditionnement à la peur, labyrinthe en Y et actimétrie) et l’anatomie du cerveau (IRM à haute résolution) de souris âgées de 6 à 8 semaines, exposées ou non à plusieurs l’AG antre l’âge de 4 à 10 jours, ont été évalués. Une deuxième étude a consisté en une analyse complémentaire rétrospective à partir de la cohorte préexistante APEX (APprentissages EXécutifs et cerveau chez les enfants d’âge scolaire), chez des sujets ayant bénéficié d’une AG pour une chirurgie mineure dans l’enfance afin d’évaluer la reproductibilité des données murines chez l’homme.
Les comportements (fonctions exécutives avec la BRIEF, contrôle émotionnel, mémoire de travail, empan numérique inversé et matrices de Raven) et l’anatomie cérébrale (IRM à haute résolution) ont été comparés chez 102 enfants âgés de 9 à 10 ans exposés ou non à une seule AG pour chirurgie pendant la petite enfance (âge moyen d’exposition : 4 ans).
– Prudence
Chez l’animal, une exacerbation chronique du comportement de peur chez les souris adultes qui avaient été exposées à une AG post-natale a été mise en évidence (intervalle de confiance à 95 % [IC95 %] 4 - 80 ; p = 0,03) ; cette modification comportementale était associée à une réduction de 11 % (IC95 % 7,5 - 14,5) de la substance grise péri-aqueducale (p = 0,046).
L’étude chez l’enfant a suggéré un contrôle émotionnel plus faible (IC95 %, 0,33 - 9,10 ; p = 0,06) et une réduction de 6,1 % (IC95 % 4,3 - 7,8) du volume de la partie postérieure du gyrus frontal inférieur droit (p = 0,019) chez les enfants qui avaient été exposés à une AG pour chirurgie. Les modifications cérébrales observées chez l’enfant étaient d’autant plus marquées que l’âge d’exposition à l’AG était précoce.
Les résultats de ces études indépendantes suggèrent des effets durables de l’exposition précoce aux produits anesthésiques sur les comportements de contrôle émotionnel et les structures cérébrales.
Bien que s’agissant, chez l’enfant, d’une étude d’un faible effectif et rétrospective ne permettent pas d’établir un lien de cause à effet entre l’exposition à l’AG et les modifications cérébrales et comportementales observées, elle pointe néanmoins l’importance d’en mener rapidement d’autres et appelle les praticiens à une réflexion sur la période la plus propice pour mener une chirurgie chez le tout-petit.
Dr Bernard-Alex Gaüzère
RÉFÉRENCE
Salaün J-P, Chagnot A, Cachia A et coll. : Consequences of General Anesthesia in Infancy on Behavior and Brain Structure. Anesthesia & Analgesia : 2022 ; publication en ligne le 27 octobre- doi : 10.1213/ANE.0000000000006233
Source : jim.fr
— -
Arnaud BASSEZ
IADE
Administrateur
Formateur AFGSU
