
Actualisation 23 mars 2022
Le remplissage vasculaire est une technique consistant à perfuser une solution de remplissage via une voie veineuse pour corriger une hypovolémie
– QU’EST-CE QUE LA VOLEMIE ?
La volémie est le volume sanguin total de l’organisme (plasma et éléments figurés du sang).
La valeur normale de la volémie est de 65 à 75 ml/kg.
– QU’EST-CE QU’UNE HYPOVOLEMIE ?
L’hypovolémie absolue est définie comme une diminution du volume sanguin total circulant.
Cette diminution peut être liée à des pertes sanguines (hémorragie) ou à des pertes purement plasmatiques (pertes digestives, rénales, cutanées).
L’hypovolémie en diminuant la pression systémique moyenne est responsable d’une diminution du retour veineux systémique, de la précharge cardiaque, du volume sanguin central et du débit cardiaque, en dépit de l’augmentation de la fréquence cardiaque (régulation neurohumorale).
– L’hypovolémie relative est définie par une mauvaise répartition de la volémie entre les compartiments central et périphérique : il existe alors une insuffisance de volume sanguin central comme lors de la ventilation en pression positive ou lors d’une veinodilatation.
– Rappel physiologique
La circulation sanguine peut être considérée comme un circuit fermé avec une pompe (le coeur) et des vaisseaux constituant les artères et les veines.
Une diminution de la pression de remplissage du cœur entraîne une diminution du débit général (aspect macrocirculatoire), une baisse de la pression de perfusion des organes (aspect microcirculatoire)
Si les organes « nobles » (cœur, poumons, cerveau) sont relativement protégés par les mécanismes de régulation, les organes « périphériques » sont sacrifiés, et le déficit en oxygène hypoxie résultant du déficit d’apport en sang (hypoperfusion) peut provoquer la mort de certaines cellules et donc l’émission de toxines.
Au pire, la chute de la pression artérielle peut provoquer un désamorçage de la pompe cardiaque entraînant un état de collapsus, voire un arrêt cardio-circulatoire.
Le remplissage vasculaire permet d’augmenter la pression de remplissage du cœur et n’est utile que si cette dernière est basse. Dans le cas contraire, il peut être extrêmement nocif, entraînant une insuffisance cardiaque avec un tableau d’œdème aigu pulmonaire.
A noter que la transfusion sanguine qui permet aussi un bon remplissage vasculaire est à préférer lorsqu’il y a une perte avérée de globules rouges.
Un soluté de remplissage doit rester dans les vaisseaux, sans diffuser dans le secteur interstitiel.
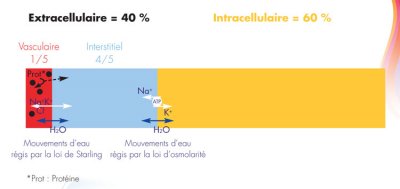
– Compartiments hydriques et échanges d’eau
L’eau totale représente 60 à 70 % du poids corporel.
L’eau est répartie dans différents secteurs : intracellulaire, interstitiel et vasculaire.
L’osmolarité intracellulaire varie peu et ce sont les variations de l’osmolarité extracellulaire qui provoquent les échanges d’eau entre ces deux secteurs.
Entre les secteurs interstitiel et vasculaire, il n’existe pas de différence de concentration des différents ions. La paroi vasculaire est une membrane semi-perméable retenant, au moins en partie, les protéines dans le secteur plasmatique.
La concentration de protéines est beaucoup plus élevée dans le secteur plasmatique que dans le secteur interstitiel. Starling a défini les facteurs conditionnant les échanges liquidiens entre les secteurs vasculaire et interstitiel.
– Les cristalloïdes :
Les cristalloïdes contiennent de l’eau et des ions.
- les solutions de chlorure de sodium NaCl 0,9 %
- les solutions de Ringer et Ringer-lactate.
Les solutions cristalloïdes se caractérisent par une expansion volémique faible (0,2 à 0,3 litre par litre perfusé).
Ces solutions s’équilibrent rapidement entre le secteur intravasculaire et interstitiel. On estime ainsi que seulement 1/3 à 1/4 du volume perfusé reste dans le secteur intravasculaire.
Ces solutions diffusent dans l’ensemble du secteur extracellulaire. C’est-à-dire qu’ils ne restent pas dans les vaisseaux sanguins et se diffusent rapidement dans les tissus. L’action est de courte durée.
– Les colloïdes :
Les colloïdes exercent une pression oncotique contribuant à retenir l’eau dans le secteur intravasculaire, c’est-à-dire les vaisseaux. La pression oncotique est définie par le nombre de molécules oncotiquement actives. L’efficacité dépend du pouvoir oncotique.
la pression oncotique
On peut classer les colloïdes en deux grandes familles :
- Colloïdes naturels
- Colloïdes de synthèse
Les colloïdes naturels (albumine) ont des indications bien, définies depuis la dernière conférence de consensus de 1996 (Hypoalbuminemie vraie, ponction d’ascite, contre indication aux colloïdes de synthèse...).
Dans les colloïdes de synthèse, on classe les gélatines et les amidons.
- Qu’est ce qu’une Gélatine ?
Les gélatines commercialisées sont des gélatines fluides modifiées (GFM). Elles sont obtenues par dégradation du collagène d’os bovidés par une technique mise au point en 1952. Cette dégradation aboutit à la formation de peptides de gélatines de faibles masses moléculaires qui sont modifiés chimiquement et s’associent pour former des molécules dont la masse moléculaire moyenne est voisine de 35 000 Da.
Les molécules sont de tailles variables et la solution est dite polydispersée (à 3 ou 4 %) dans une solution ionique.
L’osmolarité et la viscosité des GFM est proche de celle du plasma.
La distribution et l’élimination de la GFM administrée par perfusion intraveineuse dépend de nombreux facteurs : la taille des particules, le poids moléculaire, la charge électrique, le volume administré, la vitesse d’administration, etc.
Les GFM permettent d’augmenter la volémie d’un volume inférieur à celui du volume perfusé (80%). Chez le sujet normal, la durée de cette expansion volémique initiale est de 2 à 3 heures.
- Qu’est ce qu’un Hydroxyéthylamidon (HEA) ?
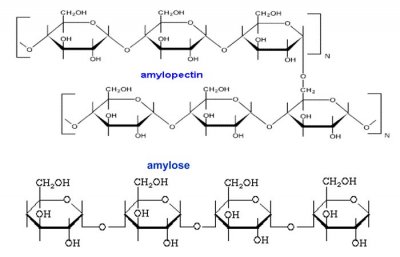
Les HEA sont des polymères naturels de glucose, dérivés de l’amylopectine.
Amylopectine : polymère de glucose ramifié par des liaisons
(Alpha 1-6) et (Alpha 1-4)
Propriétés physicochimiques des HEA :
Les HEA sont des solutions polydispersées.
Ils se distinguent par 4 paramètres physicochimiques :
- le poids moléculaire in vitro : PM in vitro (Kda)
- la concentration d’HEA en solution (%)
- le taux de substitution molaire (TSM) : reflète le pourcentage d’hydroxyéthylation sur la molécule, soit le rapport entre le nombre de groupements hydroxyéthyl sur le nombre total de molécules de glucose
- le rapport C2/C6 : paramètre quantifiant la position du groupement hydroxyéthyl sur la molécule de glucose, soit sur le carbone 2, soit sur le carbone 6.
Le TSM permet de classifier les différents HEA :
- Les "Hetastarch" (TSM : 0,7) ne sont pas commercialisés en France
- Les "Hexastarch" (TSM : 0,6, HEA 200/0,6) ne sont plus commercialisés.
- Les "Pentastarch" (TSM : 0,5) sont des HEA d’ancienne génération représentés par les HEA 200/0,5.
- Les "Tetrastarch" (TSM : 0,4) sont des HEA de plus récente génération comme les HEA 130/0,4.
L’importance de l’expansion volémique d’une solution colloïdale dépend de la pression oncotique qu’elle développe dans le secteur vasculaire.
L’expansion volémique immédiate est au moins égale au volume perfusé, avec un HEA concentré à 6%, chez le sujet normal.
Les Presses Universitaires François Rabelais et le CNEAR vous propose le manuel "Hémodynamique appliquée" 2020 gratuitement en téléchargement PDF.
– Remplissage vasculaire au cours des hypovolémies relatives ou absolues (RPC 1997)
— -
— -
- Et la suite
— -
A lire en complément
Monitorage de la volémie] (un peu ancien)
Le maintien de la volémie ou masse sanguine totale est indispensable à l’oxygénation tissulaire. Toute hypovolémie, qu’elle soit absolue par diminution de la masse sanguine, ou relative par diminution du retour veineux au cœur, expose au risque d’effondrement du débit cardiaque, de la pression artérielle et surtout du transport et de la délivrance tissulaire en oxygène, à l’origine d’un syndrome de défaillance multiviscérale. Le remplissage vasculaire a donc pour objectifs la restauration d’une volémie efficace ainsi que le maintien d’une pression de perfusion et d’un apport d’oxygène adéquats.Différents solutés de remplissage sont à notre disposition. Ils se répartissent en deux grandes catégories, les cristalloïdes et les colloïdes. Le choix d’un produit de remplissage doit prendre en compte les propriétés physico-chimiques, pharmacocinétiques et pharmacodynamiques du soluté, ses effets secondaires, ainsi que le contexte et l’indication du remplissage vasculaire.
— -
— -
Exploration hémodynamique et angiographie cardiaque
Cathétérisme et angiocardiographie :
Le cathétérisme cardiaque consiste dans le passage d’une sonde (tige, creuse ou pleine), dans les cavités cardiaques et les vaisseaux proches, dans un but diagnostique ou thérapeutique.
L’angiocardiographie enregistre sur un dispositif adéquat les images obtenues au cours de l’injection, à travers une sonde, d’un produit de contraste, opaque aux rayons X, dans un endroit choisi du système circulatoire, afin d’établir un diagnostic.
Ces deux techniques, introduites dans la médecine il y a près de 50 ans, ont été à l’origine du développement de la cardiologie.
Elles permettent :
– la mesure des pressions et des débits ;
– la quantification des résistances du système vasculaire, des insuffisances et des rétrécissements valvulaires ;
– l’étude morphologique et fonctionnelle des cavités cardiaques, particulièrement du ventricule gauche, de l’aorte et des artères pulmonaires ;
– la détection des communications et courts-circuits anormaux ;
– la quantification de ces shunts ;
– l’étude de la fonction cardiaque, systolique et diastolique ;
– l’étude du métabolisme myocardique ;
– le prélèvement de biopsies myocardiques, pour examen histologique ;
– le traitement de certaines cardiopathies.
Entre 1945 et 1975, ces deux procédés ont occupé une place privilégiée dans la cardiologie ; ils ont été la pierre de touche des autres techniques et permis le progrès de la chirurgie et l’approfondissement de nos connaissances.
Depuis, le développement extraordinaire des capacités diagnostiques de l’échocardiographie et d’autres moyens non invasifs, l’explosion de l’informatique , la disparition quasi totale des cardiopathies congénitales et rhumatismales des services de cardiologie d’adultes, le changement des modes de vie et des conditions sociales, le vieillissement de la population, et l’augmentation, probablement réelle, des maladies par athérosclérose et des possibilités de traitement interventionnel (c’est-à-dire énergique, par action mécanique sur une partie du corps en vue de la modifier) par voie percutanée transluminale, des lésions des artères coronaires, ont abouti à ce que ce soit surtout des patients souffrant d’une insuffisance coronaire qui occupent actuellement les services de cardiologie.
Le nombre de cathétérismes effectués pour évaluer l’importance d’une valvulopathie, le stade évolutif d’une cardiomyopathie, la réponse à un traitement ou autre est aujourd’hui restreint.
Il est habituel de nommer cathétérisme, ou cathétérisme droit, l’exploration des cavités droites du coeur, oreillette et ventricule droits, AP et ses branches et de faire référence à l’exploration du coeur gauche sous les dénominations de cathétérisme gauche ; le terme angiographie sous-entendant l’opacification sélective d’une cavité déterminée, oreillette ou ventricule droits, AP, oreillette ou ventricule gauches ou aorte sus-sigmoïdienne.
A - Indications et contre-indications de l’exploration hémodynamique et angiographique :
Le besoin d’effectuer une exploration hémodynamique et angiocardiographique pour établir le diagnostic ou évaluer l’importance d’une cardiopathie est devenu aujourd’hui un fait rare.
Dans la plupart des cas, les méthodes non invasives ont largement remplacé ces deux techniques sanglantes.
Il en reste toutefois, à notre avis, un certain nombre d’indications :
– les cardiopathies valvulaires dont l’estimation est difficile, sténoses ou insuffisances mitrales, aortiques, tricuspides ou pulmonaires, ainsi que les cardiopathies valvulaires complexes, mitroaortiques et mitrotricuspidiennes.
La plupart des cardiopathies congénitales entrent dans ce cadre ;
– les myocardiopathies primitives ou secondaires, très souvent moins dans un but diagnostique que pour faire une évaluation et choisir un traitement ;
– les rétrécissements mitraux, afin d’effectuer une valvuloplastie mitrale percutanée.
Le cathétérisme cardiaque est par ailleurs nécessaire :
– pour la surveillance des paramètres hémodynamiques dans les unités de soins intensifs ; pour l’évaluation des effets thérapeutiques d’une drogue ou d’une intervention ;
– pour obtenir des biopsies endomyocardiques afin de faire un diagnostic étiologique ou dans le cadre du dépistage d’un rejet d’une greffe cardiaque ;
– pour le diagnostic des embolies pulmonaires.
L’attitude est diverse en ce qui concerne la convenance ou non de faire un cathétérisme droit chez les patients valvulaires, dont le vice est connu, qui doivent être opérés, et qui sont envoyés pour une artériographie coronaire.
B - Contre-indications :
Elles sont devenues exceptionnelles.
La seule contre-indication absolue serait le refus d’un patient pleinement responsable, ou des personnes le représentant devant la loi.
Il existe, en revanche, de nombreuses contreindications relatives.
Si l’exploration n’est pas une urgence, toutes les conditions qui augmentent les risques et qui peuvent être corrigées (fièvre, anémie, intoxication digitalique, insuffisance rénale sévère, taux de prothrombine inférieur à 30 %, troubles du rythme...) sont des contreindications relatives.
L’âge physiologique avancé et les tares viscérales accroissent les risques.
L’existence d’extrasystoles ventriculaires ou de lambeaux de tachycardie augmente les probabilités de déclenchement d’une crise de tachycardie ou de fibrillation ventriculaire comme conséquence des excitations mécaniques dues à la sonde.
C - Incidents et accidents :
Le cathétérisme et l’angiocardiographie s’accompagnent, dans certains cas, d’incidents et d’accidents.
Les risques dépendent de la voie d’abord choisie, de la nature de l’exploration, de l’état clinique du patient, du type des lésions et de certains facteurs tels qu’un âge supérieur à 70 ans, une fraction d’éjection inférieure à 30 %, une insuffisance rénale ou respiratoire, un diabète, une hypertension artérielle pulmonaire (HTAP), une sténose du tronc commun de la coronaire gauche et autres.
La mort au cours des explorations hémodynamique et angiographique est devenue exceptionnelle.
Elle est habituellement la conséquence :
– d’un choc cardiogénique consécutif à un infarctus du myocarde, un malaise vagal ou à l’angiographie sélective ventriculaire gauche, chez des patients en situation critique ;
– d’un trouble du rythme grave, tachycardie ou fibrillation ventriculaire ou arrêt cardiaque irréversible ;
– d’une myocardiographie avec ou sans tamponnade.
La perforation du coeur ou des vaisseaux est extrêmement rare, en dehors des tentatives de cathétérisme transseptal et des valvuloplasties percutanées.
Les troubles du rythme sont fréquents : extrasystoles auriculaires ou ventriculaires, bradycardies vagales.
Les malaises vagaux s’annoncent en général par des bâillements répétés, des sueurs ; le patient devient pâle et se sent angoissé.
La bradycardie et l’hypotension suivent.
Il faut, dès les premiers symptômes, injecter de l’atropine de 0,5 à 1 mg en intraveineux (IV) et mettre en place une perfusion de soluté à grosses molécules.
Les complications cérébrovasculaires dues à des embolies sont aujourd’hui, avec l’emploi systématique des anticoagulants, très rares.
Les rétrécissements aortiques calcifiés peuvent être à l’origine d’embolies calcaires.
La migration de cristaux de cholestérol, à partir des plaques d’athérosclérose ulcérées, serait relativement fréquente au cours du passage des sondes dans les artères, et des angiographies et angioplasties, surtout chez les sujet âgés.
Cependant, les manifestations cliniques de ces embolies, qui peuvent toucher tous les organes situés en aval, passent souvent inaperçues.
Il existe habituellement un délai entre le moment de leur survenue et celui de leur découverte.
Les atteintes rénales peuvent être la cause d’une insuffisance terminale de ce système.
Les crises d’étouffement, la dyspnée ou l’oedème aigu du poumon apparaissent quelquefois au décours d’un cathétérisme, du fait du volume des liquides perfusés, de l’angiocardiographie, de l’effort, des troubles du rythme ou de l’insuffisance coronaire.
Les complications locales sont fonction de la technique employée et de la voie choisie.
L’abord percutané de la veine et de l’artère fémorales peut être à l’origine d’une fistule artérioveineuse, d’un hématome, d’un faux anévrisme artériel, ou d’une phlébothrombose veineuse.
Les ponctions des veines sous-clavière et jugulaire interne peuvent se compliquer d’un pneumothorax.
Voies d’abord :
Les cathétérismes droit et gauche peuvent être effectués par dénudation d’une veine ou artère du bras (veines médiane, basilique ou humérale, artère humérale, plus rarement veine saphène) ; ou par voie percutanée, selon la technique de Seldinger.
Les cathétérismes gauches sont généralement effectués par voie percutanée artérielle rétrograde et, d’une façon exceptionnelle, par voie transseptale.
Chacune de ces techniques a des avantages, des inconvénients et des indications précises.
La voie percutanée préserve le capital vasculaire et permet la répétition des examens.
L’abord par dénudation limite les possibilités de répétition de l’examen.
Le cathétérisme de l’AP dans les cas de dilatation de l’oreillette droite et d’insuffisance tricuspide importante, le cathétérisme du sinus coronaire, sont plus faciles à partir des veines du bras gauche.
L’approche brachiale, veineuse et artérielle est nécessaire en cas d’artérite des membres inférieurs, de lésions athéroscléreuses ou de tortuosités des vaisseaux, de thrombose des veines abdominales, dans certains cas de coarctation aortique, en cas d’échec du cathétérisme artériel rétrograde à partir de la fémorale.
Voie percutanée :
Le cathétérisme percutané est effectué par la méthode de Seldinger, ensemble de manoeuvres qui permettent d’introduire un cathéter dans la lumière d’un vaisseau en se servant d’un guide métallique très fin préalablement passé dans ce vaisseau à travers une aiguille, sous anesthésie locale.
Le vaisseau est piqué avec une aiguille, montée sur une seringue dans le cas des veines, prise entre les doigts dans le cas des artères.
Les sensations tactiles et l’aspiration dans le cas des veines, et le recul du piston ou l’écoulement du sang en jet dans le cas des artères témoignent de la position intraluminale de l’aiguille.
Un guide est alors introduit à travers l’aiguille dans la lumière du vaisseau.
Puis l’aiguille est retirée, et, grâce au guide, un Desilet veineux ou artériel à valves, ou des sondes à orifice distal, sont poussés à travers la peau dans le système circulatoire.
Le Desilet est un cathéter ou tube court, d’à peu près 10 cm de longueur, à parois minces, qui est placé dans les vaisseaux au niveau de la ponction de la peau et à travers lequel sont introduites les sondes.
L’emploi du Desilet à valves diminue les traumatismes artériels et rend indolore le changement des sondes.
Ces changements doivent être effectués, dans le cas des cathéters préformés à orifice distal, à l’aide du guide ; l’ensemble guide-sonde est poussé ou retiré du vaisseau.
Une fois l’examen terminé, les sondes et Desilet sont enlevés et les tissus sont comprimés au niveau des ponctions vasculaires, de façon à empêcher le saignement et à faciliter l’hémostase.
Les pouls distaux doivent être contrôlés.
Après 5 à 10 minutes, si tout semble correct, un pansement compressif est posé, constitué par un rouleau de quelques compresses et une bande d’Élastoplaste.
A - Sondes :
Les sondes sont des tubes, d’un diamètre de 1,6 à 2,9 mm et d’une longueur de 80 à 125 cm, qui permettent d’enregistrer les pressions, d’effectuer des prélèvements et d’injecter des substances diverses dans les cavités ou les vaisseaux du coeur.
Les sondes doivent être radio-opaques, lisses, peu traumatiques et peu thrombogènes, relativement flexibles pour franchir les tortuosités et les orifices valvulaires, et en même temps assez rigides pour ne pas se plier ni se casser et pour obéir facilement aux manœuvres de torsion.
Les cathéters destinés à l’injection d’un volume important de produit de contraste en un temps très court doivent résister aux pressions nécessaires sans éclater (jusqu’à 1 000 pounds per square inch [PSI] soit 70 kg/cm²) et rester en place, relativement immobiles, pendant l’injection.
Cela n’est possible qu’avec des sondes munies de trous latéraux à leur extrémité distale.
Le cathétérisme rapide des cavités cardiaques et des vaisseaux est aujourd’hui possible grâce aux sondes préformées.
Ces sondes doivent avoir une bonne mémoire plastique.
Le nombre de sondes préformées, dont le but est d’atteindre un point déterminé du circuit sanguin, et de cathéters destinés à accomplir une tâche bien précise s’est accru considérablement ces dernières années.
L’usage de ces sondes très spécifiques, qui offrent des possibilités autres assez limitées, oblige à l’emploi de plusieurs cathéters au cours d’une même exploration.
Les cathéters ont des calibres exprimés par des chiffres, 5 F, 6 F, 7 F, 8 F, 9 F, qui indiquent leur circonférence.
Le diamètre externe de la sonde est égal à ce chiffre divisé par ð. Le diamètre externe d’une sonde 8 F est de 2,5 mm.
La majorité des cathéters qui sont fournis aujourd’hui par les fabricants est stérilisée au gaz d’éthylène comme des produits à usage unique.
B - Choix de la sonde :
Le choix de la sonde dépend du but poursuivi.
Dans les services d’adultes, le cathétérisme des cavités droites du coeur est généralement effectué avec une sonde de Swan-Ganz.
Ces sondes ont été conçues pour être montées jusque dans l’AP à partir d’une veine, même sans radioscopie, au lit du malade.
Elles sont très souples et disposent généralement de trois conduits ou lumières : l’un est en communication avec le ballonnet situé autour de l’extrémité distale ; ce ballonnet peut être gonflé à partir d’un embout externe avec une seringue remplie de 1,5 mLd’air ou d’un gaz neutre ; le gonflage du ballon facilite la progression de la sonde entraînée par le courant sanguin ; les deux autres voies permettent l’injection ou l’aspiration de liquides ou l’enregistrement des pressions ; l’une aboutit à l’extrémité distale du cathéter et l’autre se termine à près de 20 cm de cette extrémité.
Les pressions artérielle et « capillaire » pulmonaires peuvent être obtenues en dégonflant (pression artérielle) ou gonflant (pression « capillaire ») bien le ballon une fois la sonde dans l’AP.
Les sondes de Swan-Ganz comportent encore une sortie supplémentaire qui permet de brancher la thermistance située au bout du cathéter sur un appareil adéquat pour mesurer le débit cardiaque par thermodilution.
Le cathétérisme gauche est généralement effectué avec une sonde dite « queue de cochon ».
Pour l’enregistrement des pressions ventriculaires gauches dans les myocardiopathies primitives hypertrophiques obstructives et dans les rétrécissements aortiques, la sonde idéale est celle de Schoonmaker ou « multipropos » à trou uniquement distal.
Les sondes de stimulation s’avèrent parfois nécessaires, en cas de bloc auriculoventriculaire, complet ou avancé, chronique ou paroxystique, ou si l’on craint sa survenue.
Il faut les connaître et savoir s’en servir.
C - Déroulement de l’examen :
Conduite du cathétérisme et manipulation des sondes :
Une fois la peau badigeonnée avec de l’alcool iodé et les champs disposés sur le malade, l’anesthésie locale est effectuée à l’endroit des ponctions veineuse et artérielle.
Les perfusions pour les sondes sont alors installées ; les têtes manométriques et les raccords, purgés ; les seringues pour les prélèvements, rincées à l’héparine ; les Desilets, veineux et artériel, préparés ; les sondes, droite et gauche, rincées abondamment et disposées sur un plateau de 20 × 30 cm contenant un peu de sérum.
Le guide métallique que l’on utilise et le raccord court qui sert pour l’angiocardiographie sont aussi placés dans ce plateau, entre les pieds du malade.
Le cathétérisme droit est effectué d’abord.
Les prélèvements de sang et l’enregistrement des pressions sont effectués au fur et à mesure du déroulement de l’exploration, dès l’entrée de la sonde dans la cavité :
– pressions auriculaire et ventriculaire droites ;
– enregistrement de la pression au cours du retrait de la sonde du ventricule à l’oreillette droite ;
– enregistrement des pressions artérielle et « capillaire » pulmonaire.
Dans le cas des cardiopathies valvulaires, ischémiques ou diverses, sans « court-circuit », des échantillons de sang sont prélevés dans les veines caves inférieure et supérieure, l’oreillette droite moyenne et l’AP.
Si une communication est suspectée, la série de prélèvements est plus complète : veine cave supérieure, haute et basse ; veine cave inférieure, haute et basse ; oreillette droite, haute, moyenne et basse ; ventricule droit, tricuspide, pointe et infundibulum ; tronc de l’AP et ses branches, droite et gauche ; oreillette gauche et veines pulmonaires, si possible.
Le cathétérisme gauche est effectué après avoir obtenu une pression « capillaire » pulmonaire.
Les sondes « gauches » sont généralement introduites avec un guide métallique en J, à leur intérieur.
Ces sondes doivent être manipulées doucement.
La progression du cathéter ne doit pas être douloureuse. Une fois dans l’aorte sus-sigmoïdienne, le guide est retiré.
La sonde est aspirée et rincée, la pression aortique est enregistrée, si nécessaire en même temps que la pression humérale ou fémorale.
Puis, s’il s’agit d’une « queue de cochon », la sonde est poussée dans le ventricule gauche.
Il suffit souvent pour cela de tourner la boucle distale de façon à la placer dans le plan frontal et de pousser la sonde doucement.
Les angiocardiographies sont généralement effectuées en fin d’examen.
Elles doivent être réalisées dans les conditions les meilleures pour analyser le problème posé par le malade.
Le lieu de l’injection, l’incidence des rayons X et la quantité de produit doivent être adéquats.
D - Renseignements fournis par le cathétérisme :
Les renseignements fournis par le cathétérisme découlent de l’analyse :
– du trajet des sondes ;
– des pressions existant dans les cavités cardiaques et dans les vaisseaux ;
– des oxymétries effectuées sur les échantillons de sang prélevés à différents niveaux ;
– des courbes de dilution ;
– des valeurs du débit cardiaque, des résistances vasculaires et des surfaces valvulaires ;
– des données tirées des angiocardiographies ;
– de l’étude de la fonction cardiaque et des réponses aux épreuves d’effort, de remplissage et de provocation ou pharmacologiques.
E - Trajet des sondes :
Le trajet des sondes peut être normal ou inhabituel.
Dans certains cas, la veine cave inférieure débouche par l’azygos dans la veine cave supérieure.
La sonde, poussée depuis la veine fémorale, passe d’abord derrière l’oreillette droite et redescend ensuite pour pénétrer dans le coeur.
La persistance d’une veine cave supérieure gauche communiquant avec le sinus coronaire peut être une anomalie isolée ou s’associer à un retour veineux pulmonaire anormal.
Les incidences transverses et l’injection à la main d’un peu de produit radioopaque permettent de vérifier la position du cathéter et la nature du vaisseau.
Le franchissement d’une communication interauriculaire, ou d’un foramen ovale perméable, est facile à reconnaître par le prélèvement de sang à l’endroit que l’on suppose être l’oreillette gauche (celui-ci est bien oxygéné) et par le cathétérisme des veines pulmonaires ou du ventricule gauche.
Le passage de la sonde du ventricule droit (à travers une communication interventriculaire) dans l’aorte ascendante, ou de l’AP (à travers un canal artériel persistant) dans l’aorte descendante, ou vice versa, est aisément identifié grâce à l’oxymétrie, à l’enregistrement des pressions et à la progression du cathéter dans les champs pulmonaires, dans les vaisseaux du cou, ou dans l’aorte abdominale.
L’aorte peut descendre à droite de la colonne vertébrale.
Le cheminement, dans un situs solitus, du cathéter artériel rétrograde, depuis l’aorte thoracique descendant à gauche dans une aorte ascendante située aussi sur le bord gauche de l’ombre cardiaque, est hautement suggestif d’une transposition corrigée des gros vaisseaux par inversion bulboventriculaire.
F - Pressions :
1- Définition :
Les pressions cardiovasculaires sont surtout le résultat de la contraction cardiaque et varient tout le long du cycle cardiaque.
Les pressions cardiovasculaires peuvent être considérées comme des fluctuations périodiques de force par unité de surface.
Leur mesure est effectuée au moyen de microcapteurs, très fidèles, placés à l’extrémité distale des sondes, ou par transmission à travers la colonne de liquide contenue dans le cathéter et les raccords, grâce à des capteurs externes.
Ces capteurs, transducteurs ou têtes manométriques transforment l’énergie mécanique en énergie électrique.
Les systèmes de mesure utilisés habituellement s’appuient sur le principe du pont de Wheatstone.
Les pressions exercées sur une membrane induisent des différences de potentiel qui, convenablement amplifiées et transformées, peuvent être enregistrées.
Dans les services d’hémodynamique et en cardiologie, malgré les recommandations des sociétés savantes, les pressions continuent, encore aujourd’hui, à être exprimées en millimètres de hauteur d’une colonne de mercure (mmHg).
Il faut mesurer ces pressions comme une force par unité de surface, en newtons (N) par mètre carré, pascals ou kilo-pascals, 1 Pa = 1 N/m².
Il faudrait multiplier les mmHg par 133,3 pour obtenir des pascals.
La pression est donc exprimée comme une « hauteur », hauteur piézométrique.
Mais, dans un système de vaisseaux et pour des liquides parfaits et circulants, l’énergie mécanique du fluide par unité de poids ou « charge totale » est la somme de la « hauteur piézométrique » (hp = P/pg), de la « hauteur de position » (z), et de la « hauteur dynamique » (hd = V²/2g, liée à l’énergie cinétique ; V, vitesse ; hd est la hauteur à laquelle s’élèverait le liquide, comme conséquence de l’énergie dynamique : pV²/2 = pgh => h = V²/2g).
Si le système est fermé, la somme de ces trois variables reste constante (théorème de Bernouilli).
Au cours du cathétérisme cardiaque, les pressions sont mesurées chez des sujets couchés.
Les capteurs de pression sont disposés au niveau d’un plan horizontal passant par l’oreillette droite du patient.
Ainsi, z est nul.
L’énergie cinétique n’est pas mesurée. Seule est estimée la « hauteur piézométrique ».
Dans un système vasculaire, l’écoulement ou débitQ, dans deux points proches, a et b, est constant et égal au produit de la surface de section S par la vitesse V du flux.
Q= VaSa = VbSb.
S’il existe une portion de calibre réduit, la vitesse augmente.
L’énergie totale restant la même pour des vitesses d’écoulement suffisamment élevées, la pression latérale peut s’abaisser au point qu’une aspiration se produit, c’est l’effet « Venturi ».
En traversant un orifice de surface s, le liquide transforme son énergie potentielle ou de gravitation pghi en énergie cinétique pVe²/2 (théorème deTorricelli) ; pghi = pVe²/2=>Ve² = 2ghi et Ve =√2ghi.
En substituant Ve = √2ghi dans la formule de continuité, Q= SV, on obtient Q= S √2ghi, d’où S, surface de l’orifice, S = Q/ √2g √hi.
La racine carrée de 2g (2 × 980 cm·s-2) est égale à 44,3.
Cette formule est un peu inexacte car, d’une part, la vitesse réelle et le débit sont inférieurs aux valeurs théoriques, et la surface réelle, supérieure.
Il faut donc introduire un facteur de correction empirique, C.
Et, d’autre part, dans le système circulatoire, les pressions dépendent des forces cardiaques et les orifices sont noyés : h est en fait le gradient des pressions existant de côté (hi) et d’autre (he) de l’orifice.
D’où, S = Q/(C × 44,3 √[hi - he]).
2- Pressions cardiovasculaires :
Les pressions cardiovasculaires dépendent des conditions de l’activité cardiaque et des relations qui existent entre la contraction cardiaque, le volume de sang, la distensibilité des parois, les résistances périphériques, les forces de gravitation, l’inertie et la tension des tissus.
Le système circulatoire comprend un élément moteur, le coeur, dont l’activité est cyclique et analogue à celle de deux pompes, le coeur droit et le coeur gauche, fonctionnant côte à côte d’une manière semblable, mais sous des régimes de pressions différents face à deux résistances inégales.
Chacune des deux pompes, droite et gauche, est formée de deux chambres, auriculaire et ventriculaire, se contractant successivement.
L’activité cardiaque comporte une suite de systoles ou contractions et de diastoles ou relaxations.
Les ventricules ont une valve d’admission qui les sépare des oreillettes (valves auriculoventriculaires) et empêche le reflux du sang au moment de l’énergique contraction ventriculaire, et une valve d’éjection, qui les sépare des artères (valves sigmoïdes) et s’oppose au reflux du sang vers les ventricules pendant la diastole.
Bien qu’il existe une diastole et une systole auriculaire et ventriculaire, ces termes, employés sans adjectif, s’appliquent surtout aux ventricules.
Le cœur doit assurer un débit adéquat face à des résistances variables, à un niveau de pression relativement stable ; il fournit l’énergie cinétique et de pression nécessaires au déplacement du sang.
Les vaisseaux sont le réseau de distribution du courant sanguin.
Les artères, élastiques, transforment le débit systolique ventriculaire, discontinu, en un flux continu.
Le sang chassé dans les artères par la contraction ventriculaire pousse en avant le sang qui s’y trouvait et distend les parois des vaisseaux.
L’élasticité artérielle permet aux vaisseaux d’absorber un volume supplémentaire de sang pendant l’éjection.
Les artères stockent, pendant la systole, une énergie qui est libérée en diastole ; elles maintiennent ainsi un flux presque continu et une pression moyenne plus élevée que celle de tubes rigides.
Les artères se divisent et se subdivisent, pour donner des « artérioles » qui conduisent vers des vaisseaux extrêmement fins, les capillaires, dont le calibre est à peu près celui d’un globule rouge (3 à 5 ím).
Le calibre et la tension vasculaires artériolaires conditionnent l’importance des résistances et des débits.
Le système artériel, à hautes pressions, est un système « résistant ».
Les résistances artérielles systémiques sont dix fois plus élevées que les résistances artériolaires pulmonaires.
La surface vasculaire, qui est de 3 cm² au niveau de l’orifice aortique, augmente à mesure que les artères se divisent.
La surface totale des capillaires est à peu près de 3 000 cm².
La vitesse du sang est de 30 cm·s-1 à la racine de l’aorte, et de 0,5 mm·s-1 dans les capillaires.
Ceci facilite les échanges dont dépend la vie cellulaire.
La surface vasculaire diminue ensuite depuis les capillaires jusqu’aux veines caves, en même temps que la vitesse du sang augmente.
La vitesse moyenne du sang dans les veines caves est de 20 cm·s-1.
Dans les veines, les pressions sont basses.
Le système veineux est un système « capacitant », sorte de réservoir dans lequel les pressions résultent surtout de la relation existant entre le volume de sang et la distensibilité des parois vasculaires, de la gravitation et de la tension des tissus.
Le ventricule droit, l’AP et ses branches, les capillaires et les veines pulmonaires et l’oreillette gauche forment la petite circulation ; le ventricule gauche, l’aorte, les artères et capillaires périphériques, les veines caves et l’oreillette droite, la grande circulation.
G - Cycle cardiaque :
L’enregistrement des pressions auriculaires, ventriculaires et artérielles permet de reconnaître dans l’activité cyclique du coeur sept phases successives, énoncées ci-après.
* Phase de remplissage ventriculaire lent :
L’oreillette et le ventricule communiquent largement.
La valve auriculoventriculaire est ouverte.
L’apport de sang par la voie d’admission est continu.
La valve sur la voie d’éjection est fermée.
* Phase de contraction auriculaire :
La contraction auriculaire chasse le sang en amont et en aval.
Elle rouvre les valves auriculoventriculaires, qui tendent ensuite à se rapprocher, comme conséquence des remous et du remplissage ventriculaire.
* Phase de contraction ventriculaire préisovolumétrique :
La mise en tension du ventricule augmente la pression ventriculaire et assure la fermeture de la valve auriculoventriculaire.
La valve d’éjection demeure fermée.
* Phase de contraction ventriculaire isovolumétrique :
Le ventricule se contracte, toutes valves fermées, à volume constant.
La pression intraventriculaire s’élève.
* Phase d’éjection ventriculaire :
Dès que la contraction ventriculaire atteint une énergie-pression suffisante, les valves sigmoïdes s’ouvrent (point e qui coïncide avec le pied de l’ascension systolique des pressions aortique ou artérielle pulmonaire) et permettent l’écoulement du sang vers les artères.
Après un certain temps (0,10 à 0,15 seconde), le ventricule commence sa relaxation.
La pression baisse. Dès que celle-ci atteint un seuil critique, la valve sigmoïde se ferme, marquant la fin de l’éjection point i ou incisure catacrote des courbes de pressions artérielles sus-sigmoïdiennes (aortique ou pulmonaire).
* Phase de relaxation ventriculaire isovolumétrique :
La pression ventriculaire baisse, avec les valves fermées, à volume constant.
L’ouverture des valves auriculoventriculaires marque la fin de cette période.
* Phase de remplissage ventriculaire rapide :
Le ventricule continue sa relaxation, la pression ventriculaire devient inférieure à la pression auriculaire, la valve auriculoventriculaire s’ouvre. L’oreillette, qui a poursuivi son remplissage pendant les quatre phases précédentes, se vide rapidement dans le ventricule.
Classiquement, la systole ventriculaire englobe les phases 3 (contraction pré-isovolumétrique), 4 (contraction isovolumétrique) et 5 (éjection ventriculaire) ; et la diastole ventriculaire, les phases 6 (relaxation isovolumétrique), 7 et 1 (remplissage ventriculaire rapide et lent), et 2 (remplissage systolique auriculaire).
La systole auriculaire se résume à la phase 2 ; les autres phases correspondent à la diastole auriculaire. Les cavités droites et gauches du coeur sont le siège des mêmes phénomènes hémodynamiques ; la morphologie des courbes de pression est similaire, seuls diffèrent les points indiqués ci-dessous.
+ Chronologie des accidents :
La contraction auriculaire droite précède de 0,02 s celle de l’oreillette gauche.
Il existe, normalement, un intervalle de 0,04 s entre le début de la dépolarisation ventriculaire gauche (onde Q de l’électrocardiogramme) et la montée de la pression ventriculaire gauche (intervalle électromécanique).
La pression télédiastolique ventriculaire gauche coïncide, généralement, avec le sommet de l’onde R de l’électrocardiogramme en V6.
Le début de la montée de la pression ventriculaire droite survient de 0,06 à 0,065 seconde après le début de l’onde Q de l’électrocardiogramme.
Le cheminement particulier de l’activation et les conditions hémodynamiques différentes qui règnent dans le coeur droit et gauche entraînent un asynchronisme des deux pompes.
En commençant avec le complexe QRS, la fermeture et l’ouverture des valves se fait, habituellement, dans l’ordre suivant : fermeture de la valve mitrale (FM), fermeture de la valve tricuspide (FT), ouverture des sigmoïdes pulmonaires (OSP), ouverture des sigmoïdes aortiques (OSA), éjection, fermeture des sigmoïdes aortiques (FSA), fermeture des sigmoïdes pulmonaires (FSP), ouverture tricuspide (OT), ouverture mitrale (OM).
La période de fermeture de la valve auriculoventriculaire gauche encadre la période de fermeture de la valve auriculoventriculaire droite et la période d’éjection du ventricule droit encadre la période d’éjection du ventricule gauche.
+ Niveau des pressions, plus élevé dans les cavités gauches :
Dans le système cardiovasculaire, la charge totale ou énergie mécanique du sang baisse d’un bout à l’autre de chacune des deux circulations, des ventricules aux oreillettes.
L’énergie cinétique est maximale aux deux extrémités de chacune des deux circulations, aorte et veines caves,AP et veines pulmonaires.
L’énergie de pression est maximale dans les ventricules.
La brièveté du circuit et le faible degré des résistances pulmonaires ont pour effet d’aligner les pressions télédiastolique ventriculaire gauche, moyenne auriculaire gauche, moyenne « capillaire » pulmonaire et diastolique artérielle pulmonaire.
1- Courbes de pression normales :
Sur les courbes de pression auriculaires, la contraction de l’oreillette, qui précède celle du ventricule, se marque par un accident positif, l’onde a.
La fermeture de la valve auriculoventriculaire, liée à la montée de la pression dans les ventricules, s’accompagne d’un accident positif, c, qui survient au début de la contraction isovolumétrique du ventricule.
La relaxation de l’oreillette et l’abaissement du plancher ventriculaire pendant la période d’éjection du ventricule déterminent une chute de la pression, dépression x.
Puis, le remplissage auriculaire se complète et entraîne une remontée de la pression, onde v.
L’ouverture de la valve auriculoventriculaire donne lieu à une chute de la pression auriculaire, du sommet de l’onde v jusqu’à un creux, y.
L’onde a est généralement supérieure à l’onde v et la dépression x plus profonde que la dépression y.
Oreillette et ventricule se comportent ensuite comme une cavité unique, jusqu’au cycle suivant.
Sur les courbes de pression ventriculaires, la contraction des ventricules donne lieu, pendant les phases pré-isovolumétrique (1-2), isovolumétrique (2-3) et première moitié de l’éjection (3-), à une montée de la pression qui atteint rapidement un maximum. Puis l’énergie de la contraction diminue et la relaxation commence, la pression décline, l’éjection se termine (-4) et les valves sigmoïdes se ferment (-4-).
Après la fermeture des sigmoïdes, la pression chute rapidement (phase de relaxation isovolumétrique, 4-5), la valve auriculoventriculaire s’ouvre (-5-) et le remplissage ventriculaire commence.
Celui-ci comprend trois phases :
– de remplissage rapide, pendant lequel 80 % du volume systolique passe de l’oreillette au ventricule ; la pression ventriculaire descend jusqu’à son point le plus bas qui indique la pression protodiastolique, puis remonte, dessinant généralement une discrète onde F ou R (de filling : remplissage) ;
– de remplissage lent (6-7), qui donne lieu à une ascension lente de la pression ;
– de remplissage actif, dû à la systole auriculaire qui entraîne une discrète remontée arrondie de la pression ventriculaire, l’onde a (-8-).
La systole ventriculaire s’étend du début de la montée de la pression (1, point z) à la fermeture des valves sigmoïdes (-4-, i).
La diastole ventriculaire commence un peu avant le point i, et s’étend jusqu’au point z suivant. Les courbes de pression artérielles sont superposables aux courbes de pression du ventricule correspondant pendant l’éjection, du point e au point i ou incisure catacrote (3-4), de l’ouverture à la fermeture des valves sigmoïdes.
La contraction ventriculaire donne lieu à un ébranlement liquidien qui crée une onde de pression qui va se propager le long des artères, déformer leur paroi élastique et provoquer un déplacement du sang.
Dans les artères, l’onde de pression, ou onde élastique transverse, est surtout la conséquence du choc (ou « coup de bélier ») du sang, chassé par les ventricules, avec le sang artériel.
La réflexion de l’ondée systolique artérielle sur les valves sigmoïdes fermées entraîne une réascension de la courbe en protodiastole, c’est le ressaut ou onde dicrote.
La pression descend ensuite régulièrement jusqu’à la systole suivante.
Les pressions artérielles qui varient de façon cyclique, en raison de l’alternance des systoles et diastoles ventriculaires, résultent de l’action conjuguée du débit systolique, des résistances artériolaires et des particularités physiques des vaisseaux.
Les phases de contraction pré-isovolumétrique et isovolumétrique ventriculaires constituent la période de contraction préexpulsive ou de prééjection.
* Pressions artérielles :
L’onde de pression artérielle est un phénomène complexe de fréquence N(égale à la fréquence cardiaque) qui comprend des ondes incidentes et réfléchies et qui répond au théorème de Fourier, et qui se modifie à mesure qu’elle s’éloigne du coeur : elle devient de plus en plus pointue, l’encoche et l’onde dicrotes s’effacent, la pression systolique s’accroît (comme conséquence de la diminution du calibre artériel, de l’augmentation progressive de la rigidité de la paroi et de la disparition des ondes de réflexion), la pression moyenne diminue.
La pression systolique artérielle fémorale est généralement supérieure à la pression systolique aortique.
La vitesse de propagation de l’onde de pression dans les artères, Co, est normalement de 4 à 6 m/s.
Elle dépend de l’élasticité E et de l’épaisseur h de la paroi ; elle est une fonction inverse du diamètre D du vaisseau et de la masse volumique ò du sang.
* Paramètres normaux de pression :
Les pressions auriculaires sont définies par la pression moyenne et par la valeur de ses accidents les plus caractéristiques (ondes a, c, x, v et y).
La pression moyenne représente la moyenne de toutes les pressions instantanées.
Elle peut être calculée sur les courbes, par planimétrie, ou obtenue directement par intégration électrique.
La pression auriculaire droite moyenne est, normalement, inférieure à 6 mmHg (0,8kPa), avec une onde a de moins de 8 mmHg (1,06kPa).
La pression capillaire pulmonaire est un reflet de la pression auriculaire gauche, sauf dans les cas où il existerait un obstacle à la transmission de la pression auriculaire gauche vers le territoire capillaire (thrombose des veines pulmonaires, myxome ou thrombose auriculaire gauche obstruant l’abouchement des veines pulmonaires...).
La pression capillaire pulmonaire moyenne et la pression télédiastolique ventriculaire gauche sont, normalement, inférieures à 13 mmHg (1,73kPa). Les pressions ventriculaires sont définies par trois paramètres :
– la pression systolique, qui correspond au pic maximal de pression ;
– la pression protodiastolique, qui est la pression la plus basse, après l’ouverture de la valve auriculoventriculaire ;
– la pression télédiastolique, qui coïncide avec le point z, après la systole auriculaire, au début de la contraction ventriculaire.
La pression systolique ventriculaire droite est inférieure à 32 mmHg (4,26kPa), et la pression télédiastolique inférieure à 8 mmHg(1,06kPa).
Les pressions protodiastoliques ventriculaires sont, normalement, très proches de zéro, inférieures à 1 mmHg(0,13kPa) dans le ventricule droit et à 5 mmHg (0,67kPa) dans le ventricule gauche.
Les pressions artérielles sont caractérisées par trois paramètres :
– la pression systolique, pic maximal de la pression systolique ;
– la pression diastolique, point le plus déclive de la courbe, correspondant au début de l’éjection ventriculaire ;
– la pression moyenne.
La pression moyenne artérielle pulmonaire est, normalement, inférieure à 19 mmHg (2,53kPa).
La pression moyenne artérielle systémique vaut, normalement, entre 70 et 105 mmHg (de 9,31 et 13,97kPa).
* Modifications des pressions dans les cardiopathies :
L’analyse du niveau des pressions et de leur morphologie dans les cardiopathies ainsi que l’étude des gradients, différences de pression, qui pourraient exister entre deux points contigus du système cardiovasculaire, au cours des retraits de la sonde, ou sur des enregistrements simultanés, permettent souvent à eux seuls le diagnostic et l’évaluation de la gravité des lésions.
La pression auriculaire droite (PADou POD) est un reflet des conditions de travail du coeur droit. Dans la communication interauriculaire, la POD moyenne, en l’absence d’une HTAP, est généralement normale.
L’onde a est à peu près identique aux ondes c et v.
Dans l’insuffisance tricuspide, la régurgitation atténue ou fait disparaître la dépression x, et donne lieu à une POD systolique positive.
Les insuffisances tricuspides massives, traumatiques ou congénitales, donnent des POD qui ressemblent à des pressions ventriculaires .
La pression systolique ventriculaire droite est, dans ces cas, généralement normale.
La valve incompétente s’oppose au développement d’une HTAP, le ventricule se vidant facilement dans l’oreillette.
Dans le rétrécissement tricuspide, la POD est augmentée, la vitesse de chute de l’onde v est lente, le creux y n’atteint pas le zéro, son nadir est très au-dessus de la pression protodiastolique ventriculaire .
Il existe un gradient diastolique entre les pressions auriculaire et ventriculaire droites.
Le rétrécissement tricuspide s’associe habituellement à une insuffisance tricuspide.
La POD comporte, dans ces cas, les déformations propres des deux lésions. Les tracés les plus typiques de péricardite chronique constrictive s’observent chez des patients en fibrillation auriculaire.
Dans ces cas, la pression auriculaire droite dessine unMen systole, qui va être suivie d’une dépression y, très acuminée, et d’un long plateau horizontal.
Cette courbe rappelle le signe de la racine carrée et est habituellement connue sous le nom d’aspect en « dip-plateau ».
Des tracés similaires peuvent se voir, aussi, dans les restrictions fixes de toute autre origine (myocardiques ou endocardiques).
La PVD systolique est généralement normale dans l’insuffisance tricuspide massive, d’origine bactérienne, traumatique ou congénitale, et dans la péricardite chronique constrictive.
La pression télédiastolique est élevée dans les deux cas.
Dans les péricardites chroniques constrictives, la PVD représente souvent plus du tiers de la pression systolique.
La PVD est augmentée dans les insuffisances tricuspides qui s’associent à une atteinte du coeur gauche, généralement lésions de la valve mitrale qui entraînent une HTAP, et dans les syndromes de restriction d’origine myocardique, qui touchent préférentiellement le ventricule gauche.
La PVD est élevée s’il existe un obstacle à l’éjection ventriculaire, HTAP ou sténose pulmonaire (supravalvulaire, valvulaire, infundibulaire ou médioventriculaire).
La pression artérielle pulmonaire est basse dans les sténoses pulmonaires.
Dans les insuffisances mitrales aiguës, récentes et importantes, dues à une endocardite bactérienne ou à une rupture des cordages, la pression artérielle pulmonaire montre parfois un aspect en M, formé par la succession de l’onde systolique et d’un ressaut protodiastolique très marqué, qui s’ajoute ou se substitue à l’onde dicrote.
Ce ressaut, qui coïncide avec l’onde v capillaire, résulterait de la régurgitation mitrale, dans un système vasculaire encore peu altéré.
L’HTAP est une éventualité fréquente dans les cardiopathies.
Elle est précapillaire si la pression capillaire est normale, postcapillaire si la pression capillaire est élevée et l’écart des pressions moyennes artérielle pulmonaire et capillaire (PAPm-PCapm) inférieur à 10 mmHg(1,33kPa).
Elle est mixte, à la fois pré- et postcapillaire, si la pression capillaire est augmentée et la différence entre les deux pressions (PAPm-PCapm) supérieure à 10 mmHg (1,33kPa).
Dans l’HTAP précapillaire, les résistances « capillaires » pulmonaires sont normales et les résistances artériolaires accrues. Dans l’HTAP postcapillaire, les résistances artériolaires sont normales et les résistances « capillaires » augmentées. Dans l’HTAP mixte, les deux résistances sont élevées.
La pression capillaire pulmonaire dans les cardiopathies va dépendre non seulement de la pression auriculaire gauche mais aussi de la capacité et distensibilité de l’oreillette et du système veineux pulmonaire. Dans le rétrécissement mitral, la pression capillaire est uniformément élevée et les accidents sont de faible amplitude ; les ondes a, c et v sont à peu près égales, de même que les dépressions x et y.
La vitesse de chute de l’onde v est lente.
Si le patient est en fibrillation auriculaire, l’onde a manque. Dans l’insuffisance mitrale, le creux x tend à disparaître et l’onde v devient très haute, très pointue, avec une montée et une descente très rapides.
Dans les cardiopathies mitrales associant à la fois un certain degré de sténose et d’insuffisance valvulaires, communément appelées en France « maladies mitrales », le diagnostic de l’obstruction est généralement facile s’il existe un gradient holodiastolique « ventricule gauche-capillaire » et si la chute de l’onde v est lente.
Il est en revanche difficile d’affirmer, sur la seule analyse de la pression capillaire, la présence d’une régurgitation mitrale et plus encore, de déterminer l’importance relative de chacune des deux lésions.
Dans l’insuffisance aortique, la pression capillaire peut être normale ou élevée.
L’enregistrement simultané des pressions capillaire et ventriculaire gauche fait souvent apparaître, dans ces cas, un croisement mésodiastolique des deux courbes, la pression ventriculaire se plaçant au-dessus de la pression capillaire en télédiastole, les deux pressions dessinent un X.
Dans les restrictions cardiaques, les caractères de la pression capillaire sont similaires à ceux déjà décrits pour la pression auriculaire droite.
La pression télédiastolique ventriculaire gauche est généralement élevée dans les cardiopathies gauches. Dans les syndromes restrictifs, la pression ventriculaire gauche présente, pendant la diastole, un aspect caractéristique, avec une dépression précoce, aiguë et profonde (le dip) et un plateau bien défini ; la pression télédiastolique est augmentée, mais ne représente habituellement pas plus de 20 %de la pression systolique.
Dans le rétrécissement aortique valvulaire, supravalvaire ou sousvalvaire fixe, la pression aortique comporte un ralentissement de la branche anacrote qui culmine en un sommet unique et tardif.
Le temps de demi-ascension dépasse 0,05 seconde et le temps d’éjection est allongé.
Dans les cardiomyopathies primitives hypertrophiques obstructives, la pression aortique montre en systole une montée rapide, vers un premier sommet précoce, qui est suivie d’une dépression mésosystolique.
L’insuffisance aortique donne une courbe à double sommet de hauteur approximativement égale (bisfériens) ou à sommet unique, relativement tardif ; l’incisure catacrote est effacée, et la pression diastolique très basse, pouvant atteindre, dans les régurgitations importantes et lors des diastoles longues, la pression télédiastolique ventriculaire gauche.
* Retraits de pression :
L’enregistrement des retraits, c’est-à-dire de la pression au cours du passage de la sonde d’un point à l’autre du système cardiovasculaire, est très important pour reconnaître l’existence d’un gradient, différence de pression, donc d’un obstacle, de son siège et de sa nature.
Il est nécessaire d’obtenir au cours du cathétérisme au moins un retrait à partir des branches droite et gauche de l’AP jusqu’au tronc de celle-ci, de l’AP dans le ventricule droit (AP-VD), du ventricule dans l’oreillette droite (VD-OD) et du ventricule gauche dans l’aorte (VG-Ao).
Le retrait depuis les branches droite et gauche de l’AP jusqu’au tronc autorise le diagnostic de sténose ou coarctation des branches, s’il existe un gradient égal ou supérieur à 5 mmHg (0,7kPa) et un changement de la morphologie des courbes.
Certains auteurs ne retiennent comme significatifs que des gradients supérieurs à 10 ou 20 mmHg (1,3 à 2,7kPa).
L’existence, sur les retraits AP-VD, d’un gradient systolique supérieur à 10 mmHg (1,33kPa), en l’absence de court-circuit de gauche à droite, et supérieur à 30 mmHg (4kPa), en cas de shunt de gauche à droite, est le propre des rétrécissements pulmonaires.
L’analyse du tracé et la situation dans le cœur du point de changement de pression permettent, généralement, d’établir le siège et la nature de la sténose, supravalvulaire, valvulaire ou infundibulaire, musculaire ou fixe.
La pression systolique ventriculaire droite en deçà de l’obstacle dépasse 30 mmHg (4kPa), la pression artérielle pulmonaire est basse. Dans les communications interauriculaires avec un shunt important de gauche à droite et un rapport des débits pulmonaire et systémique très au-dessus de 3 (DP/DS supérieur à 3), des gradients systoliquesAP-VD de 30 et même 50 mmHg (4 et 6,65kPa), peuvent n’être que fonctionnels.
Dans les dilatations idiopathiques de l’AP, la pression ventriculaire droite est normale, même s’il existe un gradient AP-VD significatif.
Dans les sténoses pulmonaires fixes, généralement valvulaires, serrées, il existe sur les courbes de pression artérielles pulmonaires, au moment du passage à travers l’orifice, une dépression systolique, conséquence de l’effetVenturi.
Le changement d’une pression basse, artérielle, en une pression haute, ventriculaire, est brusque et se fait sans transition d’un complexe à l’autre.
Dans les sténoses musculaires, généralement infundibulaires, la pression augmente graduellement : le gradient est progressif.
Dans le cas des sténoses dues à des bourrelets musculaires anormaux, les tracés ressemblent souvent à ceux observés dans les sténoses fixes. Le retrait VD-OD rend possible le diagnostic de rétrécissement tricuspide si la pression protodiastolique ventriculaire est au-dessous du creux y auriculaire et si, en moyenne, la pression auriculaire est supérieure à la pression diastolique ventriculaire.
Le retrait VG-Ao permet de faire le diagnostic de rétrécissement aortique s’il existe un gradient et d’établir sa nature, fixe ou musculaire (dynamique), et son siège, sous-valvulaire, valvulaire ou supravalvulaire.
Dans le rétrécissement sous-aortique, le gradient est intraventriculaire.
La différence de pression s’inscrit entre deux complexes de morphologie ventriculaire.
Dans la chambre sousvalvulaire à basse pression, la pression systolique est égale à la pression aortique, la pression diastolique est ventriculaire.
Si la sténose est fixe, diaphragme sous-valvulaire, la pression aortique est vibrée avec une branche anacrote tantôt rapide, tantôt lente.
Si la sténose est musculaire, cardiomyopathie primitive hypertrophique obstructive, la pression aortique a l’aspect caractéristique décrit plus haut.
Dans le rétrécissement aortique valvulaire ou supravalvulaire, le gradient ou différence de pression se produit entre un complexe de morphologie ventriculaire et un complexe artériel (sténose valvulaire), ou entre deux complexes de morphologie artérielle (sténose supravalvulaire).
2- Calcul des surfaces valvulaires :
Dans le cas des obstacles fixes, il est possible de calculer la surface de l’orifice rétréci, grâce aux formules de Gorlin et Gorlin.
Il est nécessaire de connaître pour cela le flux à travers la sténose, en mL/s, et le gradient moyen, ou différence moyenne des pressions de côté et d’autre de l’obstruction, en mmHg ou kPa, pendant le temps de passage du sang.
Le gradient moyen peut être calculé ou mesuré sur les courbes de retrait ou sur les enregistrements simultanés des pressions des compartiments situés en amont et en aval de l’obstacle : OD-VD en cas de rétrécissement tricuspide, VD-AP dans la sténose pulmonaire, CP-VG dans le rétrécissement mitral, VG-Ao ou artère périphérique dans les sténoses aortiques.
S’il s’agit d’un retrait ou si l’on utilise comme pression artérielle, dans les rétrécissements aortiques, des pressions périphériques, humérale ou fémorale, il faut les superposer convenablement.
Le gradient moyen est calculé, généralement, par planimétrie.
La surface, mesurée en mm², est divisée par la duréelargeur en mm de ce gradient, de façon à obtenir la hauteur moyenne.
Celle-ci est alors exprimée en mmHg ou kPa, en tenant compte de la sensibilité.
Le gradient doit exister tout au long de la diastole.
Pour calculer le flux à travers l’obstacle, en mL/s, il faut diviser le débit, en mL/min, par la durée du flux en s/min.
Les surfaces valvulaires aortique et pulmonaire peuvent aussi être estimées rapidement grâce à la formule abrégée de Hatti : surface valvulaire en cm² = débit cardiaque, en L/min, divisé par la racine carrée du gradient pic à pic en mmHg.
Le gradient pic à pic est à peu près égal au gradient moyen.
3- Oxymétrie :
* Oxymétrie sanguine et « séries » :
Le cathétérisme cardiaque permet le prélèvement d’échantillons de sang, à divers niveaux dans les différentes cavités cardiaques, et la mesure de leur teneur en oxygène.
Les résultats obtenus autorisent, d’une part, le calcul du débit cardiaque par application de la méthode de Fick direct oxygène et l’appréciation de la capacité fonctionnelle du myocarde, et, d’autre part, le diagnostic des shunts et le calcul de leur volume.
L’endroit du prélèvement doit être reconnu. La position de la sonde est identifiée, grâce à la radioscopie, par l’analyse des pressions et, si besoin, par l’injection d’un indicateur.
De façon systématique, même dans le cas des cardiopathies valvulaires ou ischémiques, et en l’absence de toute suspicion clinique de court-circuit, des échantillons de sang des veines caves inférieure et supérieure et de l’AP sont obtenus dès le début de l’exploration, afin d’exclure l’existence d’un shunt significatif. Dans les cas où un court-circuit est soupçonné, il faut effectuer ce que l’on nomme une « série ».
* Méthodes et unités de mesure :
La teneur en oxygène d’un échantillon de sang peut être exprimée de trois façons :
– comme un pourcentage de l’oxygène fixé par l’hémoglobine dans l’échantillon, saturation en oxygène, par rapport à sa capacité (CapaO2), qui est la quantité maximale d’oxygène que peut fixer ce sang ; c’est ce que l’on appelle la saturation oxygénée ;
– en volumes, mL d’oxygène dans 100 mL de sang ; – en termes de pression partielle.
La valeur moyenne de la capacité oxygénée, chez l’adulte normal, est de 20 volumes oumLpour 100 mLde sang.
Elle est plus basse chez le sujet âgé (16 à 17 volumes), chez l’enfant (12 à 15 volumes) et chez les sujets anémiques, et supérieure chez les sujets polyglobuliques (24 à 30 volumes).
Elle varie, chez un même malade, à l’effort, aux émotions ou sous l’influence de drogues diverses et doit donc être mesurée, au cours d’une même exploration, chaque fois que l’état fonctionnel a pu être modifié.
Le contenu en oxygène du sang, en volumes ou mL, peut être mesuré ou calculé à partir de la capacité et de la saturation :
volumes ou mL = saturation % × capacité en volumes pour 100 mL de sang.
* Oxymétrie normale :
Le sang est oxygéné dans les poumons.
Dans les capillaires et les veines pulmonaires, l’oreillette et le ventricule gauches, et les artères systémiques, le sang est bien saturé en oxygène : il est dit « artériel ».
La valeur normale de la saturation oxygénée du coeur gauche se situe autour de 95 %, entre 100 et 93 %.
Cette situation est uniforme dans toute la circulation gauche (veines pulmonaires, oreillette et ventricule gauches, aorte et ses branches).
Dans les veines périphériques, les veines caves, l’oreillette et le ventricule droits, l’AP et ses branches, le sang est « désaturé », pauvre en oxygène : il est dit « veineux ».
Le contenu en oxygène du sang veineux est différent d’un point à l’autre, du fait de la variabilité de la saturation du sang provenant des divers territoires de l’organisme.
Chez le sujet normal, le sang de la veine cave supérieure a une saturation de 74 % en moyenne (extrêmes : 70-80 %), alors que celui de la veine cave inférieure a une saturation moyenne beaucoup plus élevée, autour de 78 % (extrêmes : 74 à 85 %), du fait du retour du sang fortement saturé des veines rénales.
Les reins, qui assurent l’épuration du sang, ont un débit important, très au-dessus de leurs besoins en oxygène.
La différence artérioveineuse en oxygène des reins est faible.
Dans l’oreillette droite se mélangent le sang des deux veines caves et celui très désaturé du sinus coronaire.
Des échantillons prélevés à divers niveaux dans cette cavité peuvent avoir des valeurs différentes, variant de 72 à 78 %.
La saturation oxygénée de l’oreillette droite peut être, dans certains cas, au-dessus de celle de la veine cave supérieure, mais ne dépasse pas celle-ci de plus de 9 % en l’absence de tout shunt.
Dans le ventricule droit, le mélange des sangs veineux est plus homogène et la saturation en oxygène prend des valeurs comprises entre 73 et 77 %.
Ces valeurs ne dépassent normalement pas de plus de 5 % celles de l’oreillette.
Dans l’AP, le mélange des sangs est plus homogène et représente le sang veineux mêlé.
La saturation d’un échantillon de l’AP ne dépasse pas celle du ventricule droit de plus de 5 %, en l’absence de tout shunt.
Lorsque la sonde est poussée dans les petites branches de l’AP jusqu’à bloquer son extrémité, le sang aspiré à cet endroit a une saturation élevée, égale à celle des veines pulmonaires.
Ce sang est dit « capillaire pulmonaire ».
Le contenu en oxygène du sang varie avec la capacité oxygénée.
Chez le sujet normal ayant une capacité de 20 volumes, c’est à dire 20 mL d’oxygène dans 100 mL, le sang artériel systémique saturé à 96 % contient 19,2 volumes d’oxygène (0,96 × 20 = 19,2) et le sang veineux mêlé, artériel pulmonaire, saturé à 75 %, 15 volumes (0,75 × 20 = 15).
La différence artérioveineuse systémique en oxygène, contenu en sang « artériel », périphérique ou central, moins le contenu en oxygène du sang « veineux mêlé », ouDAVO2, est en moyenne de 4,2 volumes pour 100 (de 3 à 5), soit 42 mL/L.
4- Débit cardiaque :
Le débit cardiaque, Q pointé ou Q, est la quantité de sang expulsée, par unité de temps, par le ventricule gauche vers la périphérie (débit systémique ou QS), et par le ventricule droit vers les poumons (débit pulmonaire ou QP).
Le débit cardiaque variant avec la surface corporelle, SC, il est habituel de le rapporter à celle-ci, estimée en m² d’après la formule de Dubois et Dubois (qui tient compte du poids P en kg et de la taille T en cm, SC en m² = 0,0072 × P0,425 × T0,725).
C’est l’index cardiaque ou IC exprimé usuellement en litres par minute par mètre carré de SC (L·min-1·m-2).
* Principe de Fick :
La mesure du débit cardiaque peut être effectuée par la méthode dite de Fick direct oxygène, ou grâce à l’injection d’un indicateur, vert d’indocyanine ou froid.
D’après le principe de Fick, le produit du débit (Qaf) par la concentration d’une substance (Caf) dans le sang afférent par rapport à un organe, plus ou moins la quantité de cette substance ajoutée ou perdue lors du passage à travers l’organe (m), est égal au produit du débit (Qef) par la concentration (Cef) de cette substance dans le sang efférent :
Qaf × Caf ± m = Qef × Cef -> Q= m/(Cef - Caf)
les débits entrants et sortants étant peu différents.
* Mesure du débit cardiaque par la méthode de Fick direct oxygène :
La mesure du débit cardiaque par la méthode de Fick direct oxygène est basée sur le fait que les poumons fixent, sur le sang éjecté par le ventricule droit, l’oxygène (élément facilement mesurable) contenu dans l’air ambiant.
C’est « dans les poumons que le sang subtil se mélange à l’air inspiré pour servir de base à l’esprit vital » (Michel de Servet, 1553).
Le débit du ventricule droit (Qd), multiplié par le contenu en oxygène du sang artériel pulmonaire (cont 02 AP ou veineux mêlé, CvßO2), plus la consommation, ou extraction d’oxygène (VO2) effectuée par les poumons sur l’air respiré, est à peu près égal au débit du ventricule gauche (Qg), multiplié par le contenu en oxygène du sang systémique, ventricule gauche, aorte ou artère périphérique (CaO2), :
Qd × CvßO2 + VO2 = Qg × CaO2 ;
d’où :
Q= VO2/(CaO2 - CvßO2)
La consommation, ou extraction d’oxygène, VO2, est exprimée en mL·min-1 ; les contenus en mL ou volumes pour 100 mL de sang.
Le débitQ, en L·min-1, est égal àVO2 /10 (CaO2 - CvßO2).
Le sang veineux mêlé doit être aspiré dans l’AP ; en cas d’impossibilité majeure, et en l’absence de shunt, le prélèvement veineux peut être fait dans le ventricule droit.
CaO2 - CvßO2 est la différence artérioveineuse (systémique) en oxygène, DAV ou DAVO2.
La consommation, captation ou extraction d’oxygène de l’organisme, ouVO2, est, chez l’homme au repos et dans des conditions normales de température et d’équilibre psychique, presque une constante, qui ne dépend que des besoins en oxygène de l’organisme et qui est fonction de la surface corporelle.
La quantité d’oxygène transportée par le sang aux tissus de l’organisme (TrO2) est égale au produit du débit cardiaqueQC par le contenu en oxygène du sang artériel CaO2 (QC × CaO2).
Avec un débit cardiaque normal, la consommation d’oxygène ouVO2 représente moins de 26 % de tout l’oxygène transporté : (VO2/TrO2) < 0,26.
Ce rapport, qui exprime le pourcentage d’utilisation d’oxygène, peut être estimé par le quotient de la différence artérioveineuse DAV sur le contenu artériel CaO2 en oxygène.
En effet :
QC = VO2/DAV=>VO2 = Q ?C × DAVet TrO2 = QC × CaO2
d’où :
VO2/TrO2 = Q ?C × DAV/QC × CaO2 = DAV/CaO2
La valeur moyenne de la consommation d’oxygène, observée chez 100 patients consécutifs étudiés dans notre laboratoire, 60 hommes et 40 femmes, d’âge moyen 45,2 ± 15 ans (extrêmes : 17 et 75), et dont la surface corporelle est de 1,67 ± 0,2 m², est de 151,3 ± 25 mL·min-1·m-2 chiffre un peu supérieur à celui de la littérature, qui est de 143 ± 14 mL·min-1·m-2.
* Mesure du débit cardiaque par les courbes de dilution :
+ Principe de Stewart-Hamilton :
Les méthodes de mesure du débit cardiaque basées sur l’analyse des courbes de dilution, obtenues après injection de l’embole d’un indicateur, ont été introduites par Stewart en 1897 et généralisées, grâce aux travaux de Hamilton et al, à partir de 1929.
Ces méthodes constituent aussi une application du principe de Fick.
Les courbes de dilution sont des courbes des variations de la concentration d’un indicateur (substance pouvant être décelée facilement dans le sang par un détecteur approprié) dans un point du système circulatoire (enregistrée en ordonnée) en fonction du temps (enregistré en abscisse), après l’injection soudaine d’une certaine quantité de cette substance dans un autre point du système circulatoire (situé généralement en amont du premier).
L’adjonction à un fluide d’une quantité connue mi d’un indicateur permet de connaître le volume V du fluide.
Il suffit de mesurer la concentration moyenne cß de l’indicateur :
mi = V × cß =>V = mi/cß.
Stewart a montré que ce calcul est valable pour un liquide circulant, le débit ou volume écoulé par unité de temps est Q = V/t = mi/cß x t, t étant la durée d’écoulement de l’indicateur en secondes.
Le débit par minute est mi × 60/cß × t.
La concentration moyenne cß est égale à la surface de la courbe de première circulation en mg·L-1·s-1 calculée en tenant compte de la vitesse d’enregistrement et du facteur de correction dû à la sensibilité de la cellule.
L’indicateur employé autrefois était le vert d’indocyanine. Aujourd’hui, on recourt surtout au froid.
+ Mesure du débit cardiaque par thermodilution :
La méthode de thermodilution utilise un indicateur thermique.
Les sondes employées pour réaliser cette technique, du type Swan-Ganz, comportent deux lumières, avec un orifice proximal et un orifice distal séparés par une distance de près de 20 cm, et une thermistance située à 2 cmde la pointe.
Une certaine quantité de sérum salé ou glucosé à 5 %, glacé (de 0 °C à 2 °C) ou à la température ambiante, est injectée soudainement dans les veines caves supérieure ou inférieure ou l’oreillette droite.
La courbe des variations de la température du sang est enregistrée grâce à la thermistance distale située dans l’AP ; ces variations modifient la résistance du capteur qui constitue le quatrième élément d’un pont de Wheatstone.
Le débit cardiaque est mesuré grâce à un traitement automatique de l’information par des calculateurs.
La thermodilution ne nécessite pas de prélèvements sanguins.
Elle oblige à vérifier la position de la sonde, de façon à éviter que la thermistance soit collée à la paroi artérielle (le ballonnet doit être à peine gonflé), et à effectuer des mesures répétées.
L’enregistrement des courbes permet de juger des qualités de la manoeuvre et de valider les résultats.
L’électrocardiogramme est obtenu simultanément afin de calculer la fréquence cardiaque.
Des échantillons de sang artériel pulmonaire et systémique sont aspirés avant ou après la mesure du débit, pour en calculer la différence artérioveineuse en oxygène (DAVO2) et la consommation d’oxygène (VO2 = QC × DAVO2).
+ Valeurs normales du débit cardiaque :
Le débit cardiaque est très variable.
Il est plus élevé chez l’homme que chez la femme.
L’index cardiaque mesuré dans le service chez des sujets âgés d’environ 40 ans, à jeun, couchés, au repos, au calme, en équilibre thermique, est en moyenne de 3,55 ± 0,75 L·min-1·m-2.
PourYang, il est de 3,5 ± 0,7.
Le débit cardiaque augmente avec la grossesse, la chaleur, la digestion, l’altitude, l’hypoxie, l’anxiété et surtout l’effort.
Il diminue avec l’orthostatisme et le vieillissement.
Brandfonbrener et al observent une diminution de près de 24,4 mL/min/année, entre 20 et 80 ans.
5- Diagnostic des shunts :
Le système circulatoire comprend deux circuits, pulmonaire et systémique, dont les débits sont à peu près égaux.
Le sang veineux, qui arrive de la périphérie par les veines caves, et passe de l’oreillette droite dans le ventricule droit et l’AP, a un contenu en oxygène bas (sang veineux).
Le sang oxygéné dans les poumons (sang artériel) a un contenu en oxygène élevé.
Un court-circuit ou shunt est le passage anormal de sang artériel dans le circuit veineux, shunt de gauche à droite (G=>D), ou de sang veineux dans le circuit artériel, shunt de droite à gauche (D=>G), ou de gauche à droite et de droite à gauche, shunt croisé (G<=>D).
Une oxymétrie normale ne permet pas d’écarter formellement une communication entre les deux circuits.
Si les pressions sont normales, cette situation peut correspondre à un shunt négligeable.
En présence d’une HTAP, elle peut conduire à un diagnostic erroné.
La détection et la localisation des shunts peut être faite au moyen de l’oxymétrie, des courbes de dilution et de l’angiocardiographie.
Elle repose surtout aujourd’hui sur l’échocardiographie.
Leur quantification est effectuée grâce à l’oxymétrie.
Les aspects anatomiques sont déduits de l’analyse du trajet des sondes, des pressions, des courbes de dilution et des angiocardiographies.
Dans les services de cardiologie pour adultes, les courbes de dilution sont actuellement très peu employées pour le diagnostic des shunts.
* Diagnostic des shunts par l’oxymétrie :
Le diagnostic des shunts par l’oxymétrie exige le prélèvement rapide d’échantillons de sang pour faire ce que l’on appelle une « série ».
Le diagnostic de la présence d’un shunt de gauche à droite et de son niveau, repose sur l’existence d’un enrichissement anormal en oxygène dans la cavité droite qui reçoit de ce fait le sang artériel.
Cet enrichissement se retrouve généralement aussi dans les cavités situées en aval.
Le diagnostic et la localisation d’un shunt de droite à gauche par l’oxymétrie sont rarement possibles.
En effet, l’existence d’une désaturation du sang ventriculaire gauche et artériel périphérique n’est pas nécessairement l’indice d’un court-circuit veinoartériel.
Elle peut relever d’une bronchopneumopathie.
« L’inhalation par le malade d’un mélange enrichi enO2 ou d’O2 pur peut permettre la discrimination entre les deux mécanismes.
S’il s’agit d’un shunt, la SaO2 sera peu modifiée.
S’il s’agit d’un trouble de l’hématose, au contraire, la SaO2 augmente et se rapproche des valeurs normales. Dans la pratique, ce test est souvent en défaut ».
Toutefois, la comparaison des prélèvements veineux pulmonaires, obtenus après franchissement d’une communication interauriculaire ou d’un foramen ovale, (ou du sang « capillaire pulmonaire »), et des prélèvements artériels périphériques effectués simultanément, permet de rapporter la désaturation artérielle à son mécanisme.
Lorsque le sang veineux pulmonaire est normalement saturé, la désaturation artérielle relève d’un shunt droit-gauche.
Lorsque la désaturation des deux échantillons est égale, celle-ci est liée à un défaut d’hématose.
L’étage du shunt peut être approché en confrontant les prélèvements veineux pulmonaire, auriculaire et ventriculaire gauches et artériels systémiques.
Dans les malformations complexes, le recours aux courbes de dilution et à l’angiocardiographie est indispensable.
* Quantification des shunts :
Elle est généralement basée sur l’analyse des oxymétries.
Les débits pulmonaires et systémiques, totaux et effectifs, doivent être calculés.
La consommation d’oxygène est mesurée ou estimée et les prélèvements veineux et artériels pulmonaires et systémiques (veine et artères pulmonaires, veines caves et artères périphériques) effectués rapidement, chaque fois que possible et nécessaire.
Si les veines pulmonaires n’ont pas été atteintes, ou si le sang « capillaire pulmonaire » n’est pas obtenu, dans les cas où la saturation des échantillons ventriculaires gauches est égale ou supérieure à 95 %, celle des veines pulmonaires est considérée comme identique ; si la saturation du ventricule gauche est inférieure à 95 %, celle des veines pulmonaires est estimée égale à 96 % et l’on accepte qu’il existe un shunt de droite à gauche si celui-ci est plausible.
Le débit pulmonaire effectif (DPE) est la quantité de sang veineux périphérique désaturé soumis chaque minute à l’hématose.
Il est égal au quotient de la consommation d’oxygène par minute (VO2) par la différence artérioveineuse des contenus en oxygène du sang veineux pulmonaire (CvpO2) et du sang veineux systémique mêlé, prélevé en amont du shunt (différence entre les contenus en oxygène du sang le mieux saturé (VP) et le plus désaturé (Vm).
Le sang veineux systémique mêlé (CvßmO2) est généralement estimé, au repos, égal à (3 VCS + 1 VCI)/4, ou 0,7 VCS + 0,3 VCI, ou, encore, au contenu en oxygène de la VCS, prélevée en amont du shunt, exprimé en mL %, plus 0,5.
Ainsi, le DPE, en L/min, est égal à : VO2/10 (CvpO2 - CvßmO2) avec laVO2 en mL/min et les contenus en oxygène en mL/100.
Le DPE est aussi le débit systémique effectif, quantité de sang normalement saturée qui atteint les cellules périphériques.
Le débit pulmonaire total (DPT), ou débit pulmonaire tout court, est la quantité de sang qui passe par minute dans la circulation pulmonaire, et dont une partie peut être déjà normalement saturée.
Le DPT est égal au quotient de la consommation d’oxygène par minute (VO2) par la différence artérioveineuse pulmonaire en oxygène ; différence des contenus en oxygène du sang qui sort des poumons (VP) et de celui qui y rentre (AP) :
DPT = VO2/10 (CvpO2 - CAPO2)
Le débit systémique total (DST), ou débit cardiaque, est la quantité de sang qui passe par minute dans la circulation générale.
Il est égal au quotient de la VO2 par la différence artérioveineuse systémique, différence dans les contenus en oxygène des sangs périphérique et veineux systémique mêlés ; différence des contenus en oxygène du sang qui va vers les tissus (Ca) et de celui qui en sort (Vm) :
DST = VO2/10 (CaO2 - CvßmO2)
Dans un shunt gauche-droit exclusif, le sang aortique a la même saturation que le sang veineux pulmonaire.
Le débit cardiaque et le débit pulmonaire effectif ont la même valeur.
Le shunt de gauche à droite (G=>D) est égal à DPT - DPE.
Dans un shunt droit-gauche exclusif, le sang artériel pulmonaire a la même saturation que le sang veineux mêlé.
Le débit pulmonaire est égal au débit pulmonaire effectif.
Le shunt de droite à gauche (D => G) est égal à la différence DST-DP.
Dans les courts-circuits bidirectionnels ou croisés, le shunt de gauche à droite (G => D) est égal au DPT moins le DPE ; le shunt de droite à gauche (D=>G), au DST moins le DPE.
L’importance des shunts peut être appréciée en établissant le rapport entre les débits pulmonaire et systémique totaux.
Ce rapport est égal au quotient des différences artérioveineuses systémique et pulmonaire :
DPT/DST = (CaO2 - CvßmO2) / (CvpO2 - CAPO2) = DAVS/DAVP
En revanche, il est impossible d’apprécier le volume d’un shunt en prenant comme base le seul enrichissement en O2, que ce soit en volumes ou en pourcentage.
6- Impédance artérielle :
Elle représente la somme des forces qui s’opposent à la progression pulsée du sang dans les artères et qui dépendent des résistances du système vasculaire et de la viscosité, de la pesanteur et de l’ inertie du sang.
Dans le système cardiovasculaire, les résistances systémiques et pulmonaires, R, sont généralement définies, par analogie avec la loi d’Ohm, comme la relation de la différence des pressions existant de part et d’autre du circuit, P1 - P2, ou perte de charge, sur le débit Qqui le traverse : R = (P1 - P2)/Q.
Or, d’après la loi de Poiseuille-Hagen, dans le cas d’un écoulement laminaire, le débitQ qui traverse un tuyau cylindrique est une fonction directe de la différence des pressions P1 - P2, existant de part et d’autre du circuit, et du rayon r du conduit, et une fonction inverse de la viscosité í du fluide et de la longueur L du tube.
Mais en fait, la loi de Poiseuille-Hagen ne peut être appliquée sans discussion au système circulatoire dont le débit est, à la sortie des ventricules, pulsé, et dont les vaisseaux ont un rayon variable.
En présence d’un courant alternatif, la résistance est l’impédance Z, rapport variable existant à chaque instant entre la pression et le débit en un point donné de l’arbre artériel.
Dans le système cardiovasculaire, l’impédance est assimilable à celle d’un circuit électrique qui comporterait :
– une résistance ohmique, ou résistance proprement dite ;
– une bobine, qui donnerait lieu à une réactance inductive, inductance ou inertance ; celle-ci résulterait surtout chez l’homme de l’inertie de la masse sanguine ;
– un condensateur, qui agirait comme une réactance capacitive ou capacitance ; dans le système cardiovasculaire, celle-ci serait la conséquence de la compliance artérielle.
Les résistances artérielles sont généralement calculées comme le rapport des pressions sur le débit.
Les résistances artériolaires systémiques ou périphériques (RAS) sont égales au quotient de la différence des pressions moyennes aortique ou artérielle systémique (PAom ou PAm) et auriculaire droite (PADm ou PODm), par le débit cardiaque Q en L/min, soit : RAS = (PAom- PODm)/Q.
Les résistances artérielles systémiques totales (RAST) sont le quotient de la PAm sur le débit.
Les résistances artériolaires pulmonaires (RAP) sont calculées en divisant la différence des pressions moyennes artérielle pulmonaire (PAPm) et auriculaire gauche (PAGm ou POGm) ou capillaire (PCap), par le débit cardiaqueQ en L/min, soit : RAP = (PAPm-PCap)/Q.
Les résistances artérielles pulmonaires totales (RAPT) sont le quotient de la PAPm sur le débit. Les résistances postcapillaires ou « capillaires » pulmonaires sont égales au rapport de la pression capillaire pulmonaire sur le débit.
Les résistances peuvent être exprimées en unités conventionnelles, Wood (UW) ou Aperia, quotient des pressions en mmHg sur le débit en L/min ; en dyn·s·cm-5 dans le système CGS (centimètre, gramme, seconde) ; en N·s·m-2 dans le système MKSA (mètre, kilogramme, seconde, ampère) et en Pa·min·m-5 dans le système international (SI) actuel.
La pression est l’action d’une force sur une surface. Le débit est un volume écoulé par unité de temps.
Dans le système CGS, la pression s’exprime en dyn·cm-2 et les débits, en cm3·s-1.
La dyne (symbole dyn) est la force qui, appliquée à une masse de 1 g, lui imprime une accélération de 1 cm/s dans chaque seconde.
En hémodynamique, les pressions sont mesurées en mmHg.
Pour passer de ces mmHg aux dynes, il faut multiplier la hauteur de la colonne de mercure, en cm, par le poids spécifique du mercure, 13,6 et par l’accélération de la gravité, 980 cm·s-2 ; c’est-à-dire :
P mmHg × 0,1 × 980 × 13,6 = P mmHg × 1 333 =Adyn·cm-2.
Dans le système CGS, les résistances sont calculées en prenant la pression en dyn·cm-2 et les débits en cm3·s-1 :
R = (P mmHg X 1 333) / (1 000QL·min-1/60) = (P mmHg × 80) /QL·min-1) = Adyn·s·cm-5.
Les résistances sont aujourd’hui fréquemment exprimées en unités Wood (W), comme le rapport des pressions en mmHg sur les débits en litre par minute : 1 UW= 80 dyn·s·cm-5
La résistance artérielle périphérique totale, R, représente la composante statique de la charge, tandis que la composante pulsatile est reflétée par la compliance artérielle totale estimée, C, et les indices de propagation et de réflexion de l’onde de pouls.
L’élasticité artérielle effective, Ea, quotient de la pression télésystolique ventriculaire gauche (PTSVG) par le volume systolique VS serait une mesure valide de la charge artérielle chez l’homme.
Systèmes radiologiques et angiocardiographie :
Le cathétérisme cardiaque et l’angiocardiographie exigent l’emploi d’un système de rayons X.
La visualisation du coeur et des sondes est nécessaire pour la manipulation des cathéters.
Le but de l’angiocardiographie est d’obtenir des images de qualité, suffisantes pour établir un diagnostic correct des cardiopathies, au cours de l’injection d’un produit radio-opaque dans les cavités ou les vaisseaux du coeur.
L’enregistrement des images peut se faire sur des pellicules de 35 × 35 cm (ou de 35 × 24 cm), à une cadence relativement basse, de zéro à huit clichés par seconde pendant un temps maximal de 15 à 30 secondes : c’est la sériographie ou angiocardiographie fixe, ou bien à une vitesse de six à 120 images par seconde, sur des films de 35 mm, ou sur tout autre support, bande magnétique ou disque : c’est la cinéangiocardiographie (de ciné, mouvement).
Les progrès considérables des systèmes radiologiques, de l’électronique, de l’informatique et de l’interprétation numérique des images, avec répétition en boucle des séquences, permettent de travailler aujourd’hui dans de très bonnes conditions, et même d’enregistrer le déroulement des examens en temps réel, sur un vidéodisque laser ineffaçable et de grande longévité (30 ans).
Dans tous les cas, il faut choisir la sonde, le point d’injection, l’incidence, la vitesse d’injection en mL·s-1 et le volume de produit de contraste.
L’injection d’un certain volume de liquide radio-opaque dans des conditions de pression et de débit bien déterminées nécessite un injecteur approprié.
La cinéangiocardiographie exige le concours de nombreuses compétences ainsi qu’un équipement complexe et cher qui comprend notamment les éléments suivants :
– un système radiologique comportant un générateur, un tube de rayons X et une unité de contrôle ;
– un système de radioscopie composé d’un amplificateur de brillance et d’un ensemble de télévisions en circuit fermé ;
– un système d’enregistrement des images, autorisant la révision et le traitement immédiat et rapide de celles-ci, afin d’effectuer des mesures et des calculs facilitant la prise d’une décision ; il doit être possible de fixer une image de référence sur un écran, pendant que l’on continue à travailler en scopie sur un autre écran ;
– un système de reproduction des images permettant une interprétation et discussion extemporanée des documents et leur communication ou transmission secondaire si nécessaire.
A - Système radiologique :
Le générateur transforme le courant alternatif du réseau urbain en un courant continu, et fournit au tube de rayons X à la fois le courant à bas voltage nécessaire pour chauffer le filament de l’électrode négative ou cathode, et les hauts voltages indispensables pour accélérer suffisamment les électrons.
Le tube de rayonsXcontient les électrodes indispensables pour produire les rayons X.
Ces électrodes sont dans une ampoule de verre sous vide qui est immergée dans l’huile.
Le tout est refroidi par de l’air.
Les rayons X résultent du bombardement de l’anode (électrode positive) par les électrons émis par la cathode.
Ces électrons frappent les électrons des couches internes des atomes de l’anode et les chassent de ses orbites.
Le passage d’un électron d’une orbite externe à une orbite interne s’accompagne de l’émission de rayons X.
Les électrons qui passent à côté du noyau atomique sont freinés et changent de direction en donnant lieu aussi à l’émission de rayons X.
Le rendement des tubes de rayons X est très faible : 99 % de l’énergie employée est perdue sous forme de chaleur et de lumière.
Les rayons X se déplacent à la vitesse de la lumière et ne sont pas déviés par les champs électriques ou magnétiques.
Ils impressionnent les plaques photographiques, excitent la fluorescence de certaines substances et ionisent les gaz.
Les rayons X sont invisibles et peuvent être considérés comme formés de particules d’énergie, photons X, ou comme des vibrations d’une toute petite longueur d’onde.
Les rayons les plus pénétrants sont ceux de plus petite longueur d’onde.
Pour les obtenir, il faut utiliser des électrodes de métaux de haute masse atomique et appliquer des tensions très élevées.
Le wolfram ou tungstène (symbole W, masse atomique 183,9) qui est un bon conducteur et a un point de fusion élevé (3 400 °C), est un des métaux les plus employés à ces fins.
L’unité de mesure de la dose émise de rayons X est le röntgen, symbole R, qui correspond à la quantité de radiation qui produit sur une certaine masse d’air une émission d’ions portant une unité électrostatique d’électricité de chaque signe.
Dans le tube à rayons X, la cathode est un filament fin de tungstène qui, chauffé, émet des électrons.
Ceux-ci sont accélérés par la différence de potentiel existant entre les électrodes, et dirigés vers une zone limitée de l’anode en wolfram qui constitue la cible.
L’anode est une couronne dans un élément en tronc de cône rotatoire.
La surface de la cible est inclinée et forme, avec le faisceau d’électrons, un angle de 7 à 12°.
Les rayons X produits par ce foyer de l’anode sont d’autant mieux délimités et les images mieux définies que cet angle est plus petit.
Mais si cet angle est inférieur à 7°, le nombre d’électrons absorbés par la cathode devient trop important.
La portion de l’anode qui émet des radiations X à chaque instant, ou foyer, est très réduite.
Les tubes de cinéangiocardiographie des salles d’exploration actuelles ont des foyers de l’ordre de 0,6 mm et donnent des décharges de rayons X qui durent 4 ms, en utilisant des différences de potentiel de 60 à 100 kV et des intensités de courant de 250 à 400 mA.
B - Amplificateur de brillance et télévision en circuit fermé :
L’amplificateur de brillance et la télévision en circuit fermé ont augmenté considérablement les possibilités diagnostiques des rayons X.
La combinaison d’un écran luminescent et d’une photocathode, d’antimoniure de césium ou d’arséniure de gallium, permet de transformer l’image lumineuse, due à l’incidence des rayons X, en une image électronique.
Les rayons X, après avoir traversé le patient, frappent une surface luminescente et donnent lieu à des photons, qui sont transformés par la photocathode en un flux d’électrons.
Les électrons issus d’un point sont concentrés par une électrode chargée d’un potentiel négatif en forme aussi de surface cylindrique, et accélérés par une deuxième électrode en forme de surface cylindrique, portée à un potentiel positif, disposée devant l’anode.
En réglant la tension de ces éléments, on obtient que tous les électrons émanant d’un point de la photocathode viennent toucher un même point dans l’anode.
Il suffit que celle-ci soit recouverte d’une substance luminescente pour que l’image de la photocathode puisse être observée sur cet écran secondaire.
L’ensemble agit comme un amplificateur de brillance.
Un photon X qui traverse un patient donne une information qui se traduit par une illumination fugitive de l’écran. Pour former une image, il faut de nombreuses instructions.
La pluie de signaux n’est pas homogène et si le nombre des photons est petit, leur répartition est irrégulière et donne lieu à une fluctuation de l’image.
Le gain de l’amplificateur est limité par le « bruit » qui se superpose au signal principal.
Si la fluctuation est importante et le facteur de conversion élevé, le « bruit » visible se manifeste comme un effet de nuage, appelé scintillation.
L’émission de lumière par l’amplificateur ne cesse pas immédiatement après l’arrêt des rayons X ; il existe toujours un certain délai entre les deux événements.
Ce phénomène, la « rémanence », est très gênant si les objets étudiés se meuvent vite. L’amplificateur de brillance doit avoir un bon pouvoir séparateur.
Celui-ci peut être mesuré à l’aide d’un objet-test formé de lames opaques séparées par une matière transparente.
Un bon amplificateur doit permettre de distinguer clairement les éléments d’une mire ayant de 20 à 25 paires de lignes noires et blanches par centimètre (une ligne noire et une blanche font une paire).
Dans les services de cathétérisme, il faut un amplificateur avec un gain élevé, une faible rémanence et un bon pouvoir séparateur.
L’intensificateur d’images et l’analyse numérique facilitent l’emploi de la télévision en circuit fermé, d’un magnétoscope et de la cinéangiocardiographie et permettent le contrôle automatique des constantes.
L’image fournie par l’amplificateur est ronde.
Il est nécessaire de faire un noircissement circulaire de l’écran de télévision.
Le signal peut être enregistré sur une bande magnétique ou un disque, et revu immédiatement.
Ceci diminue les risques, accroît la qualité des examens et permet de décider raisonnablement de la suite de l’exploration.
Le recours à un ordinateur autorise le traitement des images pour calculer le calibre des vaisseaux, les volumes cavitaires ou la masse de certaines structures.
C - Cinéangiocardiographie :
La cinéangiocardiographie consiste à enregistrer les images observées au cours de l’injection d’un produit radio-opaque dans les cavités ou les vaisseaux du coeur, sur un film ou sur tout autre support, à la vitesse de 6 à 50 poses ou images/seconde.
Tous les paramètres d’exposition, de traitement et de lecture doivent être contrôlés de façon à obtenir une bonne iconographie et un diagnostic correct.
La quantité de lumière émise par l’écran secondaire de l’amplificateur de brillance est proportionnelle à la quantité de radiations X qui traverse le patient.
Celle-ci dépend de la nature même des rayons X.
En effet, dans la radiation d’un tube à rayons X, le nombre de photons X par unité de temps est déterminé par l’intensité du courant (mA) et par la différence de potentiel (kV) appliquées dans le tube.
L’énergie de ces photons, c’est-à-dire, le pouvoir de « pénétration » ou « dureté » des rayons X, est conditionnée par les kV.
Les rayons X « durs » sont mal absorbés, ils traversent facilement le patient.
Si le voltage des rayons X est très élevé, l’écran est trop « blanc », les artères coronaires se confondent avec les structures voisines.
Si le voltage est trop bas, les rayons X sont « mous », ne passent pas à travers le patient, l’écran est noir.
Il faut obtenir le meilleur rendement possible par rapport à l’épaisseur du malade, aux organes traversés et au produit radio-opaque, pour aboutir à une bonne image radiologique.
1- Contrôle automatique des constantes radiologiques :
La constance de l’émission des rayons X et de la luminosité de l’écran secondaire est assurée par un contrôle automatique des kilovolts.
La lumière issue d’une zone centrale de l’amplificateur de brillance, d’à peu près la moitié de sa surface, excite une photocathode qui envoie le courant ainsi produit à un comparateur.
Celui-ci reçoit aussi un signal de référence choisi préalablement.
Le comparateur commande le nombre de kV en fonction de la différence des deux courants.
Le noircissement ou la luminosité des images peuvent être modifiés manuellement.
2- Imagerie et lecture des images :
La qualité des images dépend aussi des systèmes de reproduction, écrans et supports.
Dans le cas des films, leurs caractéristiques doivent être bien connues et les conditions de développement parfaitement réglées, afin d’en tirer les meilleurs résultats. Le pouvoir de résolution ou séparateur d’un système de reproduction d’images dépend de la finesse et du nombre de points noirs et blancs qu’il utilise.
Le contraste est la différence de luminosité des parties de l’image ; il est d’autant plus bas que l’écart est petit.
Il faut pouvoir le modifier afin de définir correctement les structures que l’on veut analyser.
Les documents obtenus doivent être lus avec un système convenable qui permette le déroulement image par image, l’arrêt, la marche en avant et en arrière.
Il faut souligner que la qualité des images ne dépend pas seulement des constantes radiologiques et des conditions d’acquisition mais aussi des éléments de lecture et de la luminosité ambiante.
La plupart des systèmes radiologiques comportent aujourd’hui :
– un générateur de rayons X à potentiel constant ;
– un « statif » ou dispositif en parallélogramme, équilibré et isocentré avec, sur l’extrémité inférieure, un tube radiogène à trois foyers, à charge thermique élevée et à scopie pulsée, permettant de choisir trois champs de 23, 16 ou 11 cm, et pourvu de collimateurs, d’un filtre semi-circulaire, semi-transparent, et, sur l’extrémité supérieure, d’un système d’amplification et d’acquisition des images en mode numérique, qui peut être rapproché ou éloigné du tube, en modifiant ainsi la distance à la source.
Ce « statif » peut être mû pour obtenir les différentes incidences, rotations, obliques antérieures, droite ou gauche ± 90° ou angulations crâniale ou caudale ± 55° ;
– une table d’exploration confortable, disposant des éléments de contrôle nécessaires et pouvant être déplacée dans le sens longitudinal (vers la tête ou les pieds), tournée autour d’un axe vertical (vers la droite ou la gauche) et montée ou descendue de façon à faire coïncider le centre de masse du ventricule gauche avec le point d’intersection des deux lignes imaginaires verticale et transversale (dessinées par le faisceau de rayons X qui va du tube au centre de l’amplificateur avec le « statif » ou parallélogramme en position verticale et horizontale), avec la ligne imaginaire horizontale qui représente l’axe longitudinal de rotation du « statif » ; l’ensemble permettant un abord fémoral ou brachial droit ou gauche du patient ;
– un système de visualisation, de traitement et d’enregistrement des images permettant leur affichage et leur traitement au cours de l’exploration-intervention, l’analyse de la fonction ventriculaire gauche ou droite, la quantification des sténoses coronaires, la modification du contraste, l’amplification et le déplacement des images et le renforcement des contours.
3- Irradiation radiologique :
L’irradiation radiologique est un problème important en ce qui concerne le personnel travaillant dans les salles de cardiologie interventionnelle.
Comme toutes les radiations ionisantes, les rayons X ont des effets biologiques dont certains sont inéluctables, liés à la nature même de ces rayons et qui apparaissent à partir d’un seuil de dose, spécifique de l’organe, et dont la gravité augmente avec celle-ci : ces effets concernent surtout la peau, la thyroïde (hypothyroïdie) et le cristallin (cataracte).
Et d’autres sont aléatoires, stochastiques ou conjecturaux (leucémies, cancers, anomalies génétiques...) mais la gravité est indépendante de la dose, même si leur nombre s’accroît avec elle.
La dose absorbée se mesure aujourd’hui en grays, symbole Gy, qui est la quantité de rayonnement ionisant qui communique à 1 kg de matière une énergie de 1 joule.
La dose absorbée est difficile à mesurer (par calorimétrie ou dosimétrie chimique).
Elle est estimée généralement par calcul, en fonction de la nature de la radiation (il existe un facteur multiplicateur de 1 pour les rayons X) et du tissu ou organe exposé (1 pour les muscles, 4 pour les os, 5 pour le cristallin).
La dose absorbée s’exprime aussi souvent en sieverts, Sv.
La dose biologiquement efficace s’exprime en rem.
Le rem est la dose de radiation qui donnerait lieu sur un tissu biologique à un effet équivalent à celui produit par un röntgen, R, de rayons X.
Le rem permet de comparer les diverses radiations et de calculer les doses totales. Pour les rayons X, 1 R = 0,01 Gy = 10 mSv = 1 rem.
Il est recommandé (Commision internationale de protection radiologique, ICRP) de ne pas dépasser, par an et pour l’organisme entier, la dose de 50 mSv, soit 0,05 Gy, soit 5 rem, en ce qui concerne les effets stochastiques et 150 mSv au niveau des yeux.
Par trimestre, 30 mSv, soit 0,03 Gy, soit 3 rem ; pour les femmes en état de procréer, 13 mSv, soit 0,013 Gy, soit 1,3 rem ; pour les femmes enceintes, 3 mSv.
La limite de dose par semaine serait 1 mSv, soit 0,001 Gy, soit 0,1 rem.
La dose reçue par l’opérateur au niveau du cou serait de 5 mSv pour 100 explorations, et celle reçue par le personnel beaucoup plus basse.
Il faut donc porter un dosimètre et se protéger au maximum :
– en réduisant au minimum nécessaire le temps d’exposition ;
– en faisant appel à des systèmes de protection, lunettes adéquates, cache-thyroïde, tabliers appropriés, écrans protecteurs ;
– en accroissant autant que possible la distance de l’opérateur au malade, en rapprochant au maximum l’amplificateur du patient, et en recourant aux diaphragmes ;
– en faisant contrôler périodiquement le fonctionnement du système radiologique.
4- Sondes pour angiocardiographie :
Les sondes destinées à l’injection d’un volume important de produit de contraste en un temps très court doivent résister aux pressions nécessaires, sans éclater et rester en place, relativement immobiles, pendant l’injection.
Cela n’est possible qu’avec des sondes ayant des trous latéraux à leur extrémité distale.
Les angiocardiographies sélectives auriculaires et ventriculaires droites et gauches et artérielles pulmonaires ou aortiques, sont habituellement réalisées aujourd’hui avec des sondes en « queue de cochon », 5 F, 6 F ou 7 F.
Pour l’opacification des artères pulmonaires ou de l’aorte, il vaut mieux se servir de sondes de calibre 6 F ou 7 F, qui autorisent des débits suffisants (20 à 30 mL/s).
5- Vitesse et volume d’injection, lieu d’injection et incidence des rayons X :
Pour obtenir une opacification sélective des cavités cardiaques ou des vaisseaux du coeur qui soit suffisante pour analyser certaines structures ainsi que des phénomènes donnés, et pour établir le diagnostic d’une cardiopathie, il faut délivrer un certain volume de produit radio-opaque en un temps limité.
Cela n’est possible qu’avec un injecteur approprié, qui permet de choisir la vitesse d’injection, en mL/s, et le volume total.
Ces machines développent la pression nécessaire pour assurer le débit voulu ; elles permettent de fixer un délai de montée de la pression, qui favorise la stabilité de la sonde et une pression maximale à ne pas dépasser.
L’injection s’arrête si la pression excède la limite choisie. La pression de rupture des cathéters est en général supérieure à 1 000 PSI (70 kg/cm²).
Cette pression n’est pas délivrée à l’extrémité distale de la sonde, mais à la partie proximale.
Si le cathéter se casse, il le fait à la jonction de la sonde avec l’embout proximal, là où se trouve le point de moindre résistance.
Les débits que l’on peut obtenir avec les différentes sondes sont très variables.
Il faut retenir actuellement que les cathéters 5 F permettent des débits maximaux autour de 12 mL/s, les 6 F autour de 20 mL/s, et les 7 F, 30 mL/s.
Le lieu de l’injection du produit de contraste et l’incidence des rayons X sont choisis en fonction de la cardiopathie et du diagnostic recherché.
Pour l’étude des sténoses, il faut obtenir l’opacification de la cavité située en amont ; pour l’analyse des régurgitations, l’injection doit être effectuée dans la cavité d’où celle-ci provient.
La position du cathéter va dépendre aussi du type de la sonde.
L’analyse des anomalies, propres à une cavité ou un vaisseau, est généralement plus facile si l’injection du produit de contraste est effectuée dans la cavité ou le vaisseau intéressés.
Mais une injection en amont s’accompagne naturellement de l’opacification des structures situées en aval et peut permettre dans certains cas d’étudier celles-ci convenablement.
Sur le parallélogramme ou l’arcus, les rotations de l’élément supérieur du système radiologique, qui est l’amplificateur, à partir de sa position de repos tout en haut, qui correspond au « zéro », vers la droite du malade, antihoraires par rapport à l’opérateur, (situé à la droite et vers les pieds du patient), sont appelées obliques antérieures droites (OAD) et notées en degrés négatifs ; celles vers la gauche, horaires, obliques antérieurs gauches (OAG) et notées en degrés positifs ; celles vers la tête, crâniales (Cr), antihoraires, sont notées en degrés négatifs, et celles vers les pieds, caudales (Ca), horaires, en degrés positifs.
L’anatomie particulière du coeur fait que certaines incidences sont plus adéquates que d’autres pour l’étude d’une structure donnée.
Sur un coeur en situation normale, sans inversion ventriculaire ni transposition des vaisseaux, la valve tricuspide est bien vue en projection OAD -15° ou -45°.
La chambre de chasse du ventricule droit, en transverse, latérale ou de profil, ou en OAD -45°. L’AP droite, de face ; la gauche, en discrète OAG.
La valve mitrale, les oreillettes et les ventricules droit et gauche, en OAD-45°.
Les incidences axiales, hépatoclaviculaires (ou quatre chambres) et les vues selon le grand axe du coeur, proposées par Bargeron, Elliott et al sont très intéressantes pour l’analyse de certaines structures.
Dans les services de cardiologie d’adultes, les cas de patients ayant une cardiopathie congénitale, une malformation cardiaque ou une tumeur sont devenus exceptionnels.
Le diagnostic est généralement porté sur ces malades beaucoup plus tôt et habituellement par des méthodes peu invasives, échocardiographie, doppler ou autre.
L’analyse du comportement systolique de la valve tricuspide exige d’injecter le produit radio-opaque à la partie moyenne ou apicale du ventricule droit.
La boucle de la sonde en « queue de cochon » doit être située à la pointe, pour éviter à la fois une opacification sélective de la chambre de chasse et que les trous proximaux de la sonde soient au niveau de l’orifice valvulaire.
Le volume de l’injection, de 15 à 20 mL/s pendant 2,5 à 3 secondes.
La chambre de chasse du ventricule droit et la valve pulmonaire sont généralement bien vues aussi dans cette incidence.
L’angiocardiographie sélective artérielle pulmonaire est réalisée essentiellement pour étudier :
– l’arbre vasculaire pulmonaire, dans les cas de rétrécissement pulmonaire, d’HTAP ou d’embolie pulmonaire ;
– les veines pulmonaires, surtout dans les cas de retour veineux pulmonaire anormal ;
– l’oreillette gauche ;
– la valve mitrale.
Les opacifications pulmonaires peuvent être effectuées en cinéangiocardiographie sur le champ de 23 cm, à la cadence de 25 images par seconde, après injection sélective dans les artères pulmonaires droite et gauche de 15 à 30 mL/s en 1 ou 2 secondes.
Dans le cas de retour veineux pulmonaire anormal isolé, il faut injecter le produit de contraste dans l’AP du poumon intéressé, de 20 à 30 mL/s en 1 seconde. Pour confirmer l’existence d’une communication interauriculaire, avec un shunt de gauche à droite, il faut injecter le produit de contraste dans l’AP, de 20 à 30 mL/s pendant 2 secondes, ou dans l’oreillette gauche de 15 à 20 mL/s pendant 3 secondes, en incidence hépatoclaviculaire, OAG+30° à +45° Cr -45°.
L’oreillette gauche (OG) et la valvule mitrale (VM) sont visibles au cours de l’opacification du coeur droit, oreillette ou ventricule droits ou AP.
L’incidence idéale, en ce qui concerne ces deux structures (OG et VM), est l’OAD -30° -45°.
Mais s’il existe un myxome, un thrombus ou une anomalie auriculaire gauche, il faut aussi une OAG +30° à +45° Cr -45° (« hépatoclaviculaire »).
La valvule mitrale et le ventricule gauche sont parfaitement visibles en OAD -30° -45°.
Nous effectuons généralement les angiocardiographies sélectives ventriculaires gauches avec une sonde « queue de cochon » 5 F ou 6 F, de12 à 17 mL/s pendant 2,5 à 3 secondes.
Dans le cas de prolapsus valvulaire mitral, d’anévrisme ventriculaire, de rétrécissement aortique valvulaire ou sous-valvulaire ou de cardiomyopathie hypertrophique obstructive, il faut de plus effectuer une opacification en OAG+50° +75° Cr -20° (OAG « long axe »). Dans les communications interventriculaires, les projections idéales sont l’OAG +50° +75° Cr -20° (« long axe ») et l’hépatoclaviculaire (OAG +30° +45° Cr -45°).
La « queue de cochon » doit se trouver près de la pointe (afin d’obtenir une opacification satisfaisante de toute la cavité).
Si la sonde est sous-aortique, l’opacification ventriculaire est souvent incomplète.
6- Substances de contraste :
De nombreuses substances ont été utilisées dans le passé pour opacifier les cavités et les vaisseaux du coeur.
Ces substances doivent être bien tolérées, stables, solubles dans l’eau et non toxiques.
Les produits de contraste radiologiques employés aujourd’hui sont surtout des composés « non ioniques, peu visqueux et d’osmolalité faible, relativement bien tolérés par l’organisme, monomères triiodés, obtenus par amidation de la fonction acide, tels l’iopamidol (Iopamiron) et l’iohexol (Omnipaque) qui contiennent autour de 300-350 g d’iode par litre et dont l’osmolalité se situe autour de 800 mOsm/kg.
L’iode, dont la masse atomique est très élevée (126, 9) apparaît comme un élément radio-opaque idéal.
L’osmolalité est une conséquence du nombre de particules osmotiquement actives (POA) par kg de solvant à une température donnée.
La pression osmotique totale du plasma est d’environ 300 mOsm/kg H2O à 37 °C.
La viscosité d’une solution est la résistance qu’elle oppose à un écoulement uniforme.
Elle est due aux frottements internes.
Les effets adverses des produits de contraste sont à la fois locaux et généraux.
Les réactions locales, sur la genèse desquelles nous sommes encore aujourd’hui incertains, résulteraient surtout de l’hyperosmolarité et de la composition chimique des substances utilisées.
Ces réactions sont maximales à l’endroit même ou à proximité du lieu d’injection.
L’angiocardiographie veineuse ou sélective ou auriculaire, ventriculaire, artérielle pulmonaire ou aortique, est généralement bien supportée ; elle s’accompagne d’une sensation de chaleur qui progresse comme une vague, du coeur vers les extrémités et qui entraîne une céphalée et une impression douloureuse fugace à la pointe des doigts et parfois même de l’anus.
Ces sensations sont brèves, elles ne durent habituellement que quelques secondes.
Il faut en avertir le patient avant d’effectuer l’injection.
Si la céphalée est violente, elle peut être apaisée en posant sur le front un champ humecté avec de l’eau froide. Le patient peut ressentir aussi des nausées et même vomir.
Il faut dans ces cas recommander au malade de respirer calmement, de tousser un peu et d’attendre. L’injection du produit de contraste dans le ventricule droit ou l’AP peut déclencher des quintes de toux.
L’angiocardiographie veineuse ou sélective droite, auriculaire, ventriculaire ou artérielle pulmonaire, s’accompagne d’un accroissement des pressions droites.
L’injection du produit radio-opaque dans les ventricules donne souvent lieu à des extrasystoles.
L’opacification du ventricule gauche entraîne généralement une diminution de la pression systolique ventriculaire et artérielle, à cause de l’effet dépresseur du produit de contraste sur le myocarde et de la vasodilatation périphérique.
La pression télédiastolique ventriculaire gauche, capillaire pulmonaire et artérielle pulmonaire s’accroissent.
Le produit de contraste représente une surcharge volumique qui est fonction de la vitesse de l’injection, de la quantité injectée et de l’hyperosmolalité du liquide employé.
L’hématocrite décroît initialement pour revenir vers les valeurs de départ dès la dixième minute.
La fréquence cardiaque augmente.
Le débit cardiaque s’accroît généralement pour atteindre un maximum vers la deuxième minute de l’angiocardiographie, puis descend discrètement au-dessous des valeurs de contrôle, pour revenir à la situation initiale après 15 à 20 minutes.
Les volumes ventriculaires ne seraient pas modifiés pendant les trois à quatre premières systoles.
L’effet du produit radio-opaque est aussi fonction des conditions hémodynamiques préexistantes.
Le gradient « capillaire pulmonaire » ventricule gauche s’accentue considérablement dans les cardiopathies mitrales.
Chez les malades ayant une atteinte sévère de la fonction cardiaque, l’angiocardiographie sélective peut donner lieu à une inefficacité cardiaque avec choc, ou à un oedème aigu du poumon grave.
Les réactions générales aux substances radio-opaques résulteraient de phénomènes « allergoïdes » de nature pseudoanaphylactique, de la libération de certains médiateurs, comme l’histamine et des kinines, d’une fibrinolyse, de l’activation du complément et de phénomènes de coagulation intravasculaire encore mal connus.
Le traitement anticoagulant par l’héparine, les antihistaminiques et les stéroïdes préviendraient ou amenuiseraient ces réactions.
Le traitement par bêtabloquants non sélectifs favoriserait la survenue d’un bronchospasme chez les sujets susceptibles (asthmatiques).
Les réactions du type « anaphylactoïde » incluent des événements mineurs, tels qu’éternuements, réactions papuleuses localisées, angio-oedème, urticaire ou érythème généralisé, ou des faits plus graves tels qu’un bronchospasme, un oedème de la glotte ou un collapsus cardiovasculaire pouvant être létaux.
La chute de la tension artérielle au cours d’une exploration angiocardiographique peut être d’origine vagale (elle s’accompagne alors généralement de sueurs, de bradycardie, sauf en cas de traitement par des bêtabloquants non sélectifs, et de bâillements), d’origine « toxique », par action inotrope négative et vasodilatation périphérique, ou de nature ischémique ou anaphylactoïde.
Dans ces cas, il faut remplir le patient avec du Plasmiont ou du Plasmagelt désodé, administrer de l’oxygène et de l’atropine et si nécessaire de l’adrénaline, 0,1 à 0,2 mg IV et des vasopresseurs, Dobutrex, de 2 à 10 lg/kg/min selon les besoins.
Chez les sujets prédisposés, allergiques à d’autres agents, ou ayant déjà eu des réactions défavorables aux produits de contraste au cours d’examens précédents, un traitement prophylactique est justifié.
Celui-ci, réparti sur les 24 à 48 h qui précèdent l’exploration, comporte généralement des corticoïdes, des antihistaminiques H1, et des sédatifs.
Et juste avant l’intervention, injecter en IV des corticoïdes et 0,5 mg d’atropine.
En cas de réaction allergique, administrer un traitement adéquat. Les substances radio-opaques employées en cardiologie ont deux points d’impact supplémentaires qu’il faut garder en mémoire : le cerveau et les reins.
Si la barrière sanguine cérébrale est intacte et si la concentration du produit de contraste (P de C) dans les vaisseaux du cou est peu importante, comme c’est le cas au cours des explorations effectuées dans les services de cardiologie, les risques d’accidents nerveux sont infimes et négligeables.
Il faut éviter à tout prix l’injection sélective des artères de la moelle épinière.
La néphrotoxicité des P de C est très discutée.
Les risques d’anurie sont mineurs ; celle-ci serait plus fréquente chez les patients âgés, déshydratés, ou ayant une insuffisance cardiaque, un diabète, une hypertension artérielle ou une insuffisance rénale préalable avec une urée élevée supérieure à 0,3 g/L soit 3 à 7 mmol/L, une créatininémie supérieure à 12 mg/L (120 mmol/L) et une clairance de la créatinine inférieure à 20 mL/min.
L’anurie, généralement régressive, peut parfois exiger une dialyse.
Il faut chez certains patients limiter la quantité d’iode injectée et favoriser l’hydratation en permettant l’absorption précoce de liquides après l’exploration.
7- Calcul du volume des cavités cardiaques :
Les progrès des moyens d’exploration et le traitement par ordinateurs des données recueillies au cours de l’opacification du coeur rendent actuellement possible l’estimation rapide des volumes auriculaires et ventriculaires, droits et gauches, les volumes télédiastolique, télésystolique et d’expulsion ventriculaires gauches, la fraction d’éjection, le volume et la fraction de régurgitation systolique (en cas d’insuffisance mitrale) ou diastolique (en cas d’insuffisance aortique) ainsi que la cinétique ventriculaire gauche.
Il ne faut cependant pas oublier que le calcul des volumes des cavités cardiaques est entaché d’un certain nombre d’incertitudes.
Il repose sur des hypothèses approximatives qui concernent :
– la position du coeur par rapport au support de l’image et à la source de rayons X ;
– la forme supposée de la cavité, d’après laquelle est établie la formule de calcul ;
– l’emploi d’équations de correction empiriques ;
– la difficulté de définir les limites de l’ombre cardiaque ;
– le volume variable occupé dans les ventricules par les piliers et les « trabeculae carnae » ;
– le fait que ces mesures ne sont généralement pas effectuées que sur un seul cycle cardiaque.
Le calcul pose essentiellement deux problèmes : quel est le rapport qui existe entre les dimensions de l’image radiologique et celles de la cavité elle-même ?
Quelle est la formule qui permet d’estimer au mieux le volume considéré ?
8- Déformation radiologique :
La déformation de l’ombre cardiaque résulte du non-parallélisme des rayons X et de l’effet dit de « pelote à épingles ».
Dans un tube cathodique, les rayons subissent une dispersion électromagnétique, d’autant plus marquée qu’ils sont plus loin du centre du tube et proches des quatre coins de l’écran.
Cette distorsion est surtout importante à partir d’une distance du centre égale à 9/10es du rayon de l’image.
La déformation due au non-parallélisme des rayonsXdépend de la distance du film-support de l’image au tube « radiogène » et au plan du coeur.
Les premières formules ont été établies à partir des angiocardiographies fixes biplan face et profil.
Elles ont permis de vérifier le bien-fondé des hypothèses employées.
9- Facteur de correction ou d’agrandissement :
Cependant, dans la pratique, les angiocardiographies sont souvent effectuées dans un seul plan à la fois, à la cadence de 5 à 50 images par seconde.
Cela permet de suivre le cycle cardiaque et de choisir le moment qui correspond au phénomène à étudier.
Il est difficile d’appliquer à ce système les formules établies pour les angiocardiographies fixes biplan permettant de calculer le facteur d’agrandissement.
La déformation due aux rayons X est appréciée dans ces cas en filmant, dans les conditions de l’examen, un témoin (sphère ou grille de surface connue placée à la hauteur du plan qui contient le centre de la masse cardiaque, CMC).
Ce plan est généralement considéré comme se situant à mi-hauteur du diamètre antéropostérieur thoracique du patient.
L’emploi de l’arcus, arceau mobile qui porte à une extrémité la caméra et à l’autre le tube de rayons X, ou du parallélogramme, simplifie un peu le problème.
Le facteur de correction devient une « constante » si l’on place le centre de rotation du système sur le CMC avec l’arceau en position horizontale à une distance donnée.
Dans les systèmes actuels, le facteur de calibrage est intégré dans les algorithmes de calcul.
10- Formules de calcul du volume du ventricule gauche sur les angiocardiographies biplan :
* Méthodes de la surface-longueur de Dodge et al et des multitranches de Chapman et al :
La cavité du ventricule gauche est assimilée à un ellipsoïde de révolution, ou considérée comme résultant de la superposition d’une série de tranches de section elliptique.
Le volume du ventricule est calculé grâce à des formules représentatives en utilisant des angiocardiographies biplan, par la méthode de Dodge et al dite de la surface-longueur, ou des multitranches de Chapman et al.
La méthode de Dodge et al considère le ventricule comme un ellipsoïde de révolution dont le volume serait :
Vc = (4/3) × ∏ × (Dp/2) × (Df/2) × (L/2) × F3 L est le plus long des deux grands axes tirés de la base à la pointe du coeur de face et de profil.
Df et Dp sont les plus petits axes, ou axes transverses, calculés à partir des surfaces Sf et Sp et des grands axes Lf et Lp mesurés respectivement sur les angiocardiographies de face ou de profil.
En effet, dans une ellipse, la surface S est : S = ∏ × (L/2) × (D/2) d’où : (D/2) = 2 S/ ∏ L F3 est le facteur de correction au cube.
Le volume réel du ventricule,Vr, serait égal à 0,928 fois le volume calculé Vc moins 3,8 mL : Vr = 0,928 Vc - 3,8.
La méthode des multitranches de Chapman et al est basée sur une modification de la règle de Simpson.
Le coeur est assimilé à une série de tranches de 1 mm d’épaisseur (h = 0,1 cm) et de section elliptique de diamètre frontalAet antéropostérieur B.
Le volumeVde chaque tranche est :
V = (∏ × h ×A× B) / 4
et le volume de la cavité, Vc :
Vc = p (h/3) [∑ Ai B i + ∑ (1/2)A j B j]
ce qui devient
Vc = p (h’/3) [∑ Ai B i + ∑ (1/2) Aj B j]
une fois chaque dimension multipliée par le facteur de correction F avec i = 1, 3, 5,... sections impaires, et j = 2, 4, 6,... sections paires.
Cette méthode est parfaite pour l’étude des ventricules irréguliers, myocardiopathies hypertrophiques obstructives et anévrismes ventriculaires.
Les tranches situées au même niveau sur l’axe principal de l’angiocardiographie de face et de profil sont supposées être les mêmes.
La surface elliptique de chaque section peut être obtenue plus exactement en considérant le diamètre majeur (A ou B) comme le grand axe et en calculant le petit axe en fonction du grand et de l’angle compris entre les deux.
* Calcul du volume du ventricule gauche sur les angiocardiographies monoplan :
Le calcul du volume du ventricule gauche est aussi possible à partir des angiocardiographies monoplan.
En effet, les deux diamètres transverses du ventricule sont à peu près identiques, sauf dans le cas des cavités très irrégulières.
Dodge et Sandler trouvent que le diamètre antéropostérieur du ventricule gauche Dp, mesuré sur le film de profil, est en moyenne égal à 0,987 fois le diamètre transverse Df, mesuré sur le film frontal, plus 0,2 (Dp = 0,987 Df + 0,2).
Snow et al trouvent que le diamètre antéropostérieur du ventricule gauche en position oblique antérieure droite est égal à 0,85 fois le diamètre transverse. Dans les formules employées le plus souvent, les deux diamètres transverses sont considérés comme égaux.
Dans la méthode de la surface-longueur de Dodge et al sur les angiocardiographies de face ou en oblique antérieure droite, le volume ventriculaire Vc est calculé d’après l’équation :
Vc = (4/3) × ∏ × (L/2) × (D2/4) × F3 ;
L est le grand axe tracé de l’apex ventriculaire à la racine aortique, et passant par le centre du ventricule ; L coupe la surface du ventricule en deux moitiés.
D est le diamètre transverse, calculé à partir de la surface S du ventricule et du grand axe L : D/2 = 2S/∏L et D2/4 = 4S2 /∏2L2,
d’où Vc = 0,85 × (S2/L) × F3
D’après Dodge et al, le volume réel du ventricule gauche Vr est égal à 0,951 fois le volume calculé sur les cinéangiocardiographies effectuées de face -3 : Vr = 0,951 Vc - 3 ; Kennedy et al trouvent de bonnes corrélations entre le volume du ventricule gauche calculé sur les angiocardiographies de face ou en oblique antérieure droite et les volumes réels obtenus d’après des angiocardiographies biplan : de face, le volume réel du ventricule gauche Vr est égal au volume calculé Vc plus 9,6 et en oblique antérieure droite, l’incidence des rayons X faisant un angle de 28° avec la verticale sur un sujet couché à plat sur le dos : Vr = 0,81 Vc + 1,9.
La méthode des multitranches, de Chapman et al, peut aussi être appliquée aux angiocardiographies monoplans.
Le volume ventriculaire V est égal à : V = (∏h’/3) × [∑ A’i 2 + ∑ (1/2) A’j 2]
Le ventricule est coupé en tranches d’épaisseur égale dont les diamètres A, exprimés en centimètres, sont numérotés.
Ai sont les diamètres impairs, Aj les diamètres pairs.
Cherrier et al coupent le ventricule perpendiculairement au grand axe en 20 sections tronconiques ou trapézoïdales. Le volume ventriculaire V est égal à : V = F3 × (∏/3) × (L/20) × ∑ (R2 i + R2 j + RiRj) où i vaut de 1 à 19 (1, 3, 5,...), j, i + 1 et Ri et Rj sont les rayons de chaque tranche i et j.
Les volumes du ventricule gauche calculés ainsi sont en général surestimés.
Aux causes d’erreurs déjà citées s’ajoutent : d’une part, les difficultés de définir avec précision le contour de la cavité, particulièrement en systole (il est habituel d’inclure dans l’ombre du ventricule des régions même peu opacifiées) et, d’autre part, l’impossibilité de connaître le volume occupé dans le ventricule par les piliers et les trabécules musculaires (volume relativement important, surtout en systole et dans les petits coeurs).
Cependant, l’étude des corrélations démontre la fiabilité de la méthode.
* Volumes auriculaires :
Les volumes des oreillettes, gauche ou droite, peuvent être calculés aussi sur les angiocardiographies biplan, en assimilant ces cavités à des ellipsoïdes de révolution, par la méthode de la surface-longueur ou en appliquant la règle de Simpson.
* Volume du ventricule droit :
Le calcul du volume du ventricule droit n’est raisonnable que sur des angiocardiographies biplan.
Seul Graham a décrit une méthode, dite des deux chambres, permettant d’estimer le volume du ventricule droit sur l’angiocardiographie de profil.
La méthode de la surfacelongueur modifiée et la règle de Simpson sont aussi applicables au ventricule droit.
Celui-ci est assimilé, par certains auteurs, tantôt à un parallélépipède, tantôt à un prisme ou à une pyramide à base triangulaire.
* Volumes télédiastolique et télésystolique, fraction d’éjection et de régurgitation et vitesse moyenne du raccourcissement circonférentiel du ventricule gauche :
Les volumes télédiastolique et télésystolique ventriculaires gauches (VTD et VTS) sont les volumes, en mL ou en mL/m² de surface corporelle (volumes indexés), de cette cavité dans la phase correspondante du cycle cardiaque.
Les VTD et VTS du ventricule gauche sont généralement calculés sur les angiocardiographies sélectives ventriculaires, en considérant l’ombre ventriculaire maximale, VTD, et minimale, VTS.
Les valeurs normales duVTD et du VTS du VG sont de 70 ± 20 et 25 ± 17 mL/m².
Le volume systolique (VS) est la différence VTD - VTS.
Le VS vaut normalement 45 ± 13 mL/m².
La fraction d’éjection est le rapport du VS sur le VTD.
Elle est normalement de 67 ± 8 %.
En présence d’une régurgitation (exemple : insuffisance mitrale ou aortique), le VS chassé par le ventricule est supérieur au volume systolique effectif (quotient du débit Q par la fréquence cardiaque f, VSE =QC/f).
Le rapport (VS - VSE)/VS est la fraction de régurgitation, FR.
La vitesse moyenne de raccourcissement circonférentiel du ventricule gauche, ou VCF, s’exprime habituellement en circonférences par seconde (en prenant comme unité la circonférence télédiastolique du VG) :
VCF = (∏DTD - ∏DTS)/TE × ∏DTD = (DTD - DTS)/TE × DTD
avec DTD et DTS : diamètres ventriculaires télédiastolique et télésystolique et TE : temps d’éjection ventriculaire en seconde.
Le calcul des volumes ventriculaires, télédiastolique ou télésystolique et de la fraction d’éjection, peut être aussi effectué grâce aux courbes de dilution, vert d’indocyamine ou froid dans l’absence de régurgitation.
11- Analyse de la cinétique du ventricule gauche sur les angiocardiographies sélectives :
La fonction ventriculaire gauche est généralement analysée à partir des valeurs de la pression télédiastolique et des données tirées des angiocardiographies sélectives ventriculaires (PTDVG et ACGSVG).
Les angiocardiographies sélectives ventriculaires gauches (ACGSVG) sont généralement effectuées en OAD 30° et en OAG 60°.
Ces deux incidences permettent de calculer les volumes ventriculaires gauches télédiastolique et télésystolique indexés (VTDVGi et VTSVGi) et la fraction d’éjection (FE), d’affirmer la présence ou l’absence d’une insuffisance mitrale et d’analyser la cinétique ventriculaire.
Le VTDVGi est, dans les cardiopathies, normal ou élevé, et la FE, normale ou abaissée.
Il existe une corrélation négative entre la FE et leVTDVGi : la FE diminue à mesure que le VTDVGi augmente.
La FE, malgré son peu de valeur théorique en tant que paramètre de contractilité et de fonction ventriculaire, a une certaine valeur pronostique.
L’ischémie et la nécrose myocardique s’accompagnent souvent d’un trouble de la contraction ventriculaire, qui peut donner lieu à une réduction de la FE, et qui se traduit habituellement par une perturbation localisée de la cinétique ventriculaire : soit par une diminution (hypokinésie ou hyposynérèse) ou absence (akinésie ou asynérèse) de contraction ; soit par un mouvement paradoxal d’expansion de la paroi ventriculaire au cours de la systole, généralement reconnu sous la dénomination de dyskinésie ; soit par un asynchronisme, ou une altération du déroulement normal de la contraction ventriculaire, avec une perturbation initiale marquée de celle-ci, et une cinétique tardive normale ou quasi normale, tardokinésie, tout à fait caractéristiques.
L’ACGSVG en OAD permet d’évaluer assez correctement la cinétique VG.
Dans cette incidence, le bord antérosupérieur de l’ombre ventriculaire correspond à la paroi antérieure du VG, irriguée par l’artère interventriculaire antérieure (IVA), le bord postéro-inférieur à la paroi diaphragmatique de ce ventricule, irriguée par l’artère interventriculaire postérieure (IVP), et la pointe à l’apex ventriculaire, qui reçoit du sang d’une façon variable de l’IVA, de l’IVP et de l’artère circonflexe, Cx.
L’asynergie de ces territoires résulte de lésions significatives de ces artères. Les modifications de la contraction des territoires septal et postérolatéral du VG ne sont visibles qu’en OAG.
C’est sur cette paroi et dans cette incidence que se voient les asynergies dues à des lésions de la Cx, surtout de sa branche marginale, MG.
L’évaluation de la contraction VG est importante du point de vue diagnostique, pronostique et thérapeutique.
L’analyse subjective de cette cinétique est difficile et beaucoup trop imprécise.
L’analyse objective quantitative exige d’une part d’éviter les mouvements du coeur qui pourraient être dus au déplacement du malade ou du système radiologique, ou à la respiration ; pour ce faire, la table doit être maintenue fixe, le patient est prié de rester immobile, de gonfler la poitrine à fond et de retenir l’air dans les poumons le temps de l’opacification ; et d’autre part de tenir compte des mouvements de translation et de rotation du coeur qui accompagnent la contraction cardiaque.
L’idéal serait sans doute de suivre le parcours de chacun des points de la paroi ventriculaire tout au long de la systole.
Dans la pratique, on accepte généralement que la contraction du coeur est homogène et se fait autour d’un point central ou d’un axe de symétrie, l’axe de révolution de l’ellipsoïde ventriculaire.
De très nombreuses méthodes ont été proposées pour analyser la contraction cardiaque.
Certaines ignorent toute translation et rotation et font coïncider à chaque point diastolique un point similaire systolique : soit en divisant les contours supérieurs et inférieurs diastoliques et systoliques du VG, depuis les bords supérieur et inférieur de l’orifice aortique à la pointe, en 12 segments égaux, et en considérant le rapport de la distance existant entre chaque deux points diastolique et systolique correspondants des ombres ventriculaires à une valeur fixe (égale à la moitié du grand axe diastolique) ; soit (méthode de Stanford) en divisant le coeur grâce à dix rayons formant des angles de 36° ; ces rayons prennent comme axe de référence une ligne tirée sur le contour systolique, depuis le bord supérieur de l’orifice aortique à l’apex, et comme centre un point situé sur cet axe, à 69/100es de l’aorte.
D’autres cherchent à rassembler correctement les ombres systolique et diastolique du VG ; soit en superposant les centres géométriques ou de masse (CM) des deux contours, et en faisant alors tourner l’image systolique autour de ce centre, pour aligner les apex, soit en traçant deux axes, diastolique et systolique, depuis le point moyen de l’orifice aortique à la pointe, et en faisant alors tourner le contour systolique autour du point d’intersection des deux axes pour aligner les apex (méthode proposée par Virot et al).
Leighton et al dessinent un axe diastolique qui, partant de l’apex, divise l’ombre diastolique du VG en deux moitiés, et un axe systolique, qui va de l’apex au point d’intersection de la racine aortique avec l’axe diastolique ; ils font alors tourner le contour systolique autour de ce point, pour superposer les deux axes.
Les contours de l’ombre ventriculaire sont coupés par des rayons, ou par des diamètres perpendiculaires au grand axe aorte-apex.
Ces rayons ou diamètres sont, dans certaines méthodes, communs à la diastole et à la systole, dans d’autres, similaires mais indépendants.
Le raccourcissement de chacune de ces distances et la diminution des surfaces sont généralement exprimés comme un pourcentage par rapport aux paramètres diastoliques correspondants, axes, rayons, cordes ou surfaces : (PD - PS)/PD.
Il semble que l’estimation en fonction des surfaces soit meilleure.
Toutes les méthodes employées comportent une certaine proportion d’incertitude et d’erreurs ; Bardet et Fernandez divisent à l’aide de quatre lignes perpendiculaires le grand axe longitudinal télésystolique en cinq segments égaux.
Ils obtiennent ainsi neuf hémiaxes : quatre antérosupérieurs, quatre postéro-inférieurs et un apical, distance de la pointe au plus proche diamètre transversal. Le pourcentage de raccourcissement moyen normal des hémiaxes 1 à 7 est de 45 à 55 % ; celui des hémiaxes 8 et 9, autour de 30 et 23 %.
12- Diagnostic des cardiopathies sur les cinéangiocardiographies sélectives :
L’analyse des angiocardiographies sélectives permet non seulement l’étude de la cinétique et de la fonction ventriculaire, mais aussi le diagnostic des cardiopathies, malformations (communications interauriculaires ou interventriculaires, sténoses pulmonaires, valvulaire ou infundibulaire, maladie d’Ebstein ou autre), ou atteintes valvulaires (surtout régurgitations ventriculo-auriculaires, tricuspide ou mitrale, dans le cas des angiocardiographies ventriculaires, ou aortiques ou pulmonaires, dans le cas des angiocardiographies sus-sigmoïdiennes).
L’importance des régurgitations ventriculo-auriculaires ou artérioventriculaires peut être estimée :
– quantitativement, dans les cas des régurgitations isolées, en calculant le volume de régurgitation, VR, différence entre le volume total chassé par le ventricule (VST), égal au volume télédiastolique (VTD) moins le volume télésystolique (VTS) et le volume systolique antérograde effectif (égal au quotient du débit cardiaque, DC, sur la fréquence cardiaque, FC) ; la fraction de régurgitation, FR, est égale au rapport du volume de régurgitation sur le volume systolique total, FR : ((VST ou VTD - VTS) - VSE)/VST = VR/VST.
Le volume systolique total, VST, peut aussi être calculé à partir du volume systolique effectif, VSE, si l’on connaît la fraction de régurgitation, FR (exprimée généralement en pourcentage VST = VSE / (1 - FR) ;
– semi-quantitativement, en fonction du degré d’opacification des chambres situées en aval et en amont de la valve incompétente.
La régurgitation est dite légère (une croix), représentant moins de 20 % du flux transvalvulaire total, si l’opacification de la chambre d’amont se fait par bouffées systoliques, dans le cas des valves auriculoventriculaires, diastoliques dans le cas des valves sigmoïdes, avec opacification faible de cette chambre.
Modérée (deux croix), si l’opacification de la chambre d’amont est homogène, mais faible, de densité inférieure à celle de la chambre où a lieu l’injection ; la régurgitation représentant dans ce cas entre 20 et 40 %du flux total.
Et trois croix, régurgitation importante, si l’opacification des deux chambres est égale ; fraction de régurgitation entre 40 et 60 %.
13- Évaluation de la fonction cardiaque :
Le coeur doit assurer à toutes et à chacune des parties de l’organisme l’apport des substances dont elles ont besoin à chaque moment de leur existence, et l’élimination de leurs déchets, en respectant certaines normes.
De nombreuses conditions peuvent altérer ce travail.
Le système cardiovasculaire s’adapte de manière à compenser les défaillances.
Malheureusement, et à long terme, ces mécanismes de compensation contribuent souvent à aggraver la situation.
L’étude ou l’évaluation de la fonction cardiaque essaye de mettre au clair les causes de ces dérèglements, afin de les traiter le plus correctement possible.
L’évaluation de la fonction cardiaque exige d’apprécier :
– la qualité de la contraction (fonction pompe et fonction musculaire intrinsèque, ou contractilité) et la qualité de la relaxation ;
– le comportement diastolique passif du coeur. En effet, si l’on considère le coeur comme un muscle et une pompe, le cycle cardiaque comporte deux périodes :
– l’une active, qui comprend la contraction (contraction préisovolumétrique et isovolumétrique et une grande partie de l’éjection) et la relaxation (fin de l’éjection, relaxation préisovolumétrique et isovolumétrique et remplissage ventriculaire rapide), qui se font avec consommation d’énergie ;
– l’autre passive, la diastole, qui comprend le remplissage ventriculaire lent et le remplissage systolique auriculaire.
Cette définition diffère un peu des notions classiques, qui appliquent le terme de systole ventriculaire (du grec stole se raccourcir, sin ou sys, sur soi-même) à l’intervalle qui sépare du deuxième bruit le début de la montée de la pression ventriculaire, et celui de diastole (du grec dia, qui va vers ou qui mène à) à l’intervalle qui existe entre le deuxième bruit et le début de la systole suivante.
14- Évaluation de la fonction pompe :
L’estimation de la fonction pompe repose sur l’étude du débit cardiaque, Qou DC, et des conditions de travail du coeur (pressions et volumes télédiastoliques [PTDV et VTDV], télésystoliques [PTSV et VTSV] et systoliques [PS et VS], fraction d’éjection [FE] et travail ventriculaire, TV gauche ou droit), au repos et si nécessaire au cours d’une épreuve d’effort, de remplissage ou pharmacologique.
Le débit cardiaque par mètre carré de surface corporelle (DC/m²), ou index cardiaque (IC), vaut normalement 3,55 ± 0,75 L/min/m².
L’IC est égal au quotient de la consommation d’oxygène par minute et par mètre carré de surface corporelle VO2/m (143 ± 14 mL) par la différence artérioveineuse en oxygène (4,1 ± 0,06 mL/100 mL de sang).
Le débit cardiaque, même au repos, dépend de nombreuses variables et il est parfois difficile, face à une valeur donnée, de décider de sa normalité.
Le calcul du « pourcentage d’utilisation d’oxygène », rapport de la DAV sur le CaO2, permet d’apprécier facilement sa qualité.
Ce rapport est normalement inférieur à 26 %.
L’IC peut être considéré comme le résultat du produit du volume de sang expulsé à chaque systole par le ventricule, (ou volume systolique par mètre carré, ou indexé, VSI), par la fréquence cardiaque.
Le volume systolique (VS) dépend :
– de la précharge, souvent assimilée à la PTDVG, mais qui est en fait le « stress » ventriculaire, ou force de distension à laquelle est soumis le ventricule en télédiastole ;
– de la contractilité ;
– de la postcharge, ensemble des forces qui s’opposent à la vidange ventriculaire (résistances du système vasculaire, R [appréciées comme le rapport de la pression artérielle moyenne, PAm, sur le DC], et valeur de l’élastance artérielle effective, Ea [quotient de la pression télésystolique ventriculaire, PTSV, sur le volume d’éjection systolique, VS], qui est une mesure valide de la charge artérielle due à la distensibilité des vaisseaux et à la viscosité, pesanteur et inertie du sang).
La fraction d’éjection, FE, rapport de la différenceVTD moins VTS, sur le VTD, est un indice assez fidèle de la fonction ventriculaire.
La FE vaut normalement 67 ± 8 % ; de 56 à 83 %.
L’étude des points de fonction ventriculaire qui relient un indice de « performance », DC ou IC et un indice de remplissage, volume ou pression télédiastolique, au repos et au cours d’une épreuve d’effort, permet de se faire une idée sur la qualité de la fonction ventriculaire gauche.
Le débit augmente, la pression se modifie peu.
15- Évaluation de la contractilité :
La contractilité se caractérise par une certaine relation, indépendante du temps, entre la longueur (volume), la vitesse de raccourcissement et les forces (pressions ou tensions) développées par le myocarde.
L’analyse des courbes ventriculaires « tension (pression)-temps », « tension (pression)-longueur (volume) » et « temps-longueur (volume) » ainsi que des courbes « vitesse de raccourcissementtension (force) », « vitesse-longueur » et « tension-longueur », des fibres myocardiques ventriculaires aboutissent à formuler des lois :
– la force ou tension active (TA) développée par le ventricule est une fonction de la tension au repos ; celle-ci est une fonction de sa longueur ;
– leVS est une fonction du remplissage ventriculaire, lequel dépend de la pression de remplissage.
Avec une postcharge constante, à mesure que la précharge augmente, la tension totale, la vitesse de montée de la tension, la vitesse, l’amplitude et la durée du raccourcissement augmentent.
Avec une précharge constante, à mesure que la postcharge s’accroît, la vitesse, l’amplitude et la durée du raccourcissement diminuent.
La force et la vitesse de la contraction sont liées par une relation hyperbolique inverse, la force est maximale si la vitesse est zéro et la vitesse maximale pour une force nulle, Vmax et Fmax caractérisent l’état « contractile » du coeur.
L’évaluation de la contractilité est difficile ; elle repose sur l’analyse de certains paramètres :
– prééjectionnels (dp/dt max, (dp/dt)/Pmax, VCEmax et Vmax).
Ces paramètres sont rarement étudiés ; ils exigent l’emploi de capteurs particuliers, de haute fidélité et l’existence d’une contraction isométrique ;
– éjectionnels (surtout la FE et son évolution au cours de l’éjection ; mais la FE dépend beaucoup des conditions de charge ;
– télésystoliques (E’max). Sur les courbes de pression-volume ventriculaire, le quotient E de la pression sur le volume V à un instant déterminé t du cycle cardiaque, P(t) et V(t), est indépendant du VTDV (précharge) et de la pression diastolique aortique (postcharge).
Ce quotient E, au moment t, E(t) est constant pour des systoles consécutives et des points correspondants et caractérise parfaitement la « contractilité » : E(t) = P(t)/(V(t) - Vd).
La valeur de E serait maximale (E’max) pour le point situé au coin supérieur gauche des courbes P - V.
E max représente la pente de l’équation de la droite qui passe par les points supérieurs gauches des courbes de pression-volume ventriculaires.
E max peut être calculé à partir d’un point E max = PTS/VTS, ou de deux P1 et P2 obtenus à l’état basal et après une intervention modifiant les conditions de travail du coeur, pré- ou postcharge : E max = (PTS2 - PTS1)/(VTS2 - VTS1).
16- Analyse de la relaxation :
La relaxation ventriculaire dépend :
– de la charge ; l’augmentation de la charge au début de la systole s’accompagne d’un allongement de la durée de la contraction et d’un retard du début de la relaxation ; l’augmentation de la charge en fin de systole, avant la fermeture des sigmoïdes aortiques, comme dans les cas d’insuffisance aortique, raccourcit sa durée et accélère la relaxation et, inversement, la diminution de la charge ventriculaire en fin de systole, comme dans les cas d’insuffisance mitrale, allonge la contraction et diminue la vitesse de relaxation ;
– des conditions de l’inactivation ; – des forces de restauration, internes et externes ;
– de la distension des parois ventriculaires par la perfusion, remplissage des artères coronaires.
La qualité de la relaxation du ventricule gauche est généralement analysée en considérant la vitesse de chute de la pression ventriculaire gauche après la fermeture des sigmoïdes aortiques, qui coïncide avec le pic négatif de dp/dt.
La pression ventriculaire est, pendant cette phase, une fonction exponentielle du temps : P = e –Aô + B ; d’où en prenant des logarithmes népériens, ln P = -Aô + B ; B est négligeable.
Tau (ô), égal à -1/A, caractérise la vitesse de chute de la PVG.
17- Évaluation de la fonction diastolique passive : compliance et contrainte télédiastolique du ventricule gauche
La diastole proprement dite est un phénomène passif qui comprend le remplissage ventriculaire lent, le remplissage systolique auriculaire et qui dépend des propriétés viscoélastiques et de l’inertie du ventricule.
L’élasticité est la propriété physique qui permet à un matériel de retrouver ses dimensions initiales lorsque cesse la force qui l’a déformé.
La force Fe exercée par un corps élastique en revenant à sa longueur initiale est égale à la force de déformation Fd.
Cette force est d’autant plus importante que le corps est plus élastique et l’allongement relatif ¢L/L plus grand : Fe/S = E × ¢L/L. E est le module d’élasticité de Young.
L’allongement relatif d’un corps élastique est d’autant plus petit que E est plus grand (loi de Hooke) : ¢L/L = (1/E) × (Fe/S).
Le module d’élasticité E exprime la raideur et son inverse 1/E la distensibilité.
Mais les ressorts biologiques n’obéissent pas exactement aux lois de Hooke.
Les ventricules se comportent comme un corps viscoélastique ou solide de Kelvin.
La relation qui lie force et déformation n’est pas linéaire, mais exponentielle.
La distensibilité diminue à mesure que la tension et l’allongement augmentent.
La viscosité d’un corps fait que ses molécules frottent et freinent la vitesse d’extension et que l’allongement dû à une force dépend aussi du temps pendant lequel elle agit et de sa vitesse d’application.
L’inertie des ventricules tend, en début de diastole, à accroître, et en fin de diastole à décroître la pression de remplissage.
L’élasticité diastolique du ventricule gauche peut être étudiée en considérant les relations qui existent entre :
– les pressions et les volumes (compliance et élastance).
L’accroissement de la pression est proportionnel à l’augmentation relative du volume : dp = E’× dV/V ; E’ est le module d’élasticité en volume, ou élastance.
Il représente la résistance de l’organe à la distension, c’est-à-dire la rigidité.
Son inverse, 1/E’est la compliance, ou distensibilité en volume.
La compliance spécifique est le changement relatif de volume, dV/V, consécutif à un changement dp de pression.
Les caractéristiques du ventricule en tant que chambre, α ou Kp, de l’anglais pool, peuvent être appréciées en mesurant simultanément la pression et le volume et en calculant l’équation qui les relie.
Celle-ci serait du type : P = b eαV ; Gaasch et al donnent à b la valeur observée sur le chien, soit 0,43.
Dans ces conditions, PTDVG = 0,43 eα VTDG, d’où, α ou Kp = ln (2,33 PTDVG)/VTDVG.
Ainsi, α analyse l’élasticité de la chambre comme un tout, mais ne fournit pas de renseignements sur la qualité du myocarde.
– la « contrainte » (ou stress, ó force ou tension par unité de surface) et l’« étirement » (ou strain, €, déformation ou allongement par unité de longueur).
Ces deux paramètres sont liés par une relation exponentielle. La pente dó /d€ de cette courbe est une fonction de la force elle-même, dó /d€ = Kó + c = E.
E est la rigidité élastique qui caractérise le comportement du ventricule comme un tout et K est la constante de rigidité du myocarde.
Mais le calcul de ó et € est difficile et c’est pourquoi K est généralement estimé d’après la formule :
K = α (ou Kp) × V/M avec V, volume télédiastolique du ventricule et M, masse myocardique.
18- Apport des épreuves de provocation et pharmacodynamiques au diagnostic des cardiopathies :
L’évaluation ou le diagnostic de certaines cardiopathies ne sont pas toujours possibles ou faciles en tenant compte seulement des paramètres mesurés à un moment donné de la maladie, au repos, après traitement.
Il est parfois nécessaire de recourir à des manoeuvres de provocation, déclenchement d’extrasystoles, épreuve de Valsalva, d’effort, de remplissage ou pharmacodynamiques, qui, en modifiant les conditions de travail du coeur, permettent :
– de connaître la tolérance à l’effort, ou de mieux estimer la gravité de certaines sténoses ou cardiopathies (sténose tricuspide ou mitrale avec petit gradient transvalvulaire à l’état basal, au repos ; cardiomyopathies avec des pressions et des débits normaux à l’état basal) ; le débit cardiaque s’accroît normalement à l’effort de 5 mL pour chaque mL d’augmentation de la consommation d’oxygène (VO2) : (DC effort-DC repos)/(VO2 effort-VO2 repos) >= 5 ;
– de dévoiler des lésions cachées (syndromes de restriction ou péricardites chroniques « constrictives » masquées par un traitement déplectif, qui ne se révèlent qu’après une épreuve de « remplissage » ; sténose mitrale masquée par une insuffisance aortique importante qui, en présence d’une bradycardie, peut donner lieu à un croisement télédiastolique des pressions ventriculaire gauche et capillaire ; ce gradient devient holodiastolique et significatif à l’effort en cas de sténose mitrale serrée ; cardiomyopathies hypertrophiques obstructives avec un gradient intraventriculaire n’apparaissant qu’au cours d’une épreuve de Valsalva, après des extrasystoles, ou sous l’effet d’une perfusion d’isopropilnoradrénaline) ;
– d’établir un diagnostic différentiel :
– le comportement des pressions du ventricule gauche et de l’aorte au cours des extrasystoles permet de reconnaître la nature fixe ou dynamique d’une sténose (dans les deux cas, le gradient s’accroît sur la systole postextrasystolique, mais la pression aortique augmente dans les sténoses fixes, diminue dans les obstacles dynamiques ; c’est l’effet Brockenbrough, Braunwald et Morrow) ;
– après une épreuve de Valsalva, dans le cas des restrictions, les deux pressions ventriculaires restent superposées s’il s’agit d’une atteinte péricardique ; se croisent à un moment ou l’autre, généralement, dans les cardiomyopathies ;
– d’étudier le comportement des résistances artériolaires pulmonaires chez un patient candidat à une greffe cardiaque :
– en présence d’une HTAP « précapillaire », il faut vérifier le degré de réversibilité des résistances artériolaires pulmonaires en procédant à l’administration d’une drogue capable de les abaisser sélectivement, perfusion de nitroprussiate de sodium, inhalation de monoxyde d’azote ;
– en cas de résistances artériolaires pulmonaires basses, il faut s’assurer que celles-ci ne s’accroîtront pas en postopératoire face à l’augmentation du débit due à un coeur sain, en procédant à une perfusion de dobutamine suffisante pour obtenir un débit cardiaque normal.
source : medix.free.fr (très bon site de médecine à recommander)

