Le latex
Le latex est un produit naturel (caoutchouc naturel) issu de la sève de l’hévéa. Le latex est essentiellement utilisé dans la fabrication de gants de protection, de matériel médical mais également d’objets du quotidien.
Lors d’une allergie au latex, l’organisme réagit à certaines protéines. Les gants en latex poudrés libèrent un grand nombre de particules provoquant des allergies : la poudre contenant les allergènes se répand dans l’air de la pièce et est inhalée, entraînant une sensibilisation des voies respiratoires.
– Dans le domaine de la médecine et de l’hygiène :
Gants en caoutchouc, élastiques, chaussures en caoutchouc, seringues, poches de perfusion, appareils de mesure de tension, obturations de canaux de racines, masques respiratoires, cathéters, compresses élastiques, pansements, préservatifs, ballons insufflateurs Ambu.
– À la maison
Gants de ménage, bottes, revers de tapis, tapis de gymnastique, tapis de bain, bonnets de bain, sandales en plastique, combinaisons de plongée, lunettes de natation, alèses en caoutchouc.
– Au travail, au bureau, en voiture, dans les sports
Elastiques, poignées en caoutchouc, animaux en caoutchouc, gommes, colle pour timbres, colle, tapis de sol dans la voiture, pneus de vélo et de voiture, balles de squash, ballons de baudruche, gommes à mâcher, tétines.
Tableau I : Réactions croisées latex – aliments et niveau de preuve
– Allergies croisées
10 % des sujets allergiques au latex souffrent d’allergies croisées.
L’allergie croisée est une réaction à une substance donnée alors que le sujet est sensibilisé à une autre substance chimiquement apparentée.
Les allergies croisées sont ainsi dues à la présence de structures semblables ou très voisines dans des substances aussi différentes que des pollens, des aliments ou des poils d’animaux, etc.
Les allergies croisées les plus fréquentes surviennent entre des pollens, entre des aliments ou entre des pollens et des aliments.
Certaines sont facilement explicables car les deux allergènes ont une origine très proche comme l’allergie croisée à deux types de pollens ou à deux types d’acariens. En revanche, d’autres sont plus surprenantes, comme l’allergie croisée aux pollens et aux aliments. Les allergies croisées entre pollens et fruits ou légumes sont les plus fréquentes, comme par exemple l’allergie aux pollens de bouleau et aux pommes ou aux fruits à noyaux, l’allergie aux pollens d’armoise/ambroisie et au céleri ou aux épices ou encore l’allergie aux pollens de graminées et à la tomate ou à la pomme de terre. On considère que les personnes allergiques aux pollens présentent deux à trois fois plus fréquemment une allergie alimentaire que la population générale. Le plus souvent, c’est l’allergie aux pollens qui se manifeste en premier. Généralement décalées dans le temps, les allergies croisées sont cependant imprévisibles. La réaction à l’allergie croisée se manifeste souvent de manière bénigne par des picotements dans la bouche et la gorge, et passe souvent inaperçue. Les symptômes peuvent néanmoins être plus sévères : œdème, conjonctivite, rhinite, asthme, etc.
– Allergies croisées fréquentes :
- Ficus (ficus benjaminii, ficus elastica)
- Gutta-percha (souvent utilisée en stomatologie et en orthodontie, notamment comme matériau d’obturation des racines)
- Fruits exotiques : bananes, avocats, ananas, kiwis, pommes de terre, piments, châtaignes (vermicelles), etc.
– Troubles (symptômes)
- Démangeaisons, rougeurs et formation de papules sur la peau
- Urticaire
- Gonflement des muqueuses induisant une sécrétion aqueuse, écoulement nasal, nez bouché, crises d’éternuement
- Inflammation du tissu conjonctif
- Démangeaisons et gonflement des muqueuses du pharynx et du larynx
- Crises d’asthme, détresse respiratoire sévère
- Symptômes gastro-intestinaux
- Troubles cardiaques (notamment des arythmies)
- Fatigue physique pendant plusieurs jours
- Dans les cas les plus graves : chute de la tension artérielle allant jusqu’à la décompensation circulatoire (choc anaphylactique)
– Personnes risquant d’être fréquemment exposées au latex
Allergies croisées aliments-latex
La prévalence de l’allergie au latex dans la population générale est estimée entre 1 et 6,4%. Cette proportion est plus forte chez les sujets atopiques (9,5%), le personnel de santé (10,7%), les patients multi-opérés et les spina-bifida (18 à 73%). La liste des réactions croisées entre le latex et les aliments s’allonge périodiquement. Les aliments les plus fréquents sont la banane, l’avocat, le kiwi et la châtaigne. La découverte d’une allergie alimentaire pour un aliment qui peut présenter les réactions croisées avec le latex impose de rechercher une allergie croisée avec le latex. Si l’allergie au latex est confirmée, il faut alors prendre les précautions d’usage en évitant les contacts avec les objets pouvant contenir du latex, et surtout, il faut prévenir que toute intervention chirurgicale doit se dérouler dans une « atmosphère sans latex ».
- Spécialistes et assistants médicaux et dentaires, accompagnants et soignants
- Patients atteints de spina bifida (dos ouvert), d’anomalies au niveau génito-urinaire, ainsi que les sujets ayant subi de nombreuses interventions chirurgicales
- Ouvriers dans l’industrie de transformation du caoutchouc, du secteur du nettoyage, coiffeurs et coiffeuses
- Personnes génétiquement prédisposées et ayant tendance à faire des allergies (sujets atopiques)
– Examens (diagnostic)
- Anamnèse avec prise en compte des symptômes ; indications détaillées concernant le moment de survenue et la localisation des symptômes (éventuellement, tenue d’un carnet de bord)
- Mise en évidence d’anticorps dans le sang
- Test cutané / test de provocation : l’allergène est injecté sous la peau du patient. Ce test doit obligatoirement être effectué sous surveillance médicale étant donné qu’il peut provoquer une réaction violente, voire un choc anaphylactique.
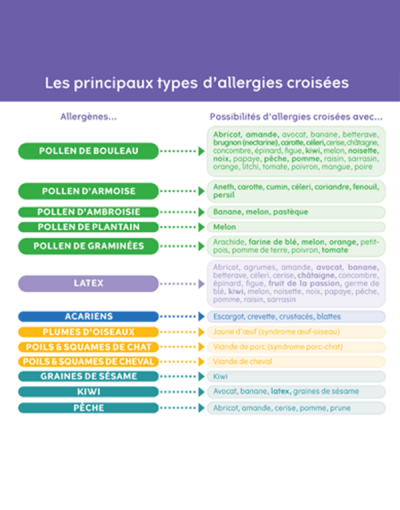
Les principales allergies croisées
source :
– santeweb.ch
– alk.fr
Recommandations de l’AAAAI (American Academy of Allergy, Asthma and Immunology) pour toute intervention chirurgicale
- identification des patients à haut risque : porteurs de spina-bifida, d’anomalies uro-génitales ou les autres multi-opérés,
- interroger tout patient, à la recherche de symptômes en faveur d’une allergie au latex : gonflements ou démangeaisons des muqueuses (buccale, rectale) lors d’un contact avec du latex (ballons gonflables, gants). Survenue d’un choc anaphylactique inexpliqué. Réactions locales ou générales lors de l’ingestion de châtaignes, bananes ou avocat,
- tester tous les patients à risque. Quand les tests ne sont pas corrélés à la clinique, ou s’ils ne peuvent être réalisés dans la crainte de la survenue d’un choc anaphylactique, on proposera la recherche d’IgE spécifiques,
- toute manoeuvre prévue chez un patient porteur de spina-bifida devraient être réalisée dans un environnement sans latex,
- tout patient ayant une histoire évocatrice doit subir les gestes médicaux et chirurgicaux dans un environnement sans latex.
Pour parfaire votre culture :
Le cismef
Allergies aux pénicillines et aux céphalosporines : faut-il craindre les réactions croisées ?
A voir le choc anaphylactique
§§§
L’allergie au caoutchouc ne prend pas de gants !
Les gants en latex ont largement été remplacés par des gants en caoutchouc synthétique pour éliminer le risque d’allergie de type I. L’éviction du latex n’a cependant pas résolu tous les problèmes : depuis quelques années, la fréquence des dermatites de contact professionnelles liées à l’utilisation des gants en caoutchouc semble en augmentation, particulièrement parmi le personnel des blocs chirurgicaux.
Le test au thiuram mix de la batterie standard explore l’allergie de contact au groupe des dithiocarbamates (accélérateurs de la vulcanisation).
La diphénylguanidine est par ailleurs un allergène de contact possible dans l’allergie au caoutchouc. Elle est souvent utilisée comme vulcanisateur en association avec le mercaptobenzothiazole.
Mais les additifs du caoutchouc ne sont pas seuls en cause. Les gants poudrés ont progressivement été supplantée par des gants sur la face interne desquels sont présentes d’autres substances destinées à faciliter l’enfilage. Le chlorure de cétylpyridinium est ainsi de plus en plus utilisé. Il a, en plus de ses propriétés de lubrification, des vertus antibactériennes. Il peut agir comme un irritant et/ou comme un allergène.
Une étude a été menée en Suède dans le but d’évaluer l’exposition cutanée aux substances chimiques des gants et tout particulièrement à la diphénylguanidine et au chlorure de cétylpyridinium.
Ce travail a permis de recruter 16 personnes (dont 4 avaient un terrain atopique). La plupart occupaient le même emploi depuis des dizaines d’années mais n’avaient une dermatite des mains que depuis quelques mois.
Les tests épicutanés ont été réalisés avec les batteries de base, des batteries additionnelles mais aussi avec les gants du patient à l’aide de Finn Chambers°.
Ils ont été appliqués sur la partie haute du dos, retirés et lus à 48 heures puis de nouveau à J3, J4 et J7.
Thiuram-mix et DPG (1,3-diphénylguanidine) ont été testés chez tous les patients alors que seulement 8 d’entre eux ont eu des patch-tests avec le chlorure de cétylpyridinium.
Une allergie de contact au thiuram mix a été mise en évidence chez 8 patients sur 16, au DPG chez 12 patients sur 16 et au chlorure de cétylpyridinium chez 7 patients sur 8.
L’analyse des gants en polyisoprène n’a pas retrouvé de thiuram mais des concentrations en chlorure de cétylpyridinium et en DPG plus élevées à l’intérieur qu’à l’extérieur des gants.
Dr Geneviève Démonet (JIM)
Pontén A et coll. : Occupational allergic contact dermatitis caused by sterile non-latex protective gloves : clinical investigation and chemical analyses. Contact Dermatitis, 2013 ; 68 : 103–110.
Produits iodés et allergie
- « L allergie à l iode » n existe pas ! E Bresson Infirmerie Protestante Lyon Caluire (Pour en finir avec cette croyance)
Certaines allergies médicamenteuses sont des réactions à des virus “dormants”
Communiqué | 26 août 2010 - 15h34 | Par INSERM (Salle de presse)
Philippe Musette et ses collaborateurs (Unité Inserm 905 “Physiopathologie et biothérapies des maladies inflammatoires et autoimmunes”, Rouen) viennent de montrer que les réactions allergiques d’origine médicamenteuse (liées à la consommation de médicaments) sont en fait provoquées par des réactions immunitaires contre des virus. En clair, chez certains individus sensibles, la médication entraîne la réactivation du virus EBV (Epstein Barr Virus), un virus de la famille Herpes, en temps normal à l’état dit “dormant”. Le virus se multiplie et provoque une réponse immunitaire ce qui entraine des éruptions cutanées et désordres viscéraux. Le détail des résultats obtenus, fondés sur le suivi de 40 patients, est publié dans la revue Science Translational Medicine.
Les chercheurs ont suivi 40 patients qui présentaient un DRESS (pour Drug reaction with eosinophilia and systemic symptoms c’est-à-dire une réaction au médicament entraînant augmentation de la concentration en lymphocytes éosinophiles et symptômes allergiques cutanés et viscéraux – hépatique, pulmonaire et rénal) en réponse à différents médicaments appartenant principalement à la famille des antibiotiques et des antiépileptiques. Philippe Musette et son équipe ont analysé la réplication virale (la multiplication du virus) chez ces 40 personnes : chez une grande majorité d’entre elles (76%), les chercheurs ont observé la multiplication du nombre d’EBV dans le sang.
Les observations effectuées au niveau des cellules de l’immunité de ces patients (lymphocytes TCD8+ en particulier) montrent que la majeure partie de la réponse immunitaire des patients est dirigée contre les particules virales. L’organisme ne réagit donc pas contre le médicament, jusqu’alors jugé responsable du déclenchement des symptômes d’allergie, mais il lutte contre l’invasion, et la réactivation virale induite par le médicament.
Les médicaments testés pourraient donc déclencher l’activation des virus Epstein Barr dormants des patients, par un mécanisme non encore élucidé mais en cours d’investigation, estiment Philippe Musette et son équipe.
Les chercheurs montrent par ailleurs que les 3 médicaments testés entraînent ce processus chez les patients “DRESS” mais pas chez les personnes-témoins. Ceci suppose donc aussi qu’il existe des déterminants encore à définir de cette plus ou moins grande vulnérabilité à la réaction allergique médicamenteuse.
Ces résultats pourraient remettre en question le point de vue généralement admis concernant les mécanismes de l’allergie médicamenteuse. Le traitement des manifestations cutanées notamment pourrait évoluer en proposant, en plus de l’arrêt du médicament en cause, une thérapie antivirale.
Pour les auteurs, il s’agit probablement d’une des premières études démontrant le rôle d’EBV (Epstein Barr virus) dans la réaction allergique médicamenteuse.
Contact Chercheur
Philippe Musette Unité Inserm 905 "Physiopathologie et biothérapies des maladies inflammatoires et autoimmunes", Rouen Tél. : 06 22 51 27 54
– Pour rester sur le même sujet
L’incidence de la réaction anaphylactique a été évaluée en France, en 1996, à 1/13 000
anesthésies générales et locorégionales, toutes substances responsables confondus.
L’incidence de l’anaphylaxie aux curares a été de 1/6 500 anesthésies ayant comporté un curare (D).
Les substances responsables des réactions anaphylactiques survenues en cours
d’anesthésie ont été identifiées à partir de 4 400 cas d’anaphylaxie publiés depuis 1980 dans la littérature en langues anglaise et française. Les curares représentent 62 % d’entre elles, le latex 16,5%, les hypnotiques 7,4%, les antibiotiques 4,7%, les substituts du plasma 3,6%, les morphiniques 1,9%. L’allergie aux anesthésiques locaux apparaît exceptionnelle (0,7%).
Aucune réaction anaphylactique n’a été publiée avec les anesthésiques halogénés. D’autres substances peuvent induire une anaphylaxie en cours d’anesthésie : aprotinine, chlorhexidine, protamine, papaïne, héparine...
Source : SFAR Réalité du risque allergique en anesthésie -Incidence - Morbidité - Mortalité - Substances responsables - Tableaux cliniques
Curares et choc anaphylactique : 4 % de mortalité en France
25.09.14
Les réactions anaphylactiques aux curares sont associées à un taux de mortalité de plus de 4% en France, selon une étude présentée le 18 septembre 2014 au congrès de la Société française d’anesthésie et de réanimation (Sfar) à Paris.
Réactions anaphylactiques aux curares : 4% de mortalité en France
A partir de la base de données du système national de pharmacovigilance, Marie Reitter du CHU de Nancy et ses collègues ont sélectionné les cas de réactions anaphylactiques aux curares, survenus entre janvier 2000 et décembre 2011, et déterminé le taux de mortalité associé et les facteurs de risque de décès.
L’analyse a porté sur 2 022 cas de réaction d’hypersensibilité à un curare, dont 84 se sont avérés mortels. Le taux de mortalité moyen s’élevait à 4,1%. Parmi les cas examinés, 1 247 cas de réaction sévère (grade 3 et 4) ont été retenus afin d’identifier les facteurs de risque de décès.
Aucun curare en particulier n’était identifié comme facteur de risque de surmortalité, même si le curare le plus souvent incriminé était le suxamethonium (65,4%), suivi de l’atracurium (14,5%), puis du rocuronium (8,4%), du cisatracurium (7,5%) et du vecuronium (Norcuron*, MSD) (1,8%).
Le sexe féminin était protecteur contre le risque de décès, avec une probabilité de décès significativement réduite de 60%. Le contexte d’urgence augmentait significativement la probabilité de décès d’un facteur 2,6, l’obésité d’un facteur 2,4, un antécédent d’hypertension artérielle (HTA) d’un facteur 2,5, un antécédent de maladie cardiovasculaire autre d’un facteur 4,4 et l’utilisation d’un bêta-bloquant au long cours d’un facteur 4,2.
Le délai moyen de survenue du premier symptôme d’anaphylaxie était de 2,1 minutes et le délai moyen d’injection du premier bolus d’adrénaline de 3,4 min, avec une dose totale injectée de 15 mg en bolus. Il n’y avait aucune différence significative de prise en charge entre les décès "précoces" (survenus immédiatement ou après mise en place d’une assistance cardiocirculatoire) et "tardifs" (liés à une défaillance multiviscérale secondaire à l’arrêt cardiovasculaire récupéré).
La prise en charge des cas mortels était conforme aux recommandations internationales, avec un délai court pour la mise en oeuvre des thérapeutiques spécifiques, soulignent les auteurs. On peut donc supposer qu’il existe une résistance à l’adrénaline. Il est donc nécessaire de développer de nouvelles approches thérapeutiques, concluent-ils.
Anaphylaxis to neuromuscular blocking drugs
Mis en ligne le 17 Juin 2013
Un article du BJA commenté par PM Mertes, pour le Comité Scientifique de la SFAR.
« Anaphylaxis to neuromuscular blocking drugs : incidence and cross-reactivity in Western Australia from 2002 to 2011.
Sadleir PH, Clarke RC, Bunning DL, Platt PR.
Br J Anaesth. 2013 Jun ;110(6):981-7.
»
- Rationnel
Les curares représentent la première cause de réaction d’hypersensibilité immédiate d’origine allergique en anesthésie. Une controverse existe concernant le risque d’allergie respectif des différents curares. Ce travail analyse le risque allergique des différents curares et la fréquence de réactivité croisée.
- Méthodologie
Analyse des réactions anaphylactiques dues à un curare explorées au sein du centre de référence Australien (Western Australia) sur une période de 10 ans. Exploration des cas et analyse de la sensibilisation croisée selon un protocole standardisé conforme aux recommandations Françaises. Estimation de la population exposée à partir des chiffres de vente des différents curares sur une période de 5 ans (2007-2011).
- Résultats
Nombre de choc anaphylactiques : 80 (grade 2 à 4).
Produits incriminés : rocuronium 56% (45/80), succinylcholine 21% (17/80), vécuronium 11% (9/80), atracurium 9% (7/80), mivacurium 3% (2/80). Pancuronium et cisatracurium aucun cas.
Estimation du nombre de sujets exposés à un curare : 1,16 million (2002-2011), succinylcholine exclue (en raison de la surestimation de l’exposition lié à une préparation systématique mais sans utilisation systématique).
Risque relatif par produit : risque significativement plus élevé avec le rocuronium (P<0,0013)
– Rocuronium 8,0/ 100 000 (95% CI 5,8–11/100 000),
– Vécuronium 2,8/100 000 (95% CI 1,3–5,3/100 000)
– Atracurium 4,01/100 000 (95% CI 1,6–8,3/100 000).
Chez les patients ayant présenté un choc anaphylactique au rocuronium ou au vecuronium, la prévalence de la réactivité croisée était plus faible avec le cis-atracurium.
- Points forts
- Explorations standardisées conformément aux recommandations actuelles
- Explorations centralisées dans un centre de référence unique
- Confirmation des résultats précédemment rapportés dans la littérature concernant un risque relatif majoré lors de l’utilisation du rocuronium (Norvège, France)1-3.
- Etude de sensibilisation croisée confirmant le taux de réaction plus faible observé avec le cis-atracurium en cas d’allergie à un autre curare.
- Discussion qui décrit d’éventuels facteurs extérieurs de sensibilisation tel que la pholcodine et qui pourraient avoir de vraies conséquences de santé publique en France4, 5.
- Points faibles
- Limites classiques des études épidémiologiques concernant les biais de déclaration en particulier pour les réactions peu sévères (grade 1).
- Extrapolation du nombre de patients exposés à partir des chiffres de vente des produits.
- Nombre de patients exposés au cis-atracurium trop faible pour apprécier le risque relatif de réactions liés à son utilisation.
- Impossibilité d’estimer le risque relatif lié à l’utilisation de succinylcholine.
- Implications pour la pratique clinique
L’existence d’un risque relatif de réaction allergique accrue lors de l’utilisation de rocuronium comparée au vécuronium et à l’atracurium, et d’un risque de sensibilisation croisée plus faible avec le cis-atracurium doit être connue lors du choix d’un curare de risque intermédiaire (curarisation et décurarisation).
– Références
- 1. Laake JH, Rottingen JA. Rocuronium and anaphylaxis—a statistical challenge. Acta Anaesthesiol Scand 2001 ; 45:1196-203.
- 2. Mertes PM, Laxenaire MC, Alla F. Anaphylactic and anaphylactoid reactions occurring during anesthesia in France in 1999-2000. Anesthesiology 2003 ; 99:536-45.
- 3. Mertes PM, Alla F, Trechot P, Auroy Y, Jougla E. Anaphylaxis during anesthesia in France : an 8-year national survey. J Allergy Clin Immunol 2011 ; 128:366-73.
- 4. Florvaag E, Johansson SG. Pholcodine in cough medicines and IgE-sensitization in the EU : an urgent task. Allergy 2012 ; 67:581-2.
- 5. Mertes PM, Demoly P, Malinovsky JM. Hypersensitivity reactions in the anesthesia setting/allergic reactions to anesthetics. Curr Opin Allergy Clin Immunol 2012 ; 12:361-8.
source : http://www.chu-rouen.fr/
LE PATIENT ALLERGIQUE A LA CONSULTATION ANESTHÉSIQUE
Jean-Marc Malinovsky
Département d’Anesthésie-Réanimation
Hôtel-Dieu, 44093, Nantes
La notion d’antécédents allergiques, de quelque nature qu’ils soient, est retrouvée chez 15 à 20 % des patients interrogés avant une anesthésie. Connaissant le risque allergique propre et le potentiel histaminolibérateur des médicaments anesthésiques et des autres agents utilisés pendant l’anesthésie, on peut se demander si un patient qui se dit allergique n’a pas plus de risque de faire une réaction « allergique » d’origine immunologique (= anaphylaxie) ou non (= histaminolibération non spécifique) pendant l’anesthésie.
En fait, l’incidence des réactions anaphylactoïdes peranesthésiques est très faible : 1 réaction anaphylactoïde pour 3.500 anesthésies (anaphylaxie + histaminolibération non spécifique), 1 réaction anaphylactique vraie pour 13.000 anesthésies. Ceci est sans commune mesure avec l’incidence élevée de l’allergie dans la population française en général, où l’atopie est présente chez 20 à 25 % des gens, l’allergie médicamenteuse chez 15 %, l’allergie alimentaire chez 10 %, la sensibilisation au latex chez 3 à 40 % suivant les catégories de patients. Le lien entre les antécédents allergiques et le risque anesthésique n’est pas évident à établir sur ces données.
Par ailleurs, chez les patients qui ont fait une réaction anaphylactoïde peranesthésique, on ne retrouve pas toujours une incidence plus élevée d’antécédents allergiques que dans la population normale, à l’exception de certains groupes de patients chez qui une stratégie de prévention doit être instituée dès la consultation d’anesthésie.
1 Quels sont les patients allergiques à risque de réaction anaphylactoïde peranesthésique ?
1.1. Patients allergiques à risque d’anaphylaxie peranesthésique :
1.1.1. Patient réputé allergique à un des médicaments de l’anesthésie (curares avant tout) ou produits susceptibles d’être administrés pour l’anesthésie ou l’analgésie postopératoire (antibiotique, substitut du plasma, latex, chlorhexidine, aprotinine, paracétamol…..), le diagnostic ayant été déjà établi par un bilan allergologique.
1.1.2. Patient ayant manifesté une réaction « allergique » lors d’une anesthésie antérieure (érythème, urticaire, bronchospasme, collapsus) et n’ayant pas fait l’objet d’un bilan allergologique diagnostique.
1.1.3. Patient présentant des signes d’intolérance au contact du latex (urticaire, œdème, rhinite, conjonctivite, asthme) ou étant allergique à certains fruits (banane, kiwi, avocat, châtaigne….)
1.1.4. Enfants multiopérés et notamment pour spina bifida, myéloméningocèle en raison de la fréquence importante de la sensibilisation au latex et de l’incidence élevée des chocs anaphylactiques au latex.
1.2. Patients allergiques ou supposés tels, dont le risque d’anaphylaxie peranesthésique n’a pas été prouvé :
· atopie (asthme, rhinite, dermatite, conjonctivite),
· allergie à un médicament et/ou un produit qui ne sera pas utilisé au cours de l’anesthésie,
· intolérance à l’aspirine et aux AINS, conservateurs (métabisulfites, parabens), antibiotiques, analgésiques….., désinfectants, colorants, produits ménagers, produits capillaires,
· allergie de type retardé (24 à 72 h) aux médicaments (antiseptiques, antibiotiques, héparine….), métaux, caoutchouc, pommades diverses,
· réaction anaphylactoïde aux produits de contraste iodés,
· mastocytose,
· œdème angioneurotique héréditaire ou acquis,
· allergie ou intolérance alimentaire à l’arachide, soja, crustacés, légumes, poissons, alcool…..
Il n’y a actuellement aucun argument scientifiquement prouvé et publié pour considérer que ces catégories de patients sont sensibilisés aux agents de l’anesthésie et pourraient faire un choc anaphylactique peranesthésique. En revanche, certaines précautions dans les gestes anesthésiques sont à prendre chez les patients ayant un asthme (risque d’aggraver l’hyperréactivité bronchique), une mastocytose et un œdème angioneurotique héréditaire.
2 Indications du bilan allergologique préanesthésique
2.1. Une consultation allergologique est à réaliser, en période préanesthésique uniquement chez les patients allergiques définis dans le paragraphe 1 : « patients allergiques à risque d’anaphylaxie peranesthésique » (1-1).
Les investigations allergologiques pratiquées auront pour but de vérifier si les symptômes allégués sont liés à une sensibilisation et de détecter le produit responsable afin de l’éliminer du protocole anesthésique ultérieur. L’allergologue testera les produits que le patient avait reçu, ce qui oblige l’anesthésiste à fournir le protocole de l’époque. Il s’agit d’un bilan diagnostique d’une réaction antérieure. En aucune façon, ce bilan ne doit être étendu aux anesthésiques prévus pour l’anesthésie future à la recherche d’une sensibilisation latente ignorée du sujet (= bilan prédictif). On ne connaît en effet pas la valeur prédictive positive et négative des tests cutanés et/ou biologiques dans la population générale. La pratique du bilan prédictif représente une fausse sécurité.
2.2. Il n’y a pas lieu de pratiquer un bilan allergologique préanesthésique chez les patients dont les antécédents allergiques ou supposés tels, ne constituent pas un risque d’anaphylaxie peranesthésique (paragraphe 1-2). Ce bilan correspondrait à un bilan prédictif dont la pratique est à bannir dans l’ignorance actuelle des valeurs prédictive positive et négative dans la population allergique. Tout comme une valeur faussement négative, une valeur faussement positive peut avoir des conséquences néfastes en matière d’anesthésie en induisant un changement de technique non nécessairement adapté. De ce fait, le rapport bénéfice/risque d’une telle pratique est inconnu.
3 Conduite du bilan allergologique préopératoire et choix de la technique anesthésique
31 = Chez les patients connus allergiques à un des médicaments de l’anesthésie ou produits susceptibles d’être administrés pour l’anesthésie ou l’analgésie postopératoire (paragraphe 1.1.1.), les conclusions du bilan allergologique antérieur sont à garder. S’il s’agit d’une allergie à un curare, on peut actualiser le bilan en testant les curares nouvellement commercialisés.
32 = Chez les autres patients allergiques à risque d’anaphylaxie peranesthésique (paragraphe 1.1.2.) :
En situation réglée, l’anesthésiste doit rechercher le protocole anesthésique suspect d’être à l’origine de la réaction pour le transmettre à l’allergologue qui réalisera les tests.
· Si le protocole est inconnu, il ne faut tester que les curares et le latex (par tests cutanés ± IgE spécifiques) ;
· Si le protocole est identifié, il faut tester tous les médicaments du protocole ancien et le latex (tests cutanés ± IgE spécifiques) ;
· S’il s’agit d’anesthésiques locaux : l’allergologue pratiquera un test de réintroduction en milieu hospitalier, après s’être assuré que les tests cutanés avec cet anesthésique local étaient négatifs.
Chez la femme enceinte suspecte d’intolérance aux anesthésiques locaux et candidate à une analgésie péridurale pour le travail, les anesthésiques locaux sont testés par l’allergologue en IDR. En cas de négativité, le test de réintroduction peut être pratiqué par l’anesthésiste en salle de naissance (0,5 à 1 ml de solution d’adrénaline non diluée et non adrénalinée par voie sous-cutanée). Le test est négatif si aucune réaction de type allergique n’est survenue pendant les 30 min suivant l’injection.
En situation d’urgence : le principe de précaution fait exclure le latex de l’environnement du patient, utiliser une anesthésie locorégionale ou une anesthésie générale en évitant les curares et les médicaments histaminolibérateurs.
33 = Chez les patients suspects d’être sensibilisés au latex (paragraphes 1.1.3. et 1.1.4.), l’allergologue pratiquera des prick-tests au latex ± des IgE spécifiques du latex. Il n’y a pas de raison de rechercher une sensibilisation aux anesthésiques et aux curares.
4 Prévention et prémédication du patient allergique
41 Prévention
La seule prévention efficace de l’anaphylaxie consiste en l’identification de l’allergène responsable et en son éviction définitive afin d’éviter les accidents allergiques à répétition. En cas d’allergie aux curares et aux antibiotiques, l’éviction concernera aussi les molécules qui partagent le même épitope (= allergie croisée).
Pour détecter les patients sensibilisés aux médicaments anesthésiques et/ou les produits qui seront administrés pendant l’anesthésie, le principe de la dose-test par voie intraveineuse est à proscrire dans la mesure où une très faible dose d’allergène peut déclencher une anaphylaxie chez le sujet allergique à ce produit.
Pour les patients allergiques au latex, un environnement opératoire exempt de latex est à instituer, dans les salles d’intervention, les SSPI, les secteurs d’hospitalisation. Une check-liste de prise en charge du patient est conseillée, à commencer dès la consultation d’anesthésie. Elle suivra le patient allergique jusqu’à sa sortie de l’hôpital.
Le principe de la check-liste peut aussi être appliquée aux patients allergiques ou intolérants aux médicaments administrés en période périopératoire (antibiotique, aspirine, AINS, antalgiques, désinfectants…..).
42 Prémédication
Il n’existe aucune médication antiallergique qui s’opposera au déclenchement d’un choc anaphylactique, que ce soit les anti-H1 seuls ou associés aux anti-H2 et/ou les corticoïdes. Il s’agit donc d’une fausse sécurité chez les patients allergiques à risque d’anaphylaxie peranesthésique (groupe 1-1).
En revanche, une prescription par un anti-H1 seul ou associé à un anti-H2 semble prévenir le bronchospasme et les variations hémodynamiques secondaires à une histaminolibération non spécifique. On pourrait ainsi la réserver aux patients atopiques et asthmatiques, à ceux qui font de l’urticaire ou érythème après absorption d’aliments ou médicaments réputés histaminolibérateurs.
Références :
1 Prévention du risque allergique peranesthésique. Recommandations pour la Pratique Clinique, SFAR-ANAES 2001.
Texte court : www.sfar.org ; Textes longs : Ann Fr Anesth Réanim 2002 ;21 (suppl 1) : 1-180.
2 Réanimation des arrêts cardiocirculatoires de l’adulte. Conférence d’experts, SFAR 1995 (www.sfar.org).
QUEL TYPE ANESTHÉSIE GÉNÉRALE EN URGENCE CHEZ LE PATIENT ALLERGIQUE ?
Claude Meistelman
Service d’Anesthésie-réanimation, Hôpital de Brabois, rue du Morvan, 54511 Vandœuvre
Peu de sujets ont entraîné autant d’avis divergents que la prise en charge anesthésique du patient allergique. Les prises de position nombreuses mais ne reposant pas toujours sur des preuves scientifiques ont pu faire croire à certains anesthésistes que le risque allergique serait majeur en oubliant que les complications d’une intubation difficile ou d’une inhalation lors de l’induction font courir au patient un risque au moins aussi important. La Société Française d’Anesthésie et de réanimation a organisé et présenté en 2001 des recommandations pour la pratique clinique sur la « Prévention du risque allergique peranesthésique » (1). Ces recommandations ont pour principal but de standardiser le diagnostic et la prise en charge en cas de réaction allergique peranesthésique. D’autre part, la conférence de consensus de juillet 1999 a fait le point sur les effets et les indications de la curarisation en anesthésie. Elle recommande sans aucune ambiguïté l’utilisation des techniques de « crash induction » avec la succinylcholine en cas d’anesthésie générale chez le patient à l’estomac plein. La difficulté majeure reste le cas du patient allergique ou présumé allergique, présentant un estomac plein et devant être opéré en urgence. Après avoir présenté les différents types de réactions allergiques et les agents incriminés, nous envisagerons plusieurs cas de figure en fonction des médicaments en cause et du terrain.
1. Mécanismes
Les réactions anaphylactiques observées avec les agents anesthésiques sont liés à la présence d’IgE spécifiques qui vont venir se fixer sur les récepteurs spécifiques membranaires des mastocytes et des basophiles circulants ainsi que sur les plaquettes en cas d’exposition à l’agent concerné. Les réactions cliniques observée en anesthésie ont une traduction clinique nette en raison de l’administration intraveineuse des agents anesthésiques ce qui entraîne une libération majeure de médiateurs tels l’histamine, la tryptase, les prostaglandines et les leucotriènes. Le choc anaphylactique est la forme la plus grave de l’anaphylaxie.
De nombreux produits utilisés en anesthésie sont capables de produire des anticorps IgE. Il peut s’agir des curares 62 %) quels qu’ils soient, des agents anesthésiques intraveineux voire des benzodiazépines ou des morphinomimétiques (2 ;3). En dehors des agents anesthésiques proprement dits, on peut citer les gélatines, l’aprotinine, la protamine et les antibiotiques. Ces derniers sont impliqués de plus en plus souvent et ce quel que soit le pays concerné, la fréquence variant de 8 % (3) à 24 % (4). Une explication serait le développement de l’antibioprophylaxie dans de nombreux types de chirurgie, l’antibiotique étant administré en intraveineux dans les minutes précédant ou suivant l’induction de l’anesthésie. Enfin la responsabilité du latex est régulièrement retrouvée avec un fréquence comprise entre 12 et 16%. L’existence de réactions croisées entre curares, y compris de familles chimiques différentes, ou entre antibiotiques s’explique par l’existence d’une partie allergénique commune entre différentes substances (2). Plus récemment c’est la chlorhexidine qui a été reconnue responsable de plusieurs accidents anaphylactiques peranesthésiques (5). Elle serait même la première cause d’accident allergique peropératoire au Danemark (6).
A l’opposé, l’histaminolibération non spécifique n’est qu’une exagération de l’effet pharmacologique du produit utilisé. Cette réaction non liée aux anticorps peut avoir lieu en dehors de toute exposition préalable à l’agent. Bien que discuté, il semblerait que l’histaminolibération puisse être plus marquée en cas de terrain atopique. En revanche, la vitesse d’administration ou la dose utilisée influencent l’importance de l’histaminolibération (1). L’histaminolibération pharmacologique entraîne des signes cliniques moindres que ceux rencontrés lors d’un accident allergique vrai. Les signes peuvent aller d’une simple rougeur ou d’une éruption urticarienne le long de la veine à une éruption généralisée, un collapsus cardiovasculaire ou un bronchospasme. Les agents le plus souvent en cause sont les curares de la famille des benzylisoquinolines (atracurium, mivacurium), le thiopental, le propofol, la morphine et les gélatines. Il faut garder à l’esprit qu’un agent responsable d’histaminolibération non spécifique peut être à l’origine d’un accident allergique lié aux IgE.
L’activation du complément n’est que rarement en cause lors des accidents anesthésiques. Elle peut se rencontrer avec les dextrans, la protamine ou les produits iodés de contraste.
2. Epidémiologie
En France, les curares restent à l’origine de la majorité des accidents allergiques liés aux IgE mais il faut cependant noter que leur part est passée de 81% dans les années 1984-1989 à 69 % lors de la dernière enquête nationale réalisée entre 1997 et 1998. La deuxième cause d’accidents allergiques per anesthésiques est liée au latex avec un pourcentage de 12 % lors de cette même enquête. Les antibiotiques apparaissent en troisième position, ils sont impliqués dans 8 % des accidents alors qu’ils ne représentaient que 2 % des cas dans les années 1984-1989. Le développement de l’antibioprophylaxie et les conférences de consensus sur ce sujet expliquent en partie au moins l’augmentation de fréquence des accidents liés aux antibiotiques. Les hypnotiques arrivent ensuite avec 3,7 % des cas. Il est également intéressant de noter que 467 accidents allergiques ont été colligés en 24 mois de janvier 1997 à décembre 1998 alors que 1030 accidents avaient été enregistrés en 30 mois entre 1992 et 94 et 734 de juillet 1994 à décembre 1996 (2 ;7). Ces chiffres sont à rapprocher de ceux observés en Australie ou les curares occupent la première place avec 56% des cas suivis par les antibiotiques (23,6%) puis les agents anesthésiques intraveineux (8%) et les produits de remplissage (7%) (4).
L’enquête épidémiologique « 3 jours d’anesthésie » a montré que 2,4 millions de patients anesthésiés étaient curarisés par an (8) alors qu’environ 180 cas d’allergie aux curares sont observés par an. En utilisant ces résultats, la fréquence des cas d’allergie aux curares est d’approximativement 1 cas pour 13 300 patients curarisés. Il n’existe actuellement aucun argument scientifique pour attribuer une fréquence plus importante aux accidents allergiques liés aux curares. Il est à noter qu’une telle fréquence est proche de celle des hyperthermies malignes après administration d’agents halogénés dont personne ne remet en cause l’utilisation anesthésique !
Un des principaux problèmes reste de savoir si un patient présentant des antécédents allergiques est plus exposé à un accident allergique peranesthésique. Bien qu’il n’y ait pas de réponse définitive à ce problème, la fréquence des antécédents allergiques ne semble pas plus importante chez des patients ayant présenté un accident allergique peranesthésique que dans une population témoin. Ainsi 17% des patients ayant présenté un cas d’allergie aux curares avaient des antécédents allergiques alors que dans la population contrôle 15% des patients présentaient des antécédents allergiques. En revanche 27% des patients ayant développé un accident allergique peranesthésique lié aux antibiotiques avaient des antécédents allergiques. En dehors des accidents liés au latex ou un terrain atopique (asthme, rhume des foins) est retrouvé dans 55% des cas, l’atopie ne semble pas être un facteur favorisant la survenue d’une accident allergique à un curare ou à un antibiotique (2) (1). En résumé, un patient allergique à un médicament et/ou un produit qui ne sera pas utilisé au cours de l’anesthésie ne sera pas considéré à risque d’anaphylaxie peranesthésique (1)
Deux point méritent enfin d’être soulignés la fréquence des allergies croisées que l’on peut rencontrer avec les antibiotiques ou les curares, la fréquence atteignant 70% sans que l’on puisse préciser à l’avance les autres curares responsables d’allergie chez un patient donné. L’existence d’accidents allergiques aux curares chez des patients n’ayant jamais été anesthésiés (17 à 30 % des cas) pourrait s’expliquer par une sensibilisation préalable aux ammoniums quaternaires par contacts répétés avec de produits comme certains cosmétiques ou les produits de nettoyage tels les lessives.
3. Conduite de l’anesthésie
Plusieurs situations très différentes peuvent se rencontrer lors de l’anesthésie en urgence d’un patient présentant un estomac plein. On peut schématiquement séparer le patient ayant présenté un accident allergique peranesthésique à un agent qui a été identifié, le patient allergique vrai à des agents étrangers à l’anesthésie et enfin le patient suspect d’allergie.
3.1 allergie à un agent anesthésique
La première situation est celle d’un patient présentant une allergie vraie aux curares avec une carte précisant les agents en cause. Il s’agit donc d’un patient qui a été testé. A partir du moment ou la succinylcholine n’apparaît pas dans les agents responsables d’allergie, celle ci peut être employée dans le cadre d’une « crash induction » typique telle qu’elle est recommandée dans la conférence de consensus sur la curarisation. En cas de doute on peut envisager en raison du terrain allergique une anesthésie loco-régionale si elle est possible techniquement et acceptée par le patient. Cette technique n’est pas une parade absolue en raison du risque d’hypotension et/ou de malaise vagal à l’origine de vomissements. La sédation intraveineuse sera proscrite.
En cas d’allergie à la succinylcholine, l’alternative recommandée est l’association propofol-alfentanil ou propofol-rémifentanil tout en sachant qu’il faut une dose minimale de respectivement 30 µg/kg d’alfentanil ou 2 µg/kg de rémifentanil pour obtenir des conditions d’intubation à 1 minute proches de celles procurées par la succinylcholine (9). Il faut savoir que le recours à cette technique va entraîner une baisse d’au moins 20% de la pression artérielle et un certain degré d’incompétence des voies aériennes supérieures pouvant durer plus d’une heure (10). Cette technique qui n’a jamais été évaluée dans le cadre de l’estomac plein n’est pas exempte de risques vu l’effet émétisant de l’alfentanil ou du rémifentanil. Si le patient est en mauvais état général (ASA 3 ou 4) une intubation première sous contrôle fibroscopique peut être envisagée tout en sachant qu’il n’est pas toujours facile de disposer du matériel dans le cadre de l’urgence et que cette technique nécessite une pratique régulière. Certains ont proposé l’utilisation de rocuronium qui permet d’obtenir de bonnes conditions d’intubation dans un délai proche de celui observé avec la succinylcholine (60 à 90 secondes). Il faut garder en mémoire que le risque majeur est celui d’une intubation difficile imprévue sur un estomac plein. Cette technique est à réserver, à priori, aux patients ayant déjà eu des anesthésies générales sans problèmes. Heier a récemment attiré l’attention sur le risque de bronchospasme lié à la précipitation du thiopental par l’administration simultanée de rocuronium (11). Cette technique ne doit être retenue que de façon exceptionnelle, il est impératif de bien rincer la ligne d’administration après le thiopental et avant l’injection de rocuronium. Dans la dernière série française, le rocuronium serait plus souvent en cause dans la survenue d’accidents allergiques que les autres curares (3), ce qui n’est pas été confirmé par les séries australiennes (12) et danoises (6)
Une situation plus difficile est celle d’un patient informant qu’il a présenté un accident allergique lors d’une précédente anesthésie et ne se souvenant pas de l’agent en cause. Si le patient ne se souvient pas de l’agent précis en cause mais évoque une allergie au curare, il est licite d’éviter la succinylcholine à l’induction en raison du risque d’allergies croisées. Plusieurs solutions peuvent être envisagées. Si une technique d’anesthésie loco-régionale est possible elle sera proposée et recommandée au patient tout en se méfiant des vomissements possibles après anesthésie rachidienne d’où l’abstention d’une sédation complémentaire. Quand une anesthésie générale est rendue nécessaire par le geste chirurgical ou le terrain du patient (anesthésie rachidienne et prise d’anticoagulants), on utilisera l’association propofol-alfentanil, propofol-rémifentanil voire une intubation première sous contrôle fibroscopique. Si les tests cutanés étaient négatifs aux curares, le risque allergique est faible et la succinylcholine peut être employée (13). Dans tous les en urgence, quand il n’existe pas d’agent causal clairement identifié il est plus prudent de travailler dans un environnement sans latex (1), voire d’éviter toute utilisation d’agents histaminolibérateurs et de chlorhexidine.
3.2 notion d’allergie à un médicament non impliqué en anesthésie
En revanche les antécédents allergiques, en dehors des agents employés en anesthésie, ne sont pas une contre indication à l’utilisation de succinylcholine car le pourcentage d’allergie aux curares n’est pas plus élevé dans une population d’allergiques que dans une population témoin. Comme le souligne les recommandations pour la pratique clinique, un patient atopique et/ou allergique à un produit qui ne sera pas utilisé pendant l’anesthésie ne doit pas être considéré comme à risque d’anaphylaxie peranesthésique. Il est cependant recommandé d’aborder le problème au cas par cas. Le patient allergique à une seule substance ou un seul médicament pourra bénéficier d’une « crash induction » conventionnelle. En revanche en cas de terrain polyallergique, avec mise en cause de plusieurs familles médicamenteuses, il est recommandé de considérer le sujet comme à risque et d’éviter si possible la succinylcholine en recourant aux techniques alternatives précédemment discutées. L’attention peut être attirée par une notion d’eczéma de contact ou d’éruption cutanée au contact d’agents cosmétiques, de produits d’entretien ménagers ou de lessive. De tels antécédents peuvent faire évoquer une allergie aux ammoniums quaternaires et une éventuelle allergie aux curares
En cas de patient ne se souvenant pas avec précision s’il est allergique, combien de patients parlent d’allergie, en cas de simple intolérance à un médicament, il peut être recommandé après un interrogatoire soigneux de se rapporter à la conduite recommandée au paragraphe précédent.
Au total, ce qui est demandé à l’anesthésiste dans ce type de situation c’est d’apprécier le rapport bénéfice-risque de chaque technique anesthésique. Ainsi on ne blâmera jamais un anesthésique qui a décidé chez un patient allergique à des agents non anesthésiques d’avoir employé de la succinylcholine. En effet le risque allergique aux curares de 1/13000 est probablement inférieur à celui du risque de survenue d’une inhalation ou de vomissements favorisés par une stimulation répétée des structures pharyngo-laryngées sans même évoquer le risque de lésions dentaires. De nombres études ont d’ailleurs clairement démontré que le risque d’inhalation pouvait atteindre 15% en cas d’intubation par une technique autre que la « crash induction » chez le patient à l’estomac plein (14). En revanche chez un patient polyallergique la prudence s’impose et toutes les alternatives à la « crash induction » devront être envisagées en terme de rapport bénéfice-risque. Il est également recommandé à l’anesthésiste de justifier dans la feuille pré anesthésique les éléments l’ayant amené à retenir une technique donnée par rapport à une autre.
RÉFÉRENCES :
(1) Prévention du risque allergique peranesthésique. Ann Fr Anesth Reanim 2002 ; 20:fi 56-fi 69.
(2) Laxenaire MC. Epidémiologie des réactions anaphylactoides peranesthésiques. Quatrième enquète multicentrique (juillet 1994-décembre 1996). Ann Fr Anesth Reanim 1999 ; 18:796-809.
(3) Laxenaire MC, Mertes PM. Anaphylaxis during anaesthesia. Results of a two-year survey in France. Br J Anaesth 2001 ; 87:549-558.
(4) Fisher MM, Baldo BA. Mast cell tryptase in anaesthetic anaphylactoid reactions [see comments]. Br J Anaesth 1998 ; 80:26-29.
(5) Stephens R, Mythen M, Kallis P, Davies DW, Egner W, Rickards A. Two episodes of life-threatening anaphylaxis in the same patient to a chlorhexidine-sulphadiazine-coated central venous catheter. Br J Anaesth 2001 ; 87:306-308.
(6) Garvey LH, Roed-Petersen J, Menne T, Husum B. Danish Anaesthesia Allergy Centre - preliminary results. Acta Anaesthesiol Scand 2001 ; 45:1204-1209.
(7) Laxenaire MC. Substances responsables des chocs anaphylactiques peranesthésiques. Troisième enquète multicentrique française (1992-94). Ann Fr Anesth Reanim 1996 ; 15:1211-1218.
(8) Clergue F, Auroy Y, Pequignot F, Jougla E, Lienhart A, Laxenaire MC. French survey of anesthesia in 1996. Anesthesiology 1999 ; 91:1509-1520.
(9) Scheller MS, Zornow MH, Saidman LJ. Tracheal intubation without the use of muscle relaxants : a technique using propofol and varying doses of alfentanil. Anesth Analg 1994 ; 75:788-793.
(10) Sundman E, Witt H, Sandin R, Kuylenstierna R, Boden K, Ekberg O et al. Pharyngeal function and airway protection during subhypnotic concentrations of propofol, isoflurane, and sevoflurane : volunteers examined by pharyngeal videoradiography and simultaneous manometry. Anesthesiology 2001 ; 95:1125-1132.
(11) Heier T, Guttormsen AB. Anaphylactic reactions during induction of anaesthesia using rocuronium for muscle relaxation : a report including 3 cases [In Process Citation]. Acta Anaesthesiol Scand 2000 Aug ;44 :775 -81 44:775-781.
(12) Rose M, Fisher M. Rocuronium : high risk for anaphylaxis ? Br J Anaesth 2001 ; 86(5):678-682.
(13) Thacker MA, Davis FM. Subsequent general anaesthesia in patients with a history of previous anaphylactoid/anaphylactic reaction to muscle relaxant. Anaesth Intensive Care 1999 ; 27:190-193.
(14) Li J, Murphy-Lavoie H, Bugas C, Martinez J, Preston C. Complications of emergency intubation with and without paralysis. Am J Emerg Med 1999 ; 17:141-143.
Allergie au latex : programmer les patients en début de bloc ne protège pas
Dr Isabelle Catala
29 avril 2019
Soure : medscape.com
Au regard des résultats d’une étude environnementale menée à Strasbourg et présentée à l’occasion du 14ème Congrès Francophone d’Allergologie[1] , la programmation d’un patient allergique au latex en début de bloc ne garantit pas d’abaisser le risque d’allergie en raison de la présence significative d’allergènes du latex dans l’air.
Mesures avant et pendant les interventions
Il est actuellement admis – sans néanmoins de preuve formelle - que la prise en charge chirurgicale des patients allergiques au latex passe par la programmation en première intervention au bloc opératoire associée à l’utilisation d’un environnement sans latex.
Derrière cette recommandation d’usage, on trouve l’idée que l’air du bloc est le moins chargé en particules de latex en début de programmation.
C’est ce qu’a voulu vérifier l’équipe du Dr Charles Tacquard (Strasbourg) en mesurant les taux d’allergènes majeurs du latex (Hev b1, Hevb2, Hev b5 et Hev b6.02) dans l’air d’un bloc ISO 7 grâce à une pompe aspirante munie d’un filtre qui capte les allergènes.
Les mesures ont été effectuées à 4 reprises : avant le programme opératoire (entre 5 h 30 et 7 h 30), entre 7 h 30 et 9 h 30, entre 11 h 30 et 13 h 30 et entre 15 h 30 et 17 h 30. Ces mesures ont été corrélées au nombre de personnes opérées, au nombre de gants latex utilisés et au nombre de personnes présentes en salle.
Allergènes présents dès la première intervention
L’analyse des données obtenues par tests de mesure montre que le taux d’allergène Hev b1 s’établissait à moins de 10 ng/m3 avant la mise en place du programme opératoire. Il passait ensuite pendant les 3 autres périodes à respectivement 75, 68 et 208 ng/m3.
Aucune corrélation n’a été retrouvée entre l’activité chirurgicale et la quantité de Hev b1 en suspension dans l’air.
Les taux d’allergènes Hev b3, Hev b5 et Hev b6.02 étaient inférieurs au seuil détectable dans toutes les mesures.
Pour les auteurs, « alors qu’aucun gant en latex n’a été utilisé pendant la première période (mesure avant le début du programme opératoire), le taux d’allergène est significatif dès l’ouverture du bloc, signe que la pollution peut persister dans le temps.
La programmation du patient allergique en première position du programme opératoire ne garantit donc pas l’absence de contact avec un allergène du latex ».
Outre l’éviction des gants en latex, une prémédication par anti H2 doit donc être systématique puisque le contact avec l’allergène semble inéluctable.
----
Résultats de six années d’exploration en allergo-anesthésie de la région Rhône Alpes Auvergne
Author R.Ferrenq-Dubost, N. Diot Junique, C.Mullet, D.Le Quang
Unité allergo-anesthésie service Pr Piriou, Pierre-Bénite, France
Available online 3 April 2019.
https://doi.org/10.1016/j.reval.2019.02.095
- Introduction
Nous présentons les résultats de six années (2013 à 2018) de bilans allergo-anesthésiques réalisés dans notre unité, chez des patients ayant présenté une réaction anaphylactique per-anesthésique.
- Méthodes
Un total de 317 patients, 198 femmes, 119 hommes, ont bénéficié de tests cutanés (prick et Intra Dermo Réaction IDR) et biologiques (IgE spécifiques et Test d’Activation des Basophiles TAB) pour les produits administrés lors de leur anesthésie. En cas d’administration de curare tous les curares existants ont été testés. En cas d’administration d’amoxicilline/acide clavulanique nous avons testé amoxicilline et amoxicilline/acide clavulanique. 280 patients (88 %) avaient eu un bilan initial lors du choc (dosage tryptasémie et histaminémie).
- Résultats
Au total, 248/280 (88 %) des bilans initiaux ont montré une élévation de la tryptasémie et/ou de l’histaminémie. 240/317 bilans réalisés ont été positifs (79 %) Sur 199 bilans pour les curares, 144/199 bilans ont été positifs (72 %) dont 87 (60 %) pour la succinylcholine. 58/144 (40 %) patients présentaient une allergie croisée à d’autres curares Sur 119 bilans pour une bêtalactamine, 69/119 bilans ont été positifs (57 %). Pendant l’année 2018 20/29 bilans pour les bêtalactamines ont été positifs (68 %). 40 bilans se sont révélés positifs pour d’autres molécules (15 Bleu Patenté mais 4 en 2017–2018, 6 latex, 5 méthylprednisolone, 4 ranitidine, 3 morphine, 1 suggamadex…). 56 bilans (17 %) ont été négatifs et correspondent à des réactions non IgE dépendantes.
- Discussion
La dernière enquête du GERAP(sur 2011–2012) montre 68 % de bilan positif, nous en trouvons dans notre unité 79 %. Au total, 72 % de nos bilans curares sont positifs contre 61 % pour le GERAP. Nous notons aussi une nette augmentation des réactions aux bêtalactamines notamment en 2018 par rapport aux résultats du GERAP. La prédominance féminine reste d’actualité 198/317 patients (62 %).
- Conclusion
Nos résultats confirment que la plupart des accidents anaphylactiques per-anesthésiques restent dus aux myorelaxants en particulier à la succinylcholine. Les accidents aux bêtalactamines sont en progression, et les réactions au Bleu Patenté sont en diminution. Les réactions au latex sont rares (2 %).
Revue Française d’Allergologie
Volume 59, Issue 3, April 2019, Page 271
§§§
Arnaud BASSEZ
IADE- formateur AFGSU
Administrateur